Tiacetazone
| Tiacetazone | |
|---|---|
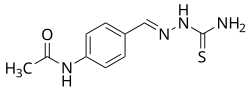 | |
| Nome IUPAC | |
| N-{4-[(etantioamidoimmino)metil]fenil}acetammide | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C10H12N4OS |
| Massa molecolare (u) | 236,3 |
| Numero CAS | |
| Numero EINECS | 203-170-6 |
| Codice ATC | J04 |
| PubChem | 9568512 |
| DrugBank | DB12829 |
| SMILES | O=C(Nc1ccc(cc1)\C=N\NC(=S)N)C |
| Dati farmacologici | |
| Modalità di somministrazione | Orale |
| Dati farmacocinetici | |
| Legame proteico | 95% |
| Emivita | 15-16 ore |
| Escrezione | Renale,in minima parte fecale |
| Indicazioni di sicurezza | |
Il tiacetazone è un tiosemicarbazone derivato dai sulfamidici contenenti tiadiazolo, ma risulta meno tossico e più efficace di questi ultimi.
Farmacodinamica[modifica | modifica wikitesto]
Il farmaco ha attività di tipo batteriostatico, in particolare nei confronti dei micobatteri.
Il suo meccanismo d'azione non è stato ancora totalmente identificato: gli studiosi ritengono che il composto formi con il rame complessi che interferiscono con gli enzimi trasportatori contenenti rame.
Altri ricercatori ritengono che tiacetazone inibisca la ciclopropanazione dell'acido micolico, una miscela complessa di acidi grassi a lunga catena ramificata, che rappresentano dei componenti chiave della parete cellulare idrofoba dei micobatteri.[1]
Il tiacetazone è attivo nei confronti della maggior parte dei ceppi di Mycobacterium tuberculosis, anche se la sensibilità al farmaco appaia variabile nelle diverse zone del mondo. La MIC (concentrazione minima inibente) per le specie sensibili si aggira normalmente intorno a 0,4 mg/l.[2]
Il tiacetazone è attivo anche nei confronti del Mycobacterium leprae (MIC 0,2 mg/l) e del Mycobacterium bovis.[3]
La resistenza al composto è un fenomeno che si sviluppa con relativa frequenza quando viene somministrato in monoterapia. Non è stata segnalata l'esistenza di resistenza crociata con i micobatteri resistenti all'isoniazide. Questo fenomeno invece si verifica tra tiacetazone ed altri farmaci antitubercolari (etionamide, tiocarlide o protionamide).
Farmacocinetica[modifica | modifica wikitesto]
A seguito di somministrazione per via orale l'assorbimento di tiacetazone da parte del tratto gastroenterico avviene con molta gradualità e lentezza. L'assunzione di una dose orale di 150 mg di farmaco determina il raggiungimento di concentrazioni plasmatiche pari a 1,6-3,2 mg/l nel giro di 4-5 ore. L'emivita plasmatica è di 15-16 ore.[4]
Il legame con le proteine plasmatiche raggiunge il 95%. Il tiacetazone viene metabolizzato principalmente mediante una combinazione di idrolisi e deacetilazione. Sono stati finora identificati 4 metaboliti: 4-aminobenzaldeide tiosemicarbazone, 4-acetilaminobenzaldeide, 4-aminobenzaldeide e acido 4-acetilaminobenzoico. L'eliminazione dall'organismo avviene attraverso l'emuntorio renale e solo in piccola quantità attraverso le feci.[5][6]
Tossicologia[modifica | modifica wikitesto]
Studi sperimentali negli animali (topo) hanno evidenziato una DL50 pari a 1000–2000 mg/kg peso corporeo, quando somministratato per via sottocutanea.
Usi clinici[modifica | modifica wikitesto]
Il tiacetazone trova indicazione nella trattamento della tubercolosi polmonare sostenuta da Mycobacterium tuberculosis. Le terapie a base di tiacetazone sono meno efficaci rispetto a quelle a più breve durata raccomandate dall'Unione Internazionale contro la Tubercolosi. Secondo l'Organizzazione Mondiale della Sanità (OMS) il tiacetazone può essere impiegato, associato ad altri farmaci antitubercolari, nei Paesi in via di sviluppo per ridurre la spesa farmaceutica.
Effetti collaterali e indesiderati[modifica | modifica wikitesto]
Si possono comunemente verificare disturbi gastrointestinali (nausea, anoressia, aumento della salivazione, vomito, dolore addominale e diarrea) ed epatici (ittero e aumento dei livelli delle transaminasi AST e ALT), reazioni di ipersensibilità cutanea (rash cutanei, prurito, eruzioni acneiformi ed eritema morbilliforme), congiuntivite, vertigini, sordità e atassia, la maggior parte dei quali scompare alla sospensione della terapia.[7]
Tuttavia alcune reazioni di ipersensibilità cutanea come necrolisi epidermica tossica (sindrome di Lyell) e dermatite esfoliativa, sono talvolta risultate fatali.[8][9][10][11] È stata segnalata anche la comparsa della sindrome di Stevens-Johnson.[12][13][14][15][16]
È stato segnalato che nei soggetti sieropositivi a HIV si verificano con maggiore frequenza diverse reazioni avverse a farmaci antitubercolari, tiacetazone compreso, e in particolare, reazioni cutanee di ipersensibilità.[17][18][19]
Altri effetti collaterali includono epilessia, movimenti coreiformi e altri disturbi neurologici.[20] Il farmaco può provocare depressione midollare con leucopenia, agranulocitosi e trombocitopenia. Si possono verificare anche edema cerebrale, anemia emolitica e un lieve stato di anemia, che si sviluppa in un'alta percentuale di pazienti.[21]
Controindicazioni[modifica | modifica wikitesto]
Il farmaco è controindicato nei pazienti con ipersensibilità individuale nota al principio attivo oppure ad uno degli eccipienti della formulazione farmaceutica.
È inoltre controindicato nei soggetti affetti da malattie epatiche o da insufficienza renale.
Il farmaco deve essere utilizzato con cautela in caso di trattamento di associazione che preveda l'utilizzo di streptomicina, dal momento che ne può aumentare l'ototossicità.[20]
È necessario, se possibile, misurare i livelli plasmatici di transaminasi (AST, ALT) prima dell'inizio della terapia e mantenerli monitorati durante tutto il trattamento.
Dosi terapeutiche[modifica | modifica wikitesto]
Nelle varie fasi della terapia antitubercolare il tiacetazone viene comunemente utilizzato in associazione ad altri agenti antimicrobici (in genere isoniazide, streptomicina, rifampicina ed altre sostanze).
Il farmaco nel soggetto adulto viene somministrato per via orale alla dose di 150 mg al giorno. Nel bambino la dose prevede l'assunzione di 4 mg/kg peso corporeo al giorno.
Al fine di non diminuire l'efficacia del trattamento viene raccomandato il rigoroso rispetto della somministrazione giornaliera. In un regime terapeutico dopo una fase iniziale di trattamento che prevede l'utilizzo di streptomicina, isoniazide, rifampicina e pirazinamide, il tiacetazone può essere associato all'isoniazide per un periodo di 6 mesi.
Secondo un altro regime terapeutico il tiacetazone può essere usato nella fase iniziale del trattamento in associazione a isoniazide e streptomicina.
Il farmaco è stato impiegato anche nel trattamento della lebbra,[22] ma viene considerato dall'Organizzazione Mondiale della Sanità inappropriato per i regimi terapeutici a breve termine basati sull'uso di associazioni di farmaci.
Interazioni[modifica | modifica wikitesto]
- Streptomicina: il trattamento di associazione con tiacetazone può aumentarne l'ototossicità.[20]
Note[modifica | modifica wikitesto]
- ^ A. Alahari, X. Trivelli; Y. Guérardel; LG. Dover; GS. Besra; JC. Sacchettini; RC. Reynolds; GD. Coxon; L. Kremer, Thiacetazone, an antitubercular drug that inhibits cyclopropanation of cell wall mycolic acids in mycobacteria., in PLoS One, vol. 2, n. 12, 2007, pp. e1343, DOI:10.1371/journal.pone.0001343, PMID 18094751.
- ^ GA. Ellard, JM. Dickinson; PT. Gammon; DA. Mitchison, Serum concentrations and antituberculosis activity of thiacetazone., in Tubercle, vol. 55, n. 1, Mar 1974, pp. 41-54, PMID 4143449.
- ^ MJ. Colston, GR. Hilson; RD. Lancaster, Intermittent chemotherapy of experimental leprosy in mice., in Am J Trop Med Hyg, vol. 29, n. 1, Gen 1980, pp. 103-8, PMID 6153254.
- ^ CA. Peloquin, AT. Nitta; SE. Berning; MD. Iseman; GT. James, Pharmacokinetic evaluation of thiacetazone., in Pharmacotherapy, vol. 16, n. 5, pp. 735-41, PMID 8888068.
- ^ PJ. Jenner, GA. Ellard; OB. Swai, A study of thiacetazone blood levels and urinary excretion in man, using high performance liquid chromatography., in Lepr Rev, vol. 55, n. 2, Giu 1984, pp. 121-8, PMID 6205236.
- ^ MR. Holdiness, Clinical pharmacokinetics of the antituberculosis drugs., in Clin Pharmacokinet, vol. 9, n. 6, pp. 511-44, DOI:10.2165/00003088-198409060-00003, PMID 6391781.
- ^ CA. Pearson, Thiacetazone toxicity in the treatment of tuberculosis patients in Nigeria., in J Trop Med Hyg, vol. 81, n. 12, Dic 1978, pp. 238-42, PMID 85717.
- ^ TR. Bedi, OP. Singh; LK. Bhutani, Acute epidermal necrolysis (Lyell syndrome) induced by thiacetazone., in Indian J Chest Dis, vol. 16, n. 1, Gen 1974, pp. 55-7, PMID 4138214.
- ^ D. Mame Thierno, S. On; S. Thierno Ndiaye; B. Ndiaye, [Lyell syndrome in Senegal: responsibility of thiacetazone]., in Ann Dermatol Venereol, vol. 128, n. 12, Dic 2001, pp. 1305-7, PMID 11908132.
- ^ SA. Hussain, HC. Saksena; RP. Kothari, Stevens-Johnson syndrome due to thiacetazone., in J Indian Med Assoc, vol. 60, n. 2, Gen 1973, pp. 57-9, PMID 4123241.
- ^ MT. Dieng, B. Ndiaye; C. Camara, [Skin toxicity of thiacetazone (TB1) at a hospital service in Dakar]., in Dakar Med, vol. 46, n. 1, 2001, pp. 1-3, PMID 15773145.
- ^ VN. Ingle, Q. Banoo, Stevens-Johnson syndrome associated with administration of a combination of isonicotinic acid hydrazide and thiacetazone., in Indian Pediatr, vol. 2, n. 8, Ago 1965, pp. 305-7, PMID 4158699.
- ^ SP. Sahi, K. Chandra, Thiacetazone induced Steven-Johnson syndrome: a case report., in Indian J Chest Dis, vol. 16, n. 2, Apr 1974, pp. 124-5, PMID 4138166.
- ^ P. Blom, [Stevens-Johnson syndrome as a complication in tuberculosis treatment with thioacetazon]., in Ned Tijdschr Geneeskd, vol. 135, n. 52, Dic 1991, pp. 2492-3, PMID 1722029.
- ^ JJ. Wirima, AD. Harries, Stevens-Johnson syndrome during anti-tuberculosis chemotherapy in HIV-seropositive patients: report on six cases., in East Afr Med J, vol. 68, n. 1, Gen 1991, pp. 64-6, PMID 2060484.
- ^ A. Okwera, JL. Johnson; MJ. Vjecha; K. Wolski; CC. Whalen; D. Hom; R. Huebner; RD. Mugerwa; JJ. Ellner, Risk factors for adverse drug reactions during thiacetazone treatment of pulmonary tuberculosis in human immunodeficiency virus infected adults., in Int J Tuberc Lung Dis, vol. 1, n. 5, Ott 1997, pp. 441-5, PMID 9441099.
- ^ CP. Theuer, PC. Hopewell; D. Elias; GF. Schecter; GW. Rutherford; RE. Chaisson, Human immunodeficiency virus infection in tuberculosis patients., in J Infect Dis, vol. 162, n. 1, Lug 1990, pp. 8-12, PMID 1972384.
- ^ PF. Barnes, AB. Bloch; PT. Davidson; DE. Snider, Tuberculosis in patients with human immunodeficiency virus infection., in N Engl J Med, vol. 324, n. 23, Giu 1991, pp. 1644-50, DOI:10.1056/NEJM199106063242307, PMID 2030721.
- ^ MR. Holdiness, Adverse cutaneous reactions to antituberculosis drugs., in Int J Dermatol, vol. 24, n. 5, Giu 1985, pp. 280-5, PMID 2410379.
- ^ a b c MR. Holdiness, Neurological manifestations and toxicities of the antituberculosis drugs. A review., in Med Toxicol, vol. 2, n. 1, pp. 33-51, PMID 3547005.
- ^ WH. Jopling, Side-effects of antileprosy drugs in common use., in Lepr Rev, vol. 54, n. 4, Dic 1983, pp. 261-70, PMID 6199637.
- ^ Antileprosy drugs., in Br Med J, vol. 3, n. 5767, Lug 1971, pp. 174-6, PMID 4104273.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su tiacetazone
Wikimedia Commons contiene immagini o altri file su tiacetazone