Sinensetina
| Sinensetina | |
|---|---|
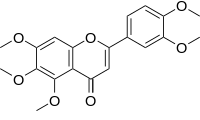 | |
| Nome IUPAC | |
| 2-(3,4-dimetossfenil)-5,6,7-trimetossicromene-4-one | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C20H20O7 |
| Massa molecolare (u) | 372,36 g/mol |
| Numero CAS | |
| Numero EINECS | 803-609-7 |
| PubChem | 145659 |
| SMILES | COC1=C(C=C(C=C1)C2=CC(=O)C3=C(C(=C(C=C3O2)OC)OC)OC)OC |
| Dati farmacocinetici | |
| Biodisponibilità | % |
| Emivita | ore |
| Indicazioni di sicurezza | |
La sinensetina o 5,6,7,3',4'-pentametossiflavone è un flavone metilato simile ai flavoni naturali apigenina, luteolina e ai flavoni sintetici diosmina e flavossato. Si può trovare nella pianta Orthosiphon stamineus, insieme al flavonoide eupatorina, pianta conosciuta anche come il tè di Giava e introdotta in Occidente nel XX secolo.[1]
Proprietà fitoterapiche[modifica | modifica wikitesto]
La sinensetina ha un metile, nella molecola del flavonoide, in posizione C3, ciò garantirebbe alla sostanza notevoli proprietà antiangiogenetiche; a fronte di una minore tossicità dovuta alla mancanza del gruppo metile in posizione C8.[2]
Gli estratti alcolici di Orthosiphon stamineus (sinensetina) hanno due enzimi: α-glucosidasi e α-amilasi che conferiscono all'estratto proprietà antidiabetiche nel diabete non insulino-dipendente.[3]
La sinensetina vanta proprietà antinfiammatorie[4][5] e antipiretiche.[6]
Una proprietà della sinensetina unica è la capacità di prevenire e/o migliorare il trattamento dell'obesità, attraverso una proprietà di downregulation della via metabolica mediata dal SREBP1c (Sterol Regulatory Element-Binding Protein che influenzano la trascrizione del DNA) e, inoltre, essa aumenta la fosforilazione della proteina chinasi A e lipasi ormone-sensibile, ciò indica proprietà lipolitiche per la sinensetina tramite una via di segnalazione metabolica cAMP-mediata.[7]
Una proprietà studiata molto interessante della sostanza consiste nella capacità di ridurre i meccanismi di segnale delle cellule batteriche e la loro adesività (quorum sensing).[8]
Diverse ricerche in vitro mostrano per la sinensetina proprietà antimutageniche[9][10][11] proprietà che farebbero intravedere per la sostanza capacità chemiopreventive,[12][13] in assenza di proprietà genotossiche.[14] Inoltre, una ricerca del 2002 indica proprietà chemiosensibilizzanti per la sinensetina ai farmaci antitumorali, con il vantaggio anche di avere un elevato indice terapeutico, di essere un inibitore non trasportabile, e di non indurre la glicoproteina-P.[15]
Note[modifica | modifica wikitesto]
- ^ G.A. Akowuah, Z. Ismail, I. Norhayati e A. Sadikun, The effects of different extraction solvents of varying polarities on polyphenols of Orthosiphon stamineus and evaluation of the free radical-scavenging activity, in Food Chemistry, vol. 93, n. 2, 2005, p. 311, DOI:10.1016/j.foodchem.2004.09.028.
- ^ Lam IK, Alex D, Wang YH, et al., In vitro and in vivo structure and activity relationship analysis of polymethoxylated flavonoids: identifying sinensetin as a novel antiangiogenesis agent, in Mol Nutr Food Res, vol. 56, n. 6, giugno 2012, pp. 945–56, DOI:10.1002/mnfr.201100680, PMID 22707269.
- ^ Mohamed EA, Siddiqui MJ, Ang LF, et al., Potent α-glucosidase and α-amylase inhibitory activities of standardized 50% ethanolic extracts and sinensetin from Orthosiphon stamineus Benth as anti-diabetic mechanism, in BMC Complement Altern Med, vol. 12, 2012, p. 176, DOI:10.1186/1472-6882-12-176, PMC 3533584, PMID 23039079.
- ^ Shin HS, Kang SI, Yoon SA, Ko HC, Kim SJ, Sinensetin attenuates LPS-induced inflammation by regulating the protein level of IκB-α, in Biosci. Biotechnol. Biochem., vol. 76, n. 4, 2012, pp. 847–9, PMID 22484952.
- ^ Laavola M, Nieminen R, Yam MF, et al., Flavonoids eupatorin and sinensetin present in Orthosiphon stamineus leaves inhibit inflammatory gene expression and STAT1 activation, in Planta Med., vol. 78, n. 8, maggio 2012, pp. 779–86, DOI:10.1055/s-0031-1298458, PMID 22516932.
- ^ Yam MF, Ang LF, Basir R, Salman IM, Ameer OZ, Asmawi MZ, Evaluation of the anti-pyretic potential of Orthosiphon stamineus Benth standardized extract, in Inflammopharmacology, vol. 17, n. 1, febbraio 2009, pp. 50–4, DOI:10.1007/s10787-008-8038-3, PMID 19127348.
- ^ Kang SI, Shin HS, Ko HC, Kim SJ, Effects of sinensetin on lipid metabolism in mature 3T3-L1 adipocytes, in Phytother Res, vol. 27, n. 1, gennaio 2013, pp. 131–4, DOI:10.1002/ptr.4683, PMID 22438091.
- ^ Vikram A, Jayaprakasha GK, Jesudhasan PR, Pillai SD, Patil BS, Suppression of bacterial cell-cell signalling, biofilm formation and type III secretion system by citrus flavonoids, in J. Appl. Microbiol., vol. 109, n. 2, agosto 2010, pp. 515–27, DOI:10.1111/j.1365-2672.2010.04677.x, PMID 20163489.
- ^ Miyazawa M, Okuno Y, Fukuyama M, Nakamura S, Kosaka H, Antimutagenic activity of polymethoxyflavonoids from Citrus aurantium, in J. Agric. Food Chem., vol. 47, n. 12, dicembre 1999, pp. 5239–44, PMID 10606602.
- ^ (ZH) Dong Y, Ji G, Cao A, et al., [Effects of sinensetin on proliferation and apoptosis of human gastric cancer AGS cells], in Zhongguo Zhong Yao Za Zhi, vol. 36, n. 6, marzo 2011, pp. 790–4, PMID 21710752.
- ^ Androutsopoulos VP, Ruparelia K, Arroo RR, Tsatsakis AM, Spandidos DA, CYP1-mediated antiproliferative activity of dietary flavonoids in MDA-MB-468 breast cancer cells, in Toxicology, vol. 264, n. 3, ottobre 2009, pp. 162–70, DOI:10.1016/j.tox.2009.07.023, PMID 19666078.
- ^ Zhou DY, Zhang XL, Xu Q, Xue XY, Zhang FF, Liang XM, UPLC/Q-TOFMS/MS as a powerful technique for rapid identification of polymethoxylated flavones in Fructus aurantii, in J Pharm Biomed Anal, vol. 50, n. 1, agosto 2009, pp. 2–8, DOI:10.1016/j.jpba.2009.03.010, PMID 19428213.
- ^ Walle UK, Walle T, Bioavailable flavonoids: cytochrome P450-mediated metabolism of methoxyflavones, in Drug Metab. Dispos., vol. 35, n. 11, novembre 2007, pp. 1985–9, DOI:10.1124/dmd.107.016782, PMID 17709371.
- ^ Delaney B, Phillips K, Vasquez C, et al., Genetic toxicity of a standardized mixture of citrus polymethoxylated flavones, in Food Chem. Toxicol., vol. 40, n. 5, maggio 2002, pp. 617–24, PMID 11955667.
- ^ Choi CH, Sun KH, An CS, et al., Reversal of P-glycoprotein-mediated multidrug resistance by 5,6,7,3',4'-pentamethoxyflavone (Sinensetin), in Biochem. Biophys. Res. Commun., vol. 295, n. 4, luglio 2002, pp. 832–40, PMID 12127970.
Bibliografia[modifica | modifica wikitesto]
- Hildebert H. Wagner, Plant Drug Analysis.: A Thin Layer Chromatography Atlas., Springer, 1996, pp. 232–, ISBN 978-3-540-58676-0.
- Fereidoon Shahidi, Dried Fruits: Phytochemicals and Health Effects, John Wiley & Sons, 18 dicembre 2012, pp. 1–, ISBN 978-1-118-46464-9.
- Yongping Bao e Roger Fenwick, Phytochemicals in Health and Disease, CRC Press, 24 maggio 2004, pp. 172–, ISBN 978-0-8247-5187-6.
- Danielle Julie Carrier, Chantal Bergeron e Shri Ramaswamy, Biorefinery Co-Products: Phytochemicals, Primary Metabolites and Value-Added Biomass Processing, John Wiley & Sons, 23 aprile 2012, pp. 159–, ISBN 978-0-470-97357-8.