Ciclo del carbonio

In biologia e chimica ambientale il ciclo del carbonio è il ciclo biogeochimico attraverso il quale il carbonio viene scambiato tra la geosfera (all'interno della quale si considerano i sedimenti e i combustibili fossili), l'idrosfera (mari e oceani), la biosfera (comprese le acque dolci) e l'atmosfera della Terra. Tutte queste porzioni della Terra sono considerabili a tutti gli effetti serbatoi di carbonio (carbon sinks).
Il ciclo è infatti solitamente inteso come l'interscambio dinamico tra questi quattro distretti con le dinamiche di interscambio legate a processi chimici, fisici, geologici e biologici. Il bilancio globale del carbonio è il bilancio degli scambi (entrate e perdite) tra le riserve di carbonio o tra uno specifico ciclo (ad es. atmosfera-biosfera) del ciclo del carbonio; un esame del bilancio su una riserva può fornire informazioni se questa stia funzionando da fonte o da consumatore dei biossidi di carbonio. Sembra inoltre che anche altri corpi celesti possano avere un ciclo del carbonio, ma esistono pochissime informazioni al riguardo.
Carbonio nella biosfera[modifica | modifica wikitesto]

Circa 1500 miliardi di tonnellate di carbonio sono presenti nella biosfera. Il carbonio è parte essenziale della vita sulla Terra. Esso gioca un ruolo importante nella struttura, biochimica e nutrizione di tutte le cellule viventi. E la vita gioca un ruolo importante nel ciclo del carbonio:
- Gli organismi autotrofi sono organismi che producono i loro composti organici usando il biossido di carbonio tratto dall'aria o dall'acqua in cui vivono. Quasi tutti gli autotrofi usano la radiazione solare a questo scopo e il loro processo di produzione viene chiamato fotosintesi. Un piccolo numero di autotrofi sfrutta fonti di energia chimica (in questo caso si parla di chemiosintesi). Gli autotrofi più importanti per il ciclo del carbonio sono gli alberi delle foreste sulla terraferma e il fitoplancton negli oceani. La fotosintesi clorofilliana segue la reazione 6CO2 + 6H2O → C6H12O6 + 6O2
- Il carbonio viene trasferito nella biosfera quando gli organismi eterotrofi si nutrono di altri organismi o di loro parti (ad esempio i frutti). Questo comprende l'assorbimento di materiale organico morto da parte di funghi e batteri, che producono fermentazione o decomposizione.
- Gran parte del carbonio lascia la biosfera attraverso la respirazione. Quando è presente l'ossigeno, si ha la respirazione aerobica, che rilascia biossido di carbonio nell'aria o nell'acqua circostante, seguendo la reazione C6H12O6 + 6O2 → 6CO2 + 6H2O. Altrimenti si ha la respirazione anaerobica, con rilascio di metano nell'ambiente circostante, il quale giunge fino all'atmosfera o all'idrosfera (ad esempio con i gas di palude o la flatulenza).
- La combustione di biomassa (ad esempio incendi boschivi, o legna usata per il riscaldamento) può trasferire anch'essa un sostanziale quantitativo di carbonio nell'atmosfera.[1]
L'immagazzinamento di carbonio nella biosfera è influenzato da diversi processi che si attuano su varie scale temporali: mentre la produttività primaria netta segue un ciclo diurno e stagionale, il carbonio può essere immagazzinato per diverse centinaia di anni negli alberi e fino a migliaia di anni nel suolo. Cambiamenti in questi bacini di carbonio a lungo termine (ad esempio attraverso la deforestazione o l'afforestazione, o attraverso cambiamenti nella respirazione del suolo, legati alla temperatura) possono influenzare direttamente il riscaldamento globale.
Carbonio nella geosfera[modifica | modifica wikitesto]
Il carbonio può anche lasciare la biosfera, quando la materia organica morta (come la torba o le conchiglie) sedimenta e viene ricoperta da altri depositi sedimentari, viene incorporata nella geosfera.
Il carbonio negli oceani[modifica | modifica wikitesto]
- Le conchiglie, fatte di carbonato di calcio, possono trasformarsi in calcare attraverso il processo di sedimentazione.
- Molto si deve ancora apprendere sul ciclo del carbonio nell'oceano profondo. Ad esempio, una recente scoperta è che le bolle di muco delle Appendicolarie (dette "case") vengono create in quantità talmente grande che possono fornire una quantità di carbonio all'oceano profondo pari a quella rilevata in precedenza dalle trappole per sedimenti[2]. A causa della loro dimensione e composizione, queste "case" raramente vengono raccolte da tali trappole, quindi gran parte delle analisi biogeochimiche le hanno erroneamente ignorate.
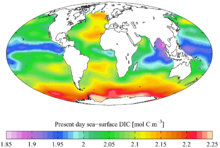
I mari contengono circa 36.000 miliardi di tonnellate di carbonio, in gran parte sotto forma di ione bicarbonato. La presenza di carbonio inorganico, rappresentato da gruppi di carbonio senza legami carbonio-carbonio o carbonio-idrogeno, è importante per le sue reazioni in acqua. Questo scambio di carbonio diventa importante nel controllare il pH degli oceani e può comportarsi sia come sorgente che come assorbente di carbonio a seconda delle condizioni. Il carbonio è scambiato rapidamente tra atmosfera e oceano. Nelle regioni oceaniche di upwelling, il carbonio viene rilasciato verso l'atmosfera. Al contrario, nelle regioni di downwelling il trasferimento di carbonio (CO2) avviene tra atmosfera e oceano. Quando esso è assorbito dall'oceano avviene la formazione di acido carbonico:
- CO2 + H2O ⇌ H2CO3
Questa reazione può avvenire in entrambe le direzioni, fino a raggiungere l'equilibrio chimico. Un'altra importante reazione che determina il pH oceanico è il rilascio di ioni idrogeno e bicarbonato:
- H2CO3 ⇌ H+ + HCO3-
Geochimica isotopica e ciclo del carbonio[modifica | modifica wikitesto]
Il carbonio in natura è presente in due isotopi stabili, 12C e 13C. Lungo il ciclo del carbonio, le specie che lo contengono subiscono trasformazioni chimiche e fisiche; queste causano un frazionamento isotopico, che modifica l'abbondanza isotopica nei diversi serbatoi di carbonio.
L'anidride carbonica nell'atmosfera ha un valore di δ13C = -10‰ ÷ -6‰ V-PDB (cioè il suo rapporto di abbondanza di 13C su 12C è del 10‰ ÷ 6‰ più basso rispetto al rapporto nello standard Pee-Dee Belemnitella).
L'anidride carbonica disciolta nell'acqua degli oceani, sotto forma di bicarbonato in equilibrio chimico con l'atmosfera, ha un valore di δ13C = +0,5‰ ÷ +0,1‰ V-PDB; questo perché a 20÷25 °C il fattore di arricchimento isotopico dalla fase gassosa alla fase disciolta è (le molecole contenenti 13C si disciolgono più facilmente in acqua rispetto a quelle contenenti 12C).
Anche nel processo di precipitazione dei carbonati le molecole contenenti 13C sono favorite: il fattore di arricchimento è leggermente positivo ( a 20 °C), così che i carbonati marini hanno un valore δ13C = +1‰ ÷ +2‰ V-PDB.
Al contrario, il processo di fotosintesi avviene più facilmente con molecole contenenti 12C (gli atomi 13C formano legami più forti, e più difficili da spezzare); il carbonio organico prodotto dalle piante (in particolare dalle piante C3 terrestri) risulta impoverito in 13C rispetto all'anidride carbonica atmosferica (δ13C = -35‰ ÷ -22‰ V-PDB). Valori un po' più alti (δ13C = -23‰ ÷ -5‰ V-PDB) si hanno nel caso delle piante C4 o delle piante grasse, il cui metabolismo genera un frazionamento meno marcato, o nel caso delle alghe o delle piante acquatiche, poiché fissano il carbonio disciolto in acqua che, come visto sopra, è più ricco in 13C rispetto a quello atmosferico.
Nel suolo la decomposizione della materia organica porta alla produzione di anidride carbonica che, data la sua provenienza, ha un contenuto di 13C inferiore a quello dell'anidride carbonica atmosferica (δ13C = -26‰ ÷ -22‰ V-PDB, vicino a quello della materia organica dalla quale ha avuto origine). Per questo il bicarbonato disciolto nelle falde acquifere ha un contenuto isotopico molto variabile: si va dall'estremo nel quale tutto il bicarbonato viene dalla soluzione di CO2 di origine organica (δ13C = -25‰ + 9‰ = -16‰ V-PDB) all'estremo opposto nel quale la CO2 è tutta di origine atmosferica (δ13C = -8‰ + 9‰ = +1‰ V-PDB); nel caso di interazione con carbonati (che come visto prima hanno valori intorno a δ13C = 1‰ ÷ +2‰ V-PDB) il bicarbonato disciolto avrà un'abbondanza isotopica che va da δ13C = -13‰ a -10‰ V-PDB.
Anche la metanogenesi operata dai batteri metanogeni è un processo che causa un importante frazionamento isotopico: le molecole contenenti 12C reagiscono molto più facilmente, conferendo a questo processo un notevole fattore di arricchimento che va da -50‰ a -90‰. Grazie a questo fatto è possibile distinguere il metano biogenico (che presenta valori di δ13C molto bassi) da quello abiogenico (con valori δ13C più prossimi allo 0).
I modelli del ciclo del carbonio[modifica | modifica wikitesto]
Diversi modelli del ciclo del carbonio possono essere incorporati all'interno del modello globale del clima, in modo da prevedere l'effetto di interazione dei futuri livelli di CO2 sugli oceani e sulla biosfera. Ci sono, comunque, considerevoli dubbi sulla loro effettiva correttezza, sia per quanto riguarda i modelli fisici che biochimici (specialmente quest'ultimo). Tali sistemi mostrano che c'è una relazione diretta tra temperatura e CO2. Ad esempio alcuni ricercatori[3] hanno mostrato che nel loro modello, includendo il ciclo del carbonio, aumenta la quantità di CO2 nell'atmosfera di circa 90 ppmv a 2100 (superiore al valore predetto dai modelli con un ciclo del carbonio non interattivo), portando ad un ulteriore aumento di 0,6 °C del riscaldamento (che, a sua volta, può provocare un ulteriore aumento della quantità di CO2 atmosferico).
Attività umana[modifica | modifica wikitesto]

Sin dagli inizi della Rivoluzione industriale, l'attività umana ha avuto un certo impatto sul ciclo del carbonio, cambiandone alcune fasi del ciclo ed arrivando a rilasciare direttamente nell'atmosfera del carbonio.
La principale e più evidente prova dell'influenza umana su questo ciclo è costituita dalle emissioni di gas di scarico prodotti dalla combustione dei combustibili fossili, che trasferiscono carbonio dalla geosfera all'atmosfera. Questi scarichi influenzano il ciclo del carbonio indirettamente, modificando la biosfera terrestre e quella oceanica.
Nel corso dei secoli, l'alterazione dei terreni adoperata dall'uomo ha comportato una perdita importante dal punto di vista della biodiversità, diminuendo la capacità degli ecosistemi di resistere agli stress ambientali e, pertanto, riducendo le possibilità di un dato ambiente di rimuovere il carbonio in eccesso dall'atmosfera. Più direttamente, può capitare che il carbonio venga riemesso nell'atmosfera, aggravando ulteriormente la situazione. Un altro grave problema è rappresentato dalla progressiva deforestazione. Gli alberi sono in grado di trattenere grandi quantità di carbonio e la loro rimozione, specialmente senza un successivo rimboschimento, fa sì che quantità maggiori di carbonio permangano nell'atmosfera.
Temperature più elevate e livelli di CO2 nell'atmosfera aumentano i tassi di decomposizione nel suolo, restituendo così all'atmosfera la CO2 immagazzinata in materiale vegetale.
Tuttavia, un aumento dei livelli di CO2 nell'atmosfera può anche portare ad una maggiore produzione primaria lorda. Aumenta i tassi di fotosintesi, consentendo alle piante di utilizzare in modo più efficiente l'acqua, perché non hanno più bisogno di lasciare i loro stomi aperti per così lunghi periodi di tempo, in modo da assorbire la stessa quantità di anidride carbonica.
Gli esseri umani influenzano anche il ciclo del carbonio oceanico. Le attuali tendenze dei cambiamenti climatici portano a temperature dell'oceano più elevate, modificando così gli ecosistemi. Inoltre, le piogge acide e il rilascio di agenti inquinanti nelle acque modificano la composizione chimica degli oceani. Tali cambiamenti possono avere effetti drammatici sugli ecosistemi particolarmente sensibili come le barriere coralline, limitando così la capacità dell'oceano di assorbire il carbonio dall'atmosfera su scala regionale e la riduzione della biodiversità oceanica globale, comportando, insieme al riscaldamento globale, una diminuzione dei ghiacci polari e un progressivo aumento del livello dell'acqua lungo le coste.
Note[modifica | modifica wikitesto]
- ^ Comune di Campi Bisenzio, La combustione delle biomasse legnose, su www.comune.campi-bisenzio.fi.it, 15 dicembre 2021. URL consultato il 18 marzo 2023.
- ^ "Sinkers" provide missing piece in deep-sea puzzle Archiviato il 27 settembre 2007 in Internet Archive.
- ^ Zeng et al. (GRL, 2004 [1] Archiviato il 12 febbraio 2007 in Internet Archive.)
Voci correlate[modifica | modifica wikitesto]
- C4MIP
- Acidificazione degli oceani
- Fotosintesi clorofilliana
- Produzione primaria
- Ciclo biogeochimico
- Macroelementi
- Effetto serra
- Riscaldamento globale
- Cattura e sequestro del carbonio
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su ciclo del carbonio
Wikimedia Commons contiene immagini o altri file su ciclo del carbonio
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) carbon cycle, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- (EN) Carbon Cycle Science Program, su carboncyclescience.gov. URL consultato il 2 giugno 2004 (archiviato dall'url originale il 2 giugno 2004).
- (EN) Sito del NASA Earth Observatory describing the carbon cycle
- (EN) Gruppo dei gas a effetto serra del ciclo del carbonio sul sito del NOAA, su cmdl.noaa.gov.
- (EN) UNEP - L'attuale ciclo del carbonio - Cambiamenti climatici, livelli e flussi del carbonio, su grida.no. URL consultato il 12 settembre 2006 (archiviato dall'url originale il 15 settembre 2008).
- (EN) Appenzeller, T. (2004), 'Il caso del carbonio mancante', National Geographic Magazine
- (EN) CarboEurope IP
| Controllo di autorità | LCCN (EN) sh85020105 · GND (DE) 4164552-2 · BNF (FR) cb12135244m (data) · J9U (EN, HE) 987007283487105171 |
|---|


