Immagazzinamento dell'idrogeno

L'immagazzinamento dell'idrogeno (o stoccaggio dell'idrogeno) descrive i metodi per immagazzinare H2 per un successivo utilizzo. Le metodologie spaziano su molti approcci, inclusi l'alta pressione e la criogenica, ma si concentrano solitamente su materiali che rilasciano reversibilmente l'idrogeno tramite il riscaldamento.
L'immagazzinamento dell'idrogeno rappresenta un punto fondamentale nello sviluppo di un'economia dell'idrogeno. La maggior parte della ricerca sull'immagazzinamento dell'idrogeno punta ad una diminuzione del volume di stoccaggio, per applicazioni mobili. Queste ricerche sono importanti anche per il ruolo che potrebbe avere l'idrogeno nel fornire un deposito per l'energia elettrica di fonti non prevedibili, come l'energia eolica. Al giorno d'oggi la principale difficoltà nell'utilizzo dell'idrogeno come sistema di stoccaggio è che le trasformazioni energia→ idrogeno→ energia sono costose e tecnologicamente complesse.
Gli idrocarburi tradizionali sono solitamente immagazzinati dove è previsto il loro utilizzo: lo stoccaggio è possibile sia in fase liquida, nei serbatoi di benzina, gasolio e GPL, sia in fase gassosa, nei serbatoi di propano e metano. L'idrogeno risulta invece molto costoso da stoccare e/o trasportare con le attuali tecnologie.
L'idrogeno presenta una elevata densità di energia per unità di massa, ma scarsa densità energetica volumetrica rispetto agli idrocarburi, richiedendo quindi serbatoi di maggiori dimensioni per il suo deposito. Tali serbatoi sono quindi più pesanti rispetto a quelli degli idrocarburi a parità di contenuto energetico, lasciando invariati tutti gli altri fattori. Aumentare la pressione del gas migliorerebbe la densità di energia per unità di volume, ottenendo contenitori meno ingombranti, ma non più leggeri.[1] Comprimere un gas richiede energia per alimentare il compressore: una compressione più spinta comporta una maggiore perdita di energia durante il processo di compressione.
Alternativamente si potrebbe usare idrogeno liquido (o neve di idrogeno) a più alta densità volumetrica di energia (come nello Space Shuttle). Tuttavia l'idrogeno liquido richiede un immagazzinamento criogenico e bolle a circa 20,268 K (-252,882 °C ovvero -423,188 °F). Quindi la sua liquefazione impone una grande perdita di energia (poiché è richiesta energia per raffreddarlo fino a quelle temperature). I serbatoi devono poi essere ben isolati per evitare l'ebollizione e l'isolante per l'idrogeno liquido è solitamente costoso e delicato. Assumendo tutto questo risolvibile, rimane il problema della densità. L'idrogeno liquido ha densità energetica per unità di volume di circa 4 volte inferiore rispetto ad altri idrocarburi, come la benzina. Questo evidenzia il problema della densità per l'idrogeno puro: vi è effettivamente il 64% in più di idrogeno in un litro di benzina (116 grammi di idrogeno) che in un litro di idrogeno liquido puro (71 grammi). Il carbonio nella benzina inoltre contribuisce attivamente all'energia della combustione.
Proposte e ricerca[modifica | modifica wikitesto]
Stoccaggio sotto forma di ammoniaca[modifica | modifica wikitesto]
L'ammoniaca (NH3) può essere un mezzo per stoccare l'idrogeno chimicamente e dopo liberarlo in un "reformer" catalitico. L'ammoniaca provvede ad un potenziale stoccaggio dell'idrogeno ad alta densità come un liquido raffreddato a temperature inferiori a -35 °C con lieve pressurizzazione ed un modesto isolamento criogenico. In miscela con acqua può essere tranquillamente stoccato a temperatura e pressioni ambientali normali.
I processi industriali dell'ammoniaca sono ampiamente conosciuti, dato che è il secondo prodotto chimico più comunemente prodotto nel mondo, e sono ampiamente disponibili enormi infrastrutture per la produzione, trasporto e distribuzione di essa. L'ammoniaca può essere convertita (reformed) per produrre idrogeno senza la produzione di gas tossici, oppure può essere mescolata con i carburanti esistenti e bruciare efficientemente. L'ammoniaca pura brucia difficilmente a pressioni atmosferiche pari a quelle che si hanno nei forni o negli scaldabagno alimentati a gas naturale. Quando l'ammoniaca viene compressa in un motore a combustione interna diventa un combustibile utile per motori a benzina lievemente modificati. L'ammoniaca è energeticamente molto costosa da produrre e l'infrastruttura esistente dovrebbe essere ingrandita enormemente per poter affrontare le necessità energetiche del sistema dei trasporti.
L'ammoniaca di per sé, alla temperatura di 25 °C e pressione ambiente (760 mmHg) è un gas tossico, ed ha un odore molto pungente e penetrante, oltre ad avere effetti lacrimogeni.
Idruri metallici[modifica | modifica wikitesto]
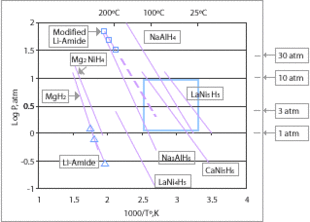
Gli idruri metallici, con differenti gradi di efficienza, possono essere usati come mezzo di stoccaggio dell'idrogeno, spesso reversibilmente.[2] Alcuni sono liquidi a temperatura ambiente e pressione standard, altri sono solidi che possono essere trasformati in sferette. Gli idruri proposti per l'uso nell'economia a idrogeno includono semplici idruri di magnesio o metalli di transizione e idruri metallici complessi, contenenti tipicamente sodio, litio o calcio e alluminio o boro. Questi materiali hanno una buona densità di energia per unità volumetrica, nonostante la loro densità di energia per unità di peso sia spesso peggiore dei più comuni carburanti idrocarburi. Inoltre, sono spesso necessarie alte temperature per il rilascio del loro contenuto di idrogeno.
Lo stoccaggio in idruri solidi è una possibile soluzione per lo stoccaggio automobilistico. Un serbatoio di idruro è circa tre volte più capiente e quattro volte più pesante di un serbatoio di benzina che produce la stessa energia. Per un'automobile standard, si tratta di circa 0,17 m3 di spazio e 270 kg contro 0,057 m3 e 70 kg. Un normale serbatoio di benzina pesa poche decine di chilogrammi ed è costruito in acciaio il cui prezzo è stimato in circa $2,20/kg. Il litio, il costituente principale per peso di un recipiente di stoccaggio di idruri, costa attualmente $90/kg. Ogni idruro necessiterà di essere riciclato o ricaricato con idrogeno, a bordo dell'automobile o in una centrale di riciclo. Una cellula energetica metallo-ossido, per esempio una cellula di carburante zinco-aria o una cellula di carburante litio-aria, fornirà un uso migliore per il peso aggiunto rispetto a una cellula di carburante a idrogeno con un serbatoio di stoccaggio in idruro metallico.
Spesso gli idruri reagiscono per combustione, piuttosto violentemente per esposizione all'aria umida, e sono molto tossici a contatto con la pelle o con gli occhi, e quindi sono abbastanza ingombranti da manipolare (si veda borano, idruro di litio e idruro di alluminio). Questa è la ragione (oltre al peso ed al costo) per la quale alcuni combustibili, anche se sono stati proposti dall'industria dei lanci spaziali che ha speso tempo e risorse in queste ricerche, non sono mai stati utilizzati per alcun veicolo in lanci spaziali.
Alcuni idruri forniscono una bassa reattività (e quindi un'elevata sicurezza) ed elevate densità di stoccaggio (al di sopra del 10% in peso). I candidati principali sono il boroidruro di sodio, il tetraidruroalluminato di litio ed il borano di ammonio. Il boroidruro di sodio ed il borano di ammonio possono essere immagazzinati in forma liquida se mescolati con acqua, ma debbono essere stivati in grandi concentrazioni per produrre una densità accettabile di idrogeno e questo richiede un complicato sistema di riciclo dell'acqua nella fuel cell. In forma liquida, il boroidruro di sodio fornisce il vantaggio di poter reagire direttamente nella cella a combustione, permettendo la produzione di meno costose, più efficienti e più potenti fuel cell che non abbisognino di catalizzatori al platino. Riciclare il boroidruro di sodio è molto costoso in termini energetici e sarebbero necessarie appositi impianti di riciclaggio. Sistemi più efficienti di riciclaggio del boroidruro di sodio sono ancora in fase sperimentale. I sistemi di riciclaggio del borano di ammonio sono ancora del tutto da sperimentare.
Idrocarburi sintetici[modifica | modifica wikitesto]
Un'alternativa agli idruri è l'utilizzo dei normali idrocarburi come portatori d'idrogeno. Successivamente un piccolo reformer d'idrogeno estrarrebbe l'idrogeno a seconda del consumo della pila a combustibile. Il problema è che i "reformers" sono lenti nell'estrazione ed alcune perdite di energia, dovute alla bassa efficienza, aggiunti al costo extra della pila a combustione rendono probabilmente più conveniente il bruciare l'idrocarburo in un più economico motore a combustione interna.
La pila a combustibile a metanolo non necessita di un reformer, ma fornisce minore efficienza energetica e densità di potenza rispetto alle celle a combustibile convenzionali, anche se questo potrebbe essere controbilanciato dalla molto maggiore densità energetica dell'etanolo e del metanolo rispetto all'idrogeno. L'alcool come carburante è già oggi, grazie all'agricoltura, una risorsa rinnovabile.
La pila a combustibile ad ossido solido può essere alimentata da idrocarburi a catena corta, come il propano ed il metano, senza la necessità di un reformer, oppure possono funzionare con idrocarburi a catena più lunga (butano, esano e ottano) con un reforming solo parziale, ma le alte temperature ed il lento tempo di avvio di queste celle a combustibile le rendono improponibili per l'uso automobilistico.
Hythane[modifica | modifica wikitesto]
La miscela nota come Hythane o idrometano è stata proposta nel 2007 dall'ASTER, dall'ENEA e dalla Hythane di Littleton (Colorado)[3]. La miscela è costituita da metano e idrogeno gassoso, mantenuti ad alta pressione (300 bar) e a temperatura ambiente, entro un recipiente in acciaio rivestito da plastiche antiurto. Questi recipienti possono contenere dal 5 al 30% di idrogeno, ed il resto della miscela è costituito da CH4. La miscela attualmente non può essere utilizzata in pile a combustibile, ma può essere bruciata con relativa efficienza in motori a combustione interna a bassa compressione, come nei motori statunitensi a benzina (ciclo Otto) oppure nel motore Wankel.[4]
Già la miscela al 7% ha vantaggi ecologici rispetto al metano puro, per il punto di fiamma più basso dell'idrogeno, che porta alla combustione completa del hythane in motori a combustione interna[5].Rispetto alla combustione dell'idrogeno puro, la miscela Hythane riduce di sette volte la produzione degli inquinanti NOx[6].
Altri metodi: nanotubi in carbonio, nanotubi in silicio[modifica | modifica wikitesto]

Attualmente vengono studiati altri metodi più esotici per veicolare l'idrogeno, per esempio basati sulle nanotecnologie, come i vari tipi di micro-sferule di carbonio-60 note come buckyballs ed i nanotubi in carbonio, ma sono ancora in una fase iniziale di ricerca [7].
Nel 2008 è stata annunciata la possibilità di utilizzare nanotubi in silicio per trasportare idrogeno in autoveicoli[8]. Simulazioni fisico/chimiche al computer con il metodo matematico "Grand Canonical Monte Carlo" indicano che i nanotubi di silicio possono assorbire maggiori quantità di idrogeno rispetto ai nanotubi al carbonio[9].
Nel febbraio del 2011, la Cella Energy Ltd., (suddivisione del Rutherford Appleton Laboratory[10]) presenterà alla Fuel Cell and Hydrogen Energy Expo di Washington una tecnologia pratica ed economica per immagazzinare l'idrogeno in micro-fibre intrecciate a formare micro-granuli finissimi (molto più fini della sabbia, tali da assumere una consistenza semi-liquida), che permetterebbe di servire l'idrogeno da distributori analoghi alle attuali pompe di benzina.
Assieme all'Università di Oxford e all'University College di Londra, questi ricercatori hanno prodotto (con tecniche di "elettrospinning" ed "elettrospray") fibre di diametro tra i due e i 50 nanometri che si intrecciano fra loro in modo da creare una sorta di "tessuto" microporoso.[11]
Note[modifica | modifica wikitesto]
- ^ si veda al riguardo la voce "recipiente in pressione"
- ^ DOE Metal hydrides
- ^ TreeHugger: Hydrogen + Methane = Hythane, su treehugger.com. URL consultato il 28 aprile 2009 (archiviato dall'url originale il 31 ottobre 2009).
- ^ L'ENEA propone la miscela idrogeno-metano[collegamento interrotto] (PDF).
- ^ www.hythane.com/system.html, su hythane.com. URL consultato il 28 aprile 2009 (archiviato dall'url originale il 20 novembre 2008).
- ^ Hythane riduce i NOx più di 7 volte rispetto all'utilizzo di H2 puro (PDF), su edenenergy.com.au. URL consultato il 28 aprile 2009 (archiviato dall'url originale il 14 settembre 2009).
- ^ Università di Trois Rivieres (Canada): I nanotubi al carbonio incrementano la quantità di H2 immagazzinata, su nanotechweb.org. URL consultato il 28 aprile 2009 (archiviato dall'url originale l'11 dicembre 2008).
- ^ I nanotubi al silicio per lo stoccaggio di idrogeno nei veicoli a fuel cells - ScienceDaily (24 aprile 2008)
- ^ http://pubs.acs.org/cgi-bin/abstract.cgi/jpccck/2008/112/i14/abs/jp711754h.html I nanotubi al silicio futuri candidati per lo stoccaggio dell'idrogeno: dal primo principio della termodinamica alle simulazioni di Monte Carlo ( Jianhui Lan, Daojian Cheng, Dapeng Cao e Wenchuan Wang )
- ^ Cella Energy Ltd. è una spin-off del Rutherford Appleton Laboratory britannico
- ^ LE SCIENZE: Un nuovo materiale per pompare idrogeno dal solito distributore
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su immagazzinamento dell'idrogeno
Wikimedia Commons contiene immagini o altri file su immagazzinamento dell'idrogeno
Collegamenti esterni[modifica | modifica wikitesto]
- EU Storhy, su storhy.net.
- Nesshy, su nesshy.net. URL consultato l'8 agosto 2008 (archiviato dall'url originale il 20 febbraio 2008).
- Hycones, su hycones.eu. URL consultato l'8 agosto 2008 (archiviato dall'url originale il 7 ottobre 2008).
- United States Department of Energy Planned program activities for 2003-2010 (PDF), su www1.eere.energy.gov.
- Ammonia Borane (NhxBHx) (PDF), su pnl.gov. URL consultato l'8 agosto 2008 (archiviato dall'url originale il 17 settembre 2008).
- Hyweb (1996), su hyweb.de.
- Research into metal-organic framework or Nano Cages [1] Archiviato il 6 luglio 2008 in Internet Archive.[2]
- Hydrogen Storage Technical Data, su public.ca.sandia.gov. URL consultato l'8 agosto 2008 (archiviato dall'url originale il 18 maggio 2008).
| Controllo di autorità | Thesaurus BNCF 34305 |
|---|