Clostridioides difficile
| Clostridioides difficile | |
|---|---|
 | |
| Classificazione scientifica | |
| Dominio | Prokaryota |
| Regno | Bacteria |
| Phylum | Firmicutes |
| Classe | Clostridia |
| Ordine | Clostridiales |
| Famiglia | Clostridiaceae |
| Genere | Clostridioides |
| Specie | C. difficile |
| Nomenclatura binomiale | |
| Clostridioides difficile Lawson & Rainey, 2016 | |
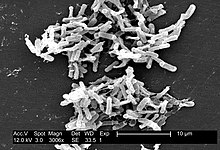
Clostridioides difficile, una volta conosciuto come Clostridium difficile,[1] è un batterio sporigeno appartenente alla famiglia Clostridiaceae. È un bastoncello, Gram +, anaerobio. Come altre specie affini, quando produce specifiche tossine, può essere patogeno per l'uomo.
Ampiamente diffuso nel suolo è presente anche nell’apparato gastrointestinale di vari animali: cani, gatti, cavalli, maiali, roditori. Il C. difficile fa parte della normale flora saprofita dell’intestino umano e colonizza tra il 3% e il 15% degli adulti sani. Può essere isolato nell'80% delle feci dei bambini fino a 1 anno di età, colonizzazione favorita dall’immaturità della flora batterica intestinale.
La specie C. difficile è definita da un grande e diversificato pangenoma con livelli estremi di plasticità evolutiva che è stata modellata per lunghi periodi di tempo dal flusso genico e dalla ricombinazione, spesso tra lignaggi divergenti. Sono stati isolati centinaia di diversi ceppi del C. difficile, non tutti tossigeni. La continua evoluzione del C. difficile in risposta alle attività ambientali e antropiche ha portato alla rapida comparsa e alla diffusione in tutto il mondo di lignaggi clonali virulenti.
L'infezione da Clostridioides difficile è, in alcuni paesi, la causa più comune di infezioni nosocomiali e causerebbe circa 15 000 morti l'anno negli USA e 3 700 nella UE/EEAA.[2][3][4]
Il costo attribuibile per ogni caso di infezione nosocomiale da Clostridioides difficile in Italia è di 14023 euro[5].
Storia[modifica | modifica wikitesto]
Hall e O'Toole, in materiale fecale di neonati, nel 1935 individuarono il batterio: Bacillus difficilis, chiamato così per la difficoltà incontrata nell'isolamento e per l'estrema lentezza di crescita dello stesso sul terreno colturale. Nel 1970 fu rinominato come Clostridium difficile.[6][7][8][9] Mentre il primo caso di colite pseudomembranosa era stato documentato da Finney nel 1893 in un'autopsia di una donna, morta per una diarrea emorragica post-intervento chirurgico, che presentava pseudomembrane simil-difteriche nel colon.[10][11]
Nel 1968 su criceti, normalmente usati per lo studio del C. difficile, trattati con l'antibiotico lincomicina si osservò la comparsa di una grave colite pseudomembranosa sperimentale mortale.[11]
Nel 1970 animali trattati con antibiotici presentavano un'alta quantità nelle feci di tossina patogena prodotta dal C. difficile, individuando con la tossina la causa primaria delle manifestazioni cliniche della patologia della colite pseudomembranosa.[11] Nel 1980 furono individuate due distinte tossine (A e B) prodotte dal C. difficile.[12] Le tossine A e B sono trascritte su un locus di patogenicità che comprende cinque geni: due geni della tossina, tcdA (tossina A) e tcdB (tossina B), e tre geni regolatori, uno dei quali (tcdC) codifica un regolatore negativo della trascrizione della tossina.[13][14]
La prima sequenza genomica completa di un ceppo di C. difficile è stata pubblicata per la prima volta nel 2005 dal Sanger Institute nel Regno Unito. Si trattava del ceppo 630, un ceppo virulento e resistente ai farmaci isolato in Svizzera nel 1982.
La specie è stata trasferita dal genere Clostridium a Clostridioides nel 2016, dandole così il binomio Clostridioides difficile.[15][16][17] Questo nuovo nome riflette le differenze tassonomiche tra questa specie e i membri del genere Clostridium, mantenendo però allo stesso tempo l'abbreviazione C. difficile.[18]
Batteriologia[modifica | modifica wikitesto]

Troviamo spore di Clostridioides difficili nel terreno, negli ospedali e nelle case per anziani. La forma attiva dei batteri si trova solo nel tratto intestinale . Al microscopio, dopo la colorazione di Gram, sono bacilli allungati con un'estremità leggermente gonfia. Il germe stesso è gram-positivo. La sua cultura è ottimale in ambiente basico di agar a 37 °C. Quando le condizioni si fanno difficili, i batteri producono spore resistenti all'essiccazione, a temperature estreme e a molti prodotti chimici e disinfettanti.[19][20].
Le spore sono metabolicamente dormienti e altamente resistenti alle procedure di disinfezione standard, consentendo loro di persistere per lunghi periodi nell'ambiente. Le spore ingerite da ospiti sensibili possono riattivarsi (o germogliare) in risposta a specifici acidi biliari nell'intestino tenue e tornare a uno stile di vita attivo per produrre tossine e causare malattie. Le spore sono altamente trasmissibili e responsabili della contaminazione degli ambienti. Il Clostridioides difficile è un germe della flora digestiva commensale. Rilevato anche nelle feci degli infanti è spesso asintomatico per l'incapacità della tossina, nei ceppi tossigenici, di legarsi ai recettori degli enterociti ancora immaturi. Alcune sue mutazioni emergenti sono multi-resistenti (si sono adattate alla maggior parte degli antibiotici) e in caso di disturbo della flora digestiva provocato dalla somministrazione di antibiotici, possono svilupparsi in modo significativo. La grande variabilità dei diversi ceppi rende difficile la loro caratterizzazione molecolare. Quando nel 2003 l'analisi molecolare ha portato all'identificazione di un ceppo di C. difficile caratterizzato come gruppo BI mediante analisi di endonucleasi di restrizione, NAP1 (nordamericano a campo pulsato) mediante elettroforesi su gel a campo pulsato e ribotipo 027, il "nuovo" ceppo è stato chiamato "C. difficile BI / NAP1 / 027". La diversa terminologia riflette le tecniche predominanti utilizzate per la tipizzazione epidemiologica.[21][22][23]
Del C. difficile esistono sia ceppi tossigenici (cioè produttori di tossine) sia non tossigenici, ma solo le forme tossigeniche sono causa di malattia negli esseri umani.
I batteri producono citotossine polipeptidiche ad alta massa molecolare, A e B. Alcuni ceppi producono solo una delle tossine, altri producono entrambe. La tossina A provoca una reazione infiammatoria che coinvolge l'ipersecrezione di liquido e la necrosi emorragica attraverso l'attivazione del rilascio di citochine da parte dei neutrofili. La citotossina B depolimerizza l'actina, la principale proteina del citoscheletro, e quindi aiuta nella distruzione dei tessuti. L'azione combinata delle tossine provoca necrosi dell'epitelio superficiale ed edema (gonfiore fluidico) nelle zone dell'intestino colpite. La proliferazione del C. difficile è normalmente contrastata dalla normale microflora intestinale, che si ritiene inibisca l'attaccamento del batterio e delle sue tossine alle pareti intestinali. L'alterazione dell'equilibrio microbico intestinale con la terapia antibiotica e la maggiore esposizione al batterio in ambiente ospedaliero consente al C. difficile di colonizzare individui suscettibili. Inoltre, è stato dimostrato che le concentrazioni subinibitorie di antibiotici promuovono una maggiore produzione di tossine da parte di C. difficile.[24][25][26][27][28][29]
Ceppi[modifica | modifica wikitesto]
Il C. difficile è tassonomicamente distinto da molti altri ben noti clostridi, con una struttura di popolazione diversificata che comprende centinaia di ceppi diversi sparsi in almeno 6 cladi filogenetici. Del C. difficile esistono sia ceppi tossigenici (cioè produttori di tossine) sia non tossigenici, ma solo le forme tossigeniche sono causa di malattia negli esseri umani. La patogenicità dipende infatti dalla presenza delle tossine A (TcdA, enterotossina) e B (TcdB, citotossina). Sono stati identificati oltre 400 diversi ceppi tossigenici.[30]
Tutti i ceppi tossigenici esprimono la tossina TcdB, con o senza la tossina TcdA. La tossina B ha infatti attività citotossica più potente della tossina A. Entrambe le tossine sopravvivono nell’ambiente acido dello stomaco e sono in grado di legarsi alla superficie delle cellule epiteliali delle mucose intestinali dove vengono internalizzate e dove catalizzano la glicosilazione di alcune proteine citoplasmatiche, con successiva morte cellulare. Una terza tossina di cui non è chiara la patogenicità, la tossina binaria (CDT), è prodotta da alcuni ceppi di C.difficile. Questa tossina ha dimostrato di incrementare la virulenza di C. difficile attraverso l’adenosina difosfato-ribosilazione di actina, inducendo la formazione di protrusioni di microtubuli nelle cellule facilitando l’adesione del batterio sulla superficie cellulare. La tossina CDT può essere presente anche nei ceppi dove le tossine A e B sono assenti, riscontrati nei pazienti asintomatici.[31]
Esistono ceppi che producono quantità massive di tossine comparsi sin dal 2000. In particolare, C. difficile PCR-ribotipo 027 (BI/NAP1/027) è stato associato a un aumento della gravità dei casi, delle ricorrenze e della mortalità. Il ceppo produce entrambe le tossine in gran quantità a causa di una mutazione (delezione) del gene regolatore tdcC e possiede, analogamente ad altre specie di Clostridi, la tossina binaria CDT. Oltre allo 027, anche altri ribotipi epidemici considerati ipervirulenti sono emersi, alcuni a diffusione internazionale, come lo 078 e lo 018.
Una varietà di approcci di tipizzazione molecolare sono stati sviluppati per studiare il C. difficile e le CDI, tra cui: multilocus sequence typing (MLST), multilocus variable-number tandem-repeat analysis (MLVA), surface layer protein A gene sequence typing, amplificated fragment length polymorphism, elettroforesi su gel a campo pulsato (PFGE), analisi dell'endonucleasi di restrizione (REA), tossinotipizzazione (basata sui dati di sequenza delle tossine A e B) e ribotipizzazione PCR.[32] Quando nel 2005, l'analisi molecolare ha portato all'identificazione di un tipo di ceppo di C. difficile caratterizzato come gruppo BI mediante analisi di endonucleasi di restrizione, NAP1 di tipo a campo pulsato nordamericano mediante elettroforesi su gel a campo pulsato e ribotipo 027 mediante ribotipizzazione PCR multiplex è stato chiamato C. difficile BI/NAP1/027. La diversa terminologia riflette le tecniche predominanti utilizzate per la tipizzazione epidemiologica, anche se la ribotipizzazione PCR è quella più ampiamente accettata in Europa dove l'Anaerobe Reference Laboratory di Cardiff (UK) tiene la collezione dei ceppi e assegna la numerazione dei ribotipi PCR. In Nord America, PFGE è il metodo di digitazione preferito.[33]
Nel Nord America, a partire dal 2016, il ceppo NAP1 è stato sostituito da nuovi ceppi in alcune aree della British Columbia. Questi nuovi ceppi includono NAP2, NAP4, NAP9 e NAP11 e alcuni ceppi che non hanno una designazione NAP. La frequenza di questi nuovi ceppi è aumentata dal 2008 al 2013 in una regione studiata, sostituendo i batteri NAP1 originariamente più comuni e riconoscibili.
In generale, la maggior parte dei metodi di identificazione sono congruenti anche se non si ha una corrispondenza biunivoca tra le diverse tipizzazioni e solo le tecniche MLVA e REA consentono una sufficiente discriminazione tra diversi focolai.[34][35]
I principali database dove sono registrate le caratterizzazioni genetiche dei diversi ceppi di C. difficile sono: Enterobase[36] Public databases for molecular typing and microbial genome diversity (PubMLST).[37]
Alcuni ceppi, ad esempio RT017 RT078 RT027, possono vivere con basse concentrazioni di zucchero trealosio; questi ceppi sono diventati più comuni dopo che il trealosio è stato introdotto come additivo alimentare nei primi anni 2000, aumentando così l'assunzione di cibi addizionati di trealosio.[38][39]
Dal 2005, la morbilità e la mortalità derivanti da C. difficile sono aumentate costantemente in tutto il mondo in funzione dell'insorgenza di ceppi definiti ipervirulenti (in particolare il ribotipo 027). I meccanismi attualmente proposti che distinguono i ceppi ipervirulenti dai ceppi precedenti (meno virulenti) sono oggetto di controversia. Sono stati proposti: l'aumentato tasso di sporulazione, l'aumentata produzione di tossine, la capacità di sopravanzare i ceppi enedemici nell'intestino dell'ospite ma come questo patogeno sia diventato la principale causa di infezioni nosocomiali rimane sconosciuto e la classificazione di "ceppo ipervirulento" resta arbitraria.[40][41] Molti ceppi di C. difficile sono stati rilevati negli animali e in alimenti ricavati da animali facendo emergere anche l'ipotesi che molte trasmissioni del C. difficile nell'uomo siano correlate con l'alimentazione di carne o pesce o interspecie.[42][43][44][45][46][47]
Genoma[modifica | modifica wikitesto]
Il pan-genoma del C. difficile è composto da un genoma centrale (quei geni presenti in tutti gli isolati) e da un genoma accessorio o adattativo (geni assenti da uno o più ceppi o unici per un particolare ceppo).
Una grande percentuale (11%) del genoma è costituita da elementi genetici mobili, principalmente sotto forma di trasposoni coniugativi.
L'analisi ha identificato quattro distinti cluster statisticamente supportati, comprendenti un clade ipervirulento, una tossina A - B +clade e due cladi con isolati umani e animali. Le differenze genetiche tra i cladi hanno rivelato diverse isole genetiche relative alla virulenza e all'adattamento di nicchia, tra cui resistenza agli antibiotici, motilità, adesione e metabolismo enterico. Solo il 19,7% dei geni era condiviso da tutti i ceppi.
Il genoma di C. difficile è ampio e geneticamente diverso, mostrando livelli notevoli di plasticità e livelli bassissimi di conservazione tra i ceppi.
C. difficile possiede un genoma "aperto" con livelli estremi di plasticità, con accesso e scambio frequente con più ambienti ospiti e pool genetici batterici. Di conseguenza, poiché vengono sequenziati più ceppi di C.difficile da linee divergenti e diverse fonti animali e ambientali, questa stima aumenterà probabilmente.
La prima sequenza genomica completa di un ceppo di C. difficile è stata pubblicata per la prima volta nel 2005 dal Sanger Institute nel Regno Unito. Si trattava del ceppo 630, un ceppo virulento e resistente ai farmaci isolato in Svizzera nel 1982. Gli scienziati del Sanger Institute hanno sequenziato genomi di circa 30 isolati di C.difficile utilizzando tecnologie di sequenziamento di nuova generazione da 454 Life Sciences e Illumina.
I ricercatori della McGill University di Montreal hanno sequenziato il genoma del ceppo di C. difficile del Quebec altamente virulento nel 2005 utilizzando una tecnologia di sequenziamento ad altissima velocità. I test hanno comportato l'esecuzione di 400 000 reazioni di sequenziamento parallelo del DNA del genoma del batterio, che era stato frammentato per il sequenziamento. Queste sequenze sono state assemblate computazionalmente per formare una sequenza genomica completa.
Nel 2012, gli scienziati dell'Università di Oxford hanno sequenziato i genomi di C. difficile da 486 casi verificatisi in quattro anni nell'Oxfordshire utilizzando le tecnologie di sequenziamento di nuova generazione.
Nel 2006, Sebaihia e colleghi hanno descritto il primo genoma chiuso completamente sequenziato e annotato di C. difficile (ceppo 630; RT012).[25] Questo ceppo virulento, altamente trasmissibile e multiresistente di C. difficile è stato originariamente isolato nel 1982 da un paziente con PMC a Zurigo, Svizzera. Il sequenziamento e l'annotazione del ceppo 630 hanno rivelato un grande cromosoma circolare di 4 290 252 bp (4,3 Mb), 3 776 sequenze putative di codifica delle proteine (CDS) e un contenuto di GC del 29,06%. È stato anche identificato un plasmide circolare (pCD630) di 7 881 bp contenente 11 CDS.[25] Cinque anni dopo, Monot e colleghi[48] hanno riannotato il genoma del ceppo 630 utilizzando un approccio trascrittomico e proteomico combinato per aggiornare le funzioni putative di > 500 geni precedentemente putativi o sconosciuti. Da allora, molti altri genomi di dimensioni comprese tra 4,1 e 4,3 Mbp sono stati completamente sequenziati e annotati: CD37 (RT009; isolato negli Stati Uniti nel 1980), M68 (RT017; isolato in Irlanda nel 2006), CF5 (RT017; isolato in Belgio nel 1995), M120 (RT078; isolato nel Regno Unito nel 2007), G46 (RT027; isolato nel Regno Unito nel 2006), R20291 (RT027; isolato nel Regno Unito nel 2006), 196 (RT027; isolato in Francia nel 1985), 2007855 (RT027; isolato negli Stati Uniti nel 2007) e BI1 (RT027; isolato negli Stati Uniti nel 1988).[49][50][51] I genomi di riferimento come quelli dei ceppi 630 e M120 svolgono un ruolo importante nella pipeline di analisi dei dati NGS. Comprendono una sequenza inequivocabile e contigua di nucleotidi noti che attraversano l'intero cromosoma e plasmidi (se presenti), fornendo quindi un riferimento di altissima qualità per la mappatura dei genomi in bozza.
In sintesi, gli studi MLST su diverse raccolte di ceppi di C. difficile suggeriscono che ci siano cinque lignaggi o cladi che possono generalmente essere suddivisi per i più importanti ribotipi PCR; 027, 017, 023, 078 e un ampio gruppo comprendente il resto dei ribotipi PCR che rappresenta un lignaggio interessante altamente divergente.
Epigenoma[modifica | modifica wikitesto]
C. difficile ha un epigenoma altamente diversificato, con 17 motivi di metilazione di alta qualità segnalati finora, la maggior parte relativi al tipo 6mA. È stato dimostrato che la metilazione in uno di questi motivi, CAAAA A, altamente conservato, influisce sulla sporulazione, un passaggio chiave nella trasmissione della malattia da C. difficile, nonché sulla lunghezza delle cellule, sulla formazione di biofilm e sulla colonizzazione dell'ospite.[52]
Batteriofagi[modifica | modifica wikitesto]
Un altro componente importante del mobiloma di C. difficile sono i batteriofagi (fagi). I fagi si sono evoluti con il C. difficile per periodi di tempo molto lunghi e l'infezione dei fagi è una parte intrinseca della storia naturale e della biologia del C. difficile. L'acquisizione di fagi e la loro perdita dal genoma di C. difficile sono eventi genetici significativi che hanno avuto un impatto sull'evoluzione dell'ospite.[53]
Almeno otto batteriofagi, principalmente temperati cioè lisogeni, sono stati isolati dal C. difficile, con dimensioni del genoma comprese tra circa 30 e circa 60 kb. Sia i ceppi di C. difficile di origine ambientale sia quelli di origine clinica sono portatori di un insieme diversificato e prevalente di profagi.
Rilevanza clinica[modifica | modifica wikitesto]
Solo i ceppi di Clostridioides difficile che producono tossine sono di rilevanza clinica.
La rapida evoluzione della resistenza agli antibiotici nel C. difficile[54] e i conseguenti effetti sulla prevenzione e il trattamento delle infezioni da C. difficile sono motivo di preoccupazione per la salute pubblica.[55]
I fattori di virulenza del C. difficile sono: enterotossina, spore e ialuronidasi. Questo bacillo si trova normalmente nel microbiota umano per cui, se si utilizzano per lungo tempo antibiotici, questi possono distruggere anche quei batteri che tengono confinato il C. difficile il quale può prendere il sopravvento e provocare crampi addominali e malattie varie (colite pseudomembranosa). Queste malattie hanno un decorso benigno e autolimitanti tranne nel caso in cui ci sono complicanze che possono compromettere la parete intestinale con un possibile passaggio in circolo del bacillo, con conseguente sepsi e quindi morte dell'individuo.
L'isolamento può avvenire tramite la coprocoltura in terreni selettivi per C. difficile. L'enterotossina può essere saggiata con il metodo ELISA, mentre la citotossina con rivelazione di tossicità in colture cellulari.
Note[modifica | modifica wikitesto]
- ^ Paul A. Lawson, Diane M. Citron e Kerin L. Tyrrell, Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O'Toole 1935) Prévot 1938, in Anaerobe, vol. 40, 2016-08, pp. 95–99, DOI:10.1016/j.anaerobe.2016.06.008. URL consultato il 22 gennaio 2021.
- ^ Evelyn Balsells, Ting Shi e Callum Leese, Global burden of Clostridium difficile infections: a systematic review and meta-analysis, in Journal of Global Health, vol. 9, n. 1, DOI:10.7189/jogh.09.010407. URL consultato il 23 gennaio 2021.
- ^ (EN) CDC, Nearly half a million Americans suffer from C. difficile infections in, su Centers for Disease Control and Prevention, 31 dicembre 2018. URL consultato il 23 gennaio 2021.
- ^ (EN) Clostridium difficile infections - Facts and surveillance, su European Centre for Disease Prevention and Control. URL consultato il 23 gennaio 2021.
- ^ (EN) Angel Asensio, Stefano Di Bella e Andrea Lo Vecchio, The impact of Clostridium difficile infection on resource use and costs in hospitals in Spain and Italy: a matched cohort study, in International Journal of Infectious Diseases, vol. 36, 2015-07, pp. 31–38, DOI:10.1016/j.ijid.2015.05.013. URL consultato il 14 novembre 2023.
- ^ Hall, Ivan C. e O'Toole. Elizabeth, Intestinal flora in newborn infants with a description of a new pathogenic anaerobe, Bacillus difficilis, in American Journal of Diseases of Children, vol. 49, n. 2, 1935, pp. 390–402.
- ^ X. Chen, K. Katchar; JD. Goldsmith; N. Nanthakumar; A. Cheknis; DN. Gerding; CP. Kelly, A mouse model of Clostridium difficile-associated disease., in Gastroenterology, vol. 135, n. 6, dicembre 2008, pp. 1984-92, DOI:10.1053/j.gastro.2008.09.002, PMID 18848941.
- ^ CP. Kelly, JT. LaMont, Clostridium difficile--more difficult than ever., in N Engl J Med, vol. 359, n. 18, ottobre 2008, pp. 1932-40, DOI:10.1056/NEJMra0707500, PMID 18971494.
- ^ MY. Hu, K. Katchar; L. Kyne; S. Maroo; S. Tummala; V. Dreisbach; H. Xu; DA. Leffler; CP. Kelly, Prospective derivation and validation of a clinical prediction rule for recurrent Clostridium difficile infection., in Gastroenterology, vol. 136, n. 4, aprile 2009, pp. 1206-14, DOI:10.1053/j.gastro.2008.12.038, PMID 19162027.
- ^ JT. Lamont, Theodore E. Woodward Award. How bacterial enterotoxins work: insights from in vivo studies., in Trans Am Clin Climatol Assoc, vol. 113, 2002, pp. 167-80; discussion 180-1, PMID 12053708.
- ^ a b c Stephen H. Gillespie e Peter M. Hawkey, Principles and Practice of Clinical Bacteriology, John Wiley and Sons, 1º luglio 2006, pp. 557–, ISBN 978-0-470-03532-0.
- ^ I. Brook, Isolation of toxin producing Clostridium difficile from two children with oxacillin- and dicloxacillin-associated diarrhea., in Pediatrics, vol. 65, n. 6, giugno 1980, pp. 1154-6, PMID 7375240.
- ^ T. Chopra, GJ. Alangaden; P. Chandrasekar, Clostridium difficile infection in cancer patients and hematopoietic stem cell transplant recipients., in Expert Rev Anti Infect Ther, vol. 8, n. 10, ottobre 2010, pp. 1113-9, DOI:10.1586/eri.10.95, PMID 20954878.
- ^ Patrizia Spigaglia e Paola Mastrantonio, Molecular Analysis of the Pathogenicity Locus and Polymorphism in the Putative Negative Regulator of Toxin Production (TcdC) among Clostridium difficile Clinical Isolates, in Journal of Clinical Microbiology, vol. 40, n. 9, 2002-9, pp. 3470–3475, DOI:10.1128/JCM.40.9.3470-3475.2002. URL consultato il 22 gennaio 2021.
- ^ Aharon Oren e George M. Garrity, List of new names and new combinations previously effectively, but not validly, published, in International Journal of Systematic and Evolutionary Microbiology, vol. 67, n. 9, 2017, pp. 3140–3143, DOI:10.1099/ijsem.0.002278, PMC 5817221, PMID 28891789.
- ^ Paul A. Lawson, Diane M. Citron, Kerin L. Tyrrell e Sydney M. Finegold, Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O'Toole 1935) Prévot 1938, in Anaerobe, vol. 40, agosto 2016, pp. 95–99, DOI:10.1016/j.anaerobe.2016.06.008, ISSN 1095-8274, PMID 27370902.
- ^ (EN) Duolong Zhu, Joseph A. Sorg e Xingmin Sun, Clostridioides difficile Biology: Sporulation, Germination, and Corresponding Therapies for C. difficile Infection, in Frontiers in Cellular and Infection Microbiology, vol. 8, 2018, pp. 29, DOI:10.3389/fcimb.2018.00029, ISSN 2235-2988, PMC 5809512, PMID 29473021.
- ^ Paul A. Lawson, Diane M. Citron, Kerin L. Tyrrell e Sydney M. Finegold, Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O'Toole 1935) Prévot 1938, in Anaerobe, vol. 40, agosto 2016, pp. 95–99, DOI:10.1016/j.anaerobe.2016.06.008, ISSN 1075-9964, PMID 27370902.
- ^ Dale N. Gerding, Carlene A. Muto e Robert C. Owens, Measures to control and prevent Clostridium difficile infection, in Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America, 46 Suppl 1, 15 gennaio 2008, pp. S43–49, DOI:10.1086/521861. URL consultato il 22 gennaio 2021.
- ^ William A. Rutala, Maria F. Gergen e David J. Weber, Efficacy of different cleaning and disinfection methods against Clostridium difficile spores: importance of physical removal versus sporicidal inactivation, in Infection Control and Hospital Epidemiology, vol. 33, n. 12, 2012-12, pp. 1255–1258, DOI:10.1086/668434. URL consultato il 22 gennaio 2021.
- ^ Spigaglia, P., Barbanti, F., Mastrantonio, P., European Study Group on Clostridium difficile (ESGCD), Ackermann, G., Balmelli, C., … & Drudy, D. (2011). Multidrug resistance in European Clostridium difficile clinical isolates. Journal of Antimicrobial Chemotherapy, 66(10), 2227-2234.
- ^ Kuijper, E. J., van den Berg, R. J., Debast, S., Visser, C. E., Veenendaal, D., Troelstra, A., … & Notermans, D. W. (2006). Clostridium difficile ribotype 027, toxinotype III, the Netherlands. Emerging infectious diseases, 12(5), 827.
- ^ John G. Bartlett, Narrative Review: The New Epidemic of Clostridium difficile–Associated Enteric Disease, in Annals of Internal Medicine, vol. 145, n. 10, 21 novembre 2006, pp. 758–764, DOI:10.7326/0003-4819-145-10-200611210-00008. URL consultato il 21 gennaio 2021.
- ^ Daniel R. Knight, Briony Elliott e Barbara J. Chang, Diversity and Evolution in the Genome of Clostridium difficile, in Clinical Microbiology Reviews, vol. 28, n. 3, 2015-7, pp. 721–741, DOI:10.1128/CMR.00127-14. URL consultato il 21 gennaio 2021.
- ^ a b c Mohammed Sebaihia, Brendan W. Wren e Peter Mullany, The multidrug-resistant human pathogen Clostridium difficile has a highly mobile, mosaic genome, in Nature Genetics, vol. 38, n. 7, 2006-07, pp. 779–786, DOI:10.1038/ng1830. URL consultato il 21 gennaio 2021.
- ^ Donald C. Vinh, Strains and toxins of Clostridium, in CMAJ : Canadian Medical Association Journal, vol. 172, n. 3, 1º febbraio 2005, pp. 312–313, DOI:10.1503/cmaj.1041642. URL consultato il 21 gennaio 2021.
- ^ L. Clifford McDonald, George E. Killgore e Angela Thompson, An Epidemic, Toxin Gene–Variant Strain of Clostridium difficile, in New England Journal of Medicine, vol. 353, n. 23, 8 dicembre 2005, pp. 2433–2441, DOI:10.1056/NEJMoa051590. URL consultato il 21 gennaio 2021.
- ^ (EN) Rawish Fatima e Muhammad Aziz, The Hypervirulent Strain of Clostridium Difficile: NAP1/B1/027 - A Brief Overview, in Cureus, vol. 11, n. 1, 29 gennaio 2019, DOI:10.7759/cureus.3977. URL consultato il 21 gennaio 2021.
- ^ Gayatri Vedantam, Andrew Clark e Michele Chu, Clostridium difficile infection, in Gut Microbes, vol. 3, n. 2, 1º marzo 2012, pp. 121–134, DOI:10.4161/gmic.19399. URL consultato il 21 gennaio 2021.
- ^ (EN) Kate E. Dingle, David Griffiths e Xavier Didelot, Clinical Clostridium difficile: Clonality and Pathogenicity Locus Diversity, in PLOS ONE, vol. 6, n. 5, 19-mag-2011, pp. e19993, DOI:10.1371/journal.pone.0019993. URL consultato il 23 gennaio 2021.
- ^ (EN) C. Eckert, A. Emirian e A. Le Monnier, Prevalence and pathogenicity of binary toxin–positive Clostridium difficile strains that do not produce toxins A and B, in New Microbes and New Infections, vol. 3, 2015-01, pp. 12–17, DOI:10.1016/j.nmni.2014.10.003. URL consultato il 23 gennaio 2021.
- ^ European Centre for Disease Prevention and Control., Laboratory procedures for diagnosis and typing of human Clostridium difficile infection., Publications Office, 2018, DOI:10.2900/04291. URL consultato il 23 gennaio 2021.
- ^ The Continually Evolving Clostridium difficile Species, su Medscape. URL consultato il 23 gennaio 2021.
- ^ George Killgore, Angela Thompson e Stuart Johnson, Comparison of seven techniques for typing international epidemic strains of Clostridium difficile: restriction endonuclease analysis, pulsed-field gel electrophoresis, PCR-ribotyping, multilocus sequence typing, multilocus variable-number tandem-repeat analysis, amplified fragment length polymorphism, and surface layer protein A gene sequence typing, in Journal of Clinical Microbiology, vol. 46, n. 2, 2008-02, pp. 431–437, DOI:10.1128/JCM.01484-07. URL consultato il 24 gennaio 2021.
- ^ Fred C. Tenover, Thomas Åkerlund e Dale N. Gerding, Comparison of Strain Typing Results for Clostridium difficile Isolates from North America▿, in Journal of Clinical Microbiology, vol. 49, n. 5, 2011-5, pp. 1831–1837, DOI:10.1128/JCM.02446-10. URL consultato il 24 gennaio 2021.
- ^ EnteroBase, su enterobase.warwick.ac.uk. URL consultato il 24 gennaio 2021.
- ^ (EN) Clostridioides difficile, su PubMLST. URL consultato il 24 gennaio 2021.
- ^ J. Collins, C. Robinson e H. Danhof, Dietary trehalose enhances virulence of epidemic Clostridium difficile, in Nature, vol. 553, n. 7688, 18 gennaio 2018, pp. 291–294, DOI:10.1038/nature25178. URL consultato il 24 gennaio 2021.
- ^ (EN) David W. Eyre, Xavier Didelot e Anthony M. Buckley, Clostridium difficile trehalose metabolism variants are common and not associated with adverse patient outcomes when variably present in the same lineage, in EBioMedicine, vol. 43, 1º maggio 2019, pp. 347–355, DOI:10.1016/j.ebiom.2019.04.038. URL consultato il 24 gennaio 2021.
- ^ (EN) Michelle Merrigan, Anilrudh Venugopal e Michael Mallozzi, Human Hypervirulent Clostridium difficile Strains Exhibit Increased Sporulation as Well as Robust Toxin Production, in Journal of Bacteriology, vol. 192, n. 19, 1º ottobre 2010, pp. 4904–4911, DOI:10.1128/JB.00445-10. URL consultato il 24 gennaio 2021.
- ^ Laith Yakob, Thomas V. Riley e David L. Paterson, Mechanisms of hypervirulent Clostridium difficile ribotype 027 displacement of endemic strains: an epidemiological model, in Scientific Reports, vol. 5, 28 luglio 2015, DOI:10.1038/srep12666. URL consultato il 24 gennaio 2021.
- ^ (EN) Alexander Rodriguez-Palacios, Kevin Q Mo e Bhavan U. Shah, Global and Historical Distribution of Clostridioides difficile in the Human Diet (1981-2019): Systematic Review and Meta-Analysis of 21886 Samples Reveal Sources of Heterogeneity, High-Risk Foods, and Unexpected Higher Prevalence Towards the Tropic, Infectious Diseases (except HIV/AIDS), 22 novembre 2019, DOI:10.1101/19012450. URL consultato il 24 gennaio 2021.
- ^ Dallas G. Hoover e Alexander Rodriguez-Palacios, Transmission of Clostridium difficile in foods, in Infectious Disease Clinics of North America, vol. 27, n. 3, 2013-09, pp. 675–685, DOI:10.1016/j.idc.2013.05.004. URL consultato il 23 gennaio 2021.
- ^ (EN) K. Keel, J. S. Brazier e K. W. Post, Prevalence of PCR Ribotypes among Clostridium difficile Isolates from Pigs, Calves, and Other Species, in Journal of Clinical Microbiology, vol. 45, n. 6, 1º giugno 2007, pp. 1963–1964, DOI:10.1128/JCM.00224-07. URL consultato il 24 gennaio 2021.
- ^ Alexander W. W. Brown e Robert B. Wilson, Clostridium difficile colitis and zoonotic origins-a narrative review, in Gastroenterology Report, vol. 6, n. 3, 2018-08, pp. 157–166, DOI:10.1093/gastro/goy016. URL consultato il 23 gennaio 2021.
- ^ Alan M. Mc Govern, Niki F. Foster e Lynette A. Pereira, Human Clostridium difficile infection caused by a livestock-associated PCR ribotype 237 strain in Western Australia, in JMM case reports, vol. 3, n. 4, 2016-08, pp. e005062, DOI:10.1099/jmmcr.0.005062. URL consultato il 23 gennaio 2021.
- ^ (EN) Luis G Arroyo, Stephen A Kruth e Barbara M Willey, PCR ribotyping of Clostridium difficile isolates originating from human and animal sources, in Journal of Medical Microbiology, vol. 54, n. 2, 1º febbraio 2005, DOI:10.1099/jmm.0.45805-0#tab2. URL consultato il 23 gennaio 2021.
- ^ Marc Monot, Caroline Boursaux-Eude e Marie Thibonnier, Reannotation of the genome sequence of Clostridium difficile strain 630, in Journal of Medical Microbiology, vol. 60, Pt 8, 2011-08, pp. 1193–1199, DOI:10.1099/jmm.0.030452-0. URL consultato il 24 gennaio 2021.
- ^ Tom Gaulton, Raju Misra e Graham Rose, Complete Genome Sequence of the Hypervirulent Bacterium Clostridium difficile Strain G46, Ribotype 027, in Genome Announcements, vol. 3, n. 2, 26 marzo 2015, DOI:10.1128/genomeA.00073-15. URL consultato il 24 gennaio 2021.
- ^ Michael S. M. Brouwer, Elaine Allan e Peter Mullany, Draft genome sequence of the nontoxigenic Clostridium difficile strain CD37, in Journal of Bacteriology, vol. 194, n. 8, 2012-04, pp. 2125–2126, DOI:10.1128/JB.00122-12. URL consultato il 24 gennaio 2021.
- ^ Miao He, Mohammed Sebaihia e Trevor D. Lawley, Evolutionary dynamics of Clostridium difficile over short and long time scales, in Proceedings of the National Academy of Sciences of the United States of America, vol. 107, n. 16, 20 aprile 2010, pp. 7527–7532, DOI:10.1073/pnas.0914322107. URL consultato il 24 gennaio 2021.
- ^ Pedro H. Oliveira, John W. Ribis e Elizabeth M. Garrett, Epigenomic characterization of Clostridioides difficile finds a conserved DNA methyltransferase that mediates sporulation and pathogenesis, in Nature microbiology, vol. 5, n. 1, 2020-1, pp. 166–180, DOI:10.1038/s41564-019-0613-4. URL consultato il 22 gennaio 2021.
- ^ Katherine R. Hargreaves e Martha R. J. Clokie, Clostridium difficile phages: still difficult?, in Frontiers in Microbiology, vol. 5, 28 aprile 2014, DOI:10.3389/fmicb.2014.00184. URL consultato il 22 gennaio 2021.
- ^ Saeed S. Banawas, Clostridium difficile Infections: A Global Overview of Drug Sensitivity and Resistance Mechanisms, in BioMed Research International, vol. 2018, 21 febbraio 2018, DOI:10.1155/2018/8414257. URL consultato il 24 gennaio 2021.
- ^ Patrizia Spigaglia, Paola Mastrantonio e Fabrizio Barbanti, Antibiotic Resistances of Clostridium difficile, in Advances in Experimental Medicine and Biology, vol. 1050, 2018, pp. 137–159, DOI:10.1007/978-3-319-72799-8_9. URL consultato il 24 gennaio 2021.
Bibliografia[modifica | modifica wikitesto]
- Giampiero Carosi, Carosi - Pauluzzi e Sergio Pauluzzi, Malattie infettive, PICCIN, 2007, pp. 233–, ISBN 978-88-299-1844-7.
- (EN) Tracy Dale Wilkins, Clostridium difficile, Springer, 2000, ISBN 978-3-540-67291-3.
- (EN) Patrice Boquet e Emmanuel Lemichez, Bacterial virulence factors and Rho GTPases, Springer, 2005, pp. 117–, ISBN 978-3-540-23865-2.
- (EN) Ferruccio Mandler, Catalogo ragionato dei presidi diagnostici per la microbiologia clinica, PICCIN, 1999, pp. 62–, ISBN 978-88-299-1442-5.
- (EN) Stephen H. Gillespie e Peter M. Hawkey, Principles and Practice of Clinical Bacteriology, John Wiley and Sons, 1º luglio 2006, pp. 557–, ISBN 978-0-470-03532-0.
- (EN) James G. Fox, The Mouse in Biomedical Research: Diseases, Academic Press, 2007, pp. 357–, ISBN 978-0-12-369456-0.
- (EN) ICDDR, B, Diarrhoeal Diseases Research, ICDDR, B, settembre 1992, pp. 156–.
- (EN) Allison Tannis, Probiotic Rescue: How You Can Use Probiotics to Fight Cholesterol, Cancer Superbugs, Digestive Complaints and More, John Wiley and Sons, 3 aprile 2008, pp. 182–, ISBN 978-0-470-15475-5.
Riviste[modifica | modifica wikitesto]
- CH. Choi, SA. Jung; BI. Lee; KM. Lee; JS. Kim; DS. Han, [Diagnostic guideline of ulcerative colitis]., in Korean J Gastroenterol, vol. 53, n. 3, marzo 2009, pp. 145-60, PMID 19835217.
- E. van Nood, P. Speelman; EJ. Kuijper; JJ. Keller, Struggling with recurrent Clostridium difficile infections: is donor faeces the solution?, in Euro Surveill, vol. 14, n. 34, 2009, PMID 19712646.
- E. Palencia-Herrejón, B. Sánchez; I. Escobar; ML. Gómez-Lus, [Proton pump inhibitors and infection risk]., in Rev Esp Quimioter, vol. 24, n. 1, marzo 2011, pp. 4-12, PMID 21412664.
- AC. de Oliveira, QS. Damasceno, [Surfaces of the hospital environment as possible deposits of resistant bacteria: a review]., in Rev Esc Enferm USP, vol. 44, n. 4, dicembre 2010, pp. 1118-23, PMID 21337799.
- J. Freeman, MP. Bauer; SD. Baines; J. Corver; WN. Fawley; B. Goorhuis; EJ. Kuijper; MH. Wilcox, The changing epidemiology of Clostridium difficile infections., in Clin Microbiol Rev, vol. 23, n. 3, luglio 2010, pp. 529-49, DOI:10.1128/CMR.00082-09, PMID 20610822.
- D. Shah, MD. Dang; R. Hasbun; HL. Koo; ZD. Jiang; HL. DuPont; KW. Garey, Clostridium difficile infection: update on emerging antibiotic treatment options and antibiotic resistance., in Expert Rev Anti Infect Ther, vol. 8, n. 5, maggio 2010, pp. 555-64, DOI:10.1586/eri.10.28, PMID 20455684.
- C. Vaishnavi, Clinical spectrum pathogenesis of Clostridium difficile associated diseases., in Indian J Med Res, vol. 131, aprile 2010, pp. 487-99, PMID 20424299.
- H. Taslim, Clostridium difficile infection in the elderly., in Acta Med Indones, vol. 41, n. 3, luglio 2009, pp. 148-51, PMID 19752488.
- M. Bixquert Jiménez, Treatment of irritable bowel syndrome with probiotics. An etiopathogenic approach at last?, in Rev Esp Enferm Dig, vol. 101, n. 8, agosto 2009, pp. 553-64, PMID 19785495.
- C. Eckert, F. Barbut, [Clostridium-difficile-associated infections]., in Med Sci (Paris), vol. 26, n. 2, febbraio 2010, pp. 153-8, DOI:10.1051/medsci/2010262153, PMID 20188046.
Veterinaria[modifica | modifica wikitesto]
- Wilfried R. Kraft e Ulrich M. Dürr, Trattato di medicina e chirurgia del gatto, Elsevier srl, 2001, pp. 199–, ISBN 978-88-214-2525-7.
- (EN) Norman Edward Robinson e Kim A. Sprayberry, Current therapy in equine medicine, Elsevier Health Sciences, 2009, pp. 158–, ISBN 978-1-4160-5475-7.
Voci correlate[modifica | modifica wikitesto]
- Infezione da Clostridioides difficile
- Terreno selettivo per Clostridioides difficile
- Infezioni correlate all'assistenza
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Clostridioides difficile
Wikimedia Commons contiene immagini o altri file su Clostridioides difficile Wikispecies contiene informazioni su Clostridioides difficile
Wikispecies contiene informazioni su Clostridioides difficile
