Ossido di ittrio bario e rame
| Ossido di ittrio bario e rame | |
|---|---|
 | |
| Nome IUPAC | |
| cuprato di ittrio bario | |
| Nomi alternativi | |
| YBCO, Y123 (obsoleto) | |
| Caratteristiche generali | |
| Formula bruta o molecolare | YBa2Cu3O7 |
| Peso formula (u) | 666,19 |
| Aspetto | solido nero |
| Numero CAS | |
| Numero EINECS | 619-720-7 |
| PubChem | 21871996 |
| SMILES | [Ba+2].[Ba+2].[Cu+2].[Cu+2].[O-2].[O-2].[O-2].[O-2].[O-2].[O-2].[O-2].[Y+3].[Y+3] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 6,4 |
| Solubilità in acqua | insolubile |
| Temperatura di fusione | >1000 °C |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| Frasi H | 302 - 315 - 319 - 335 |
| Consigli P | 261 - 264 - 270 - 271 - 280 - 301+312 - 302+352 - 304+340 - 305+351+338 - 312 - 321 - 330 - 332+313 - 337+313 |
L'ossido di ittrio bario e rame o cuprato di ittrio e bario è il composto chimico di formula YBa2Cu3O7. È un sale cristallino. Il nome è comunemente abbreviato negli Stati Uniti d'America come YBCO (iniziali degli elementi costituenti) o anche Y123 (per la stechiometria dei metalli ittrio bario e rame contenuti). In condizioni normali è un solido nero insolubile in acqua. Questo materiale è famoso per essere stato il primo a mostrare proprietà di superconduttore ad una temperatura superiore a quella di ebollizione dell'azoto liquido.
Fa parte del gruppo più generale degli ossidi di rame bario e terre rare (ReBCO) in cui, al posto dell'ittrio, sono presenti altre terre rare.
Storia[modifica | modifica wikitesto]
Dalla scoperta della superconduttività da parte di Kamerlingh Onnes del 1911, per settantacinque anni furono noti solo superconduttori a temperatura molto bassa, raggiungibile soltanto attraverso l'impiego di elio liquido. Tra questi, i superconduttori più importanti sono quelli basati sul niobio: il rappresentante di questa classe è il Nb3Ge, seguito dal niobio-titanio.
Intorno al 1986, presso il centro di ricerca IBM a Zurigo, i ricercatori Bednorz e Müller studiavano nuovi tipi di semiconduttori. In quell'anno scoprirono un particolare cuprato semiconduttore che diventava un superconduttore a una temperatura molto più alta dei superconduttori che finora erano noti. In particolare, il loro cuprato aveva una struttura cristallina del tipo perovskiti, ma rispetto a questa era carente di ossigeno. L'anno successivo i due ricercatori ricevettero il Premio Nobel per la fisica, grazie a questa scoperta.
Nel 1987, Maw-Kuen Wu, della University of Alabama a Huntsville, e Paul Chu, della University of Houston, scoprirono che un particolare cuprato, misto di bario e ittrio, (con sigla YBCO) aveva una temperatura critica pari a circa -180 °C: di nuovo, la temperatura richiesta per attivare la superconduzione era molto più alta del solito. I primi campioni di questo cuprato avevano formula bruta: Y1.2Ba0.8CuO4.
Il cuprato misto di ittrio e bario è stato il primo materiale scoperto a cui basta un raffreddamento con azoto liquido per attivare la superconduzione.
I precedenti materiali, infatti, richiedevano un raffreddamento basato sull'elio liquido, molto più difficile da realizzare e mantenere.
Sintesi e proprietà[modifica | modifica wikitesto]
Il cuprato misto di ittrio e bario relativamente puro fu preparato per la prima volta riscaldando una particolare miscela di carbonati metallici, a temperature circa comprese tra 870 e 1100 °C:[1][2]
Le sintesi successive usarono i corrispondenti ossidi o nitrati.[1] Un articolo molto interessante sia dal punto di vista storico, che per lo studio della sintesi del cuprato misto di ittrio e bario, fu pubblicato pochi mesi dopo, nel luglio 1987. L'articolo, di Paul Grant, che lavorava presso il centro di ricerca IBM della Almaden Valley (vicino a San Jose, California), fu pubblicato sul New Scientist.[3] Questo articolo conteneva una ricetta per creare questo composto nel riquadro "Shake and bake", e i reagenti nel riquadro "Where to find": si riferisce alla Gran Bretagna.
La proprietà di superconduttore per cuprati della forma YBa2Cu3O7−x è molto sensibile alla quantità di ossigeno contenuto (indicato con x). Il contenuto in ossigeno deve essere inferiore a x ≤ 0,65. Quando x ~ 0.07, il materiale superconduce alla temperatura più alta (-180 °C). Anche il campo magnetico producibile in questo modo diventa massimo. Il campo magnetico in direzione parallela ai piani cuprati (di ossido di rame: CuO2[4]) è maggiore rispetto a quello in direzione normale ai piani.
Oltre ad essere molto sensibili alla quantità di ossigeno contenuto, le proprietà di questi cuprati dipendono molto dal metodo di sintesi. Il metodo standard è una sinterizzazione. Per ottenere un materiale cristallino con adeguate proprietà, i bordi dei grani devono essere allineati tra loro. Questo è possibile solo con un attento controllo delle velocità di ricottura e di tempra del materiale.
Sono stati sviluppati anche metodi alternativi, per esempio basati sulla deposizione chimica da vapore[1][2] e sol-gel[5]
L'acido trifluoroacetico è un agente fluorante, in grado di impedire la formazione di carbonato di bario, indesiderato. Usando la più normale deposizione chimica da soluzione, si sono preparati film sottili di alta qualità.[6]
Struttura[modifica | modifica wikitesto]

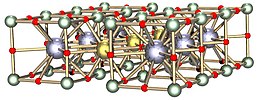
L'ossido di ittrio bario e rame cristallizza in una struttura simile alla perovskite, ma carente di ossigeno. La struttura a perovskite avrebbe infatti formula: YBa2Cu3O9.
La struttura, come per tutti i cuprati, è stratificata. Si distinguono due tipi di coordinazione per gli atomi di rame, a seconda della coordinazione da parte dell'ossigeno.
La prima coordinazione del rame è a piramide quadrata; l'atomo non è collocato esattamente alla base della piramide. Ciò provoca la formazione di piani cuprati leggermente corrugati (in figura, indicati come "copper planes").[1]
La seconda coordinazione, di tipo planare quadrata, provoca la formazione di nastri, disposti perpendicolarmente ai piani precedenti (in figura, indicati come "copper ribbons").
Gli atomi di ittrio si trovano tra i piani (di rame) e gli atomi di bario si trovano tra i nastri e i piani.
Applicazioni[modifica | modifica wikitesto]

I cuprati sono molto studiati ma solo recentemente si è riusciti a ottenere applicazioni commerciali.[8][9] I problemi maggiori riguardano la difficoltà di sintetizzare il materiale con una precisione che permetta il passaggio di correnti di interesse pratico.[2]
Infatti, come per tutti i superconduttori, le prestazioni in termini di corrente trasportabile, dipendono fortemente, oltre che dalla temperatura, dal campo magnetico a cui sono sottoposti, come mostrato nella figura a sinistra.
Nel 2021, SuperOx, un'azienda russa e giapponese, ha sviluppato un nuovo processo di produzione di fili YBCO per reattori a fusione. Questo nuovo filo ha dimostrato di condurre tra i 700 e i 2000 Ampere per millimetro quadrato. L'azienda è riuscita a produrre 300 km di filo in 9 mesi, tra il 2019 e il 2021, migliorando drasticamente la capacità produttiva. L'azienda ha utilizzato un processo di deposizione al plasma-laser, su un substrato elettrolucidato, per produrre un nastro di 12 mm di larghezza e poi tagliarlo in un nastro di 3 mm.[10]
Sicurezza[modifica | modifica wikitesto]
Il cuprato di bario e ittrio è un composto stabile.
Risulta nocivo per inalazione ed ingestione, ed è irritante per la pelle e le mucose. Non ci sono dati sufficienti per stabilire eventuali proprietà cancerogene.[11]
Note[modifica | modifica wikitesto]
- ^ a b c d (EN) Greenwood, N.N. e Earnshaw, A., Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
- ^ a b c (EN) Housecroft, C.E. e Sharpe, A.G., Inorganic chemistry, 3ª ed., Harlow, Pearson, 2007, ISBN 978-01-31-75553-6.
- ^ (EN) Paul Grant, Do-it-yourself superconductors, in New Scientist, 30 luglio 1987.
- ^ (EN) T.Sekitani, N. Miura, S. Ikeda, Y.H. Matsuda e Y. Shiohara, Upper critical field for optimally-doped YBa2Cu3O7−δ, in Physica B: Condensed Matter, vol. 346-347, 30 aprile 2004, pp. 319-324, DOI:10.1016/j.physb.2004.01.098. URL consultato il 20 marzo 2022.
- ^ (EN) Y.-K. Sun e I.-H. Oh, Preparation of ultrafine YBa2Cu3O7−x Superconductor Powders by the Poly(vinyl alcohol)-Assisted Sol−Gel Method, in Ind. Eng. Chem. Res., vol. 35, n. 11, 7 novembre 1996, pp. 4296–4300, DOI:10.1021/ie950527y. URL consultato il 20 marzo 2022.
- ^ (EN) O. Castaño, A. Cavallaro, A. Palau, J.C. González, M. Rossell, T. Puig, F. Sandiumenge, N. Mestres, S. Piñol e A. Pomar, High quality ittrium cuprate thin films, in Superconductor Science and Technology, vol. 16, n. 1, 25 novembre 2002, pp. 45-53, DOI:10.1088/0953-2048/16/1/309. URL consultato il 20 marzo 2022.
- ^ Anjela Koblischka-Veneva, Michael R. Koblischka, Kévin Berger, Quentin Nouailhetas, Bruno Douine, Miryala Muralidhar e Masato Murakami, Comparison of Temperature and Field Dependencies of the Critical Current Densities of Bulk YBCO, MgB₂, and Iron-Based Superconductors, in IEEE Transactions on Applied Superconductivity, vol. 29, n. 5, 2019-08, pp. 1–5, DOI:10.1109/TASC.2019.2900932, ISSN 1558-2515.
- ^ Fusione a confinamento magnetico, l’energia che imita le stelle, su Agi. URL consultato il 9 settembre 2021.
- ^ (EN) To 20 Tesla and beyond: the high-temperature superconductors, su CERN. URL consultato il 4 novembre 2021.
- ^ (EN) A. Molodyk, S. Samoilenkov e A. Markelov, Development and large volume production of extremely high current density YBa2Cu3O7 superconducting wires for fusion, in Scientific Reports, vol. 11, n. 1, 22 gennaio 2021, pp. 2084, DOI:10.1038/s41598-021-81559-z. URL consultato il 12 aprile 2024.
- ^ Alfa Aesar, Scheda dei dati di sicurezza di YBCO (PDF), su alfa.com:. URL consultato l'11 maggio 2011.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Ossido di ittrio bario e rame
Wikimedia Commons contiene immagini o altri file su Ossido di ittrio bario e rame
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) yttrium barium copper oxide, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
