Acido retinoico
| Acido retinoico | |
|---|---|
 | |
 | |
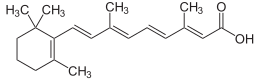
| Nome IUPAC | |
| acido 3,7-dimetil-9-(2,6,6-trimetilcicloesen-1-il)nona-2E,4E,6E,8E-tetraenoico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C20H28O2 |
| Massa molecolare (u) | 300,43512 |
| Numero CAS | |
| PubChem | 444795 |
| SMILES | CC1=C(C(CCC1)(C)C)C=CC(=CC=CC(=CC(=O)O)C)C |
| Indicazioni di sicurezza | |
L'acido retinoico è un metabolita che interviene nelle funzioni della vitamina A (retinolo) necessarie per la crescita e lo sviluppo.
Esso è fondamentale nei vertebrati durante la prima fase dello sviluppo dell'embrione, poiché permette di individuare la posizione dell'asse dell'embrione anteriore/posteriore fungendo da molecola di segnalazione intercellulare che guida lo sviluppo nella parte posteriore dell'embrione.[1]
Il ruolo chiave che riveste l'acido retinoico nello sviluppo dell'embrione interviene anche nell'elevata teratogenesi di farmaci a base di retinolo, come l'Isotretinoina usata per il trattamento di determinati tipi di neoplasie e dell'acne (referenze mancanti).
Meccanismo biologico[modifica | modifica wikitesto]
Il meccanismo d'azione dell'acido retinoico è riassumibile nel meccanismo dell'induzione genica: nel DNA delle cellule cutanee sono presenti geni inducibili dall'acido retinoico. L'acido retinoico attua una vera e propria riprogrammazione cellulare – attraverso azioni di derepressione e repressione genica - che riporta le cellule cutanee in una fase vitale tipica degli organismi in giovane età. Le CRABP (Cellular retinoic acid binding protein) hanno un peso molecolare intorno ai 15.000 dalton e la loro struttura primaria è stata esattamente definita. Queste proteine assolvono la funzione di legare e trasportare l'acido retinoico dal citoplasma verso il nucleo, vera sede della sua azione. Hanno inoltre il ruolo di limitare la quantità endocellulare di acido retinoico, evitando ogni possibilità di sovraccarico. Una volta veicolato al livello nucleare dalle CRABP, l'acido retinoico interagisce con specifici recettori nucleari, denominati RAR (Retinoic Acid Receptor o recettore dell'acido retinoico). Sono stati scoperti tre tipi di recettori nucleari per l'acido retinoico al livello cutaneo, indicati rispettivamente come RAR–alfa, RAR-beta, e RAR-gamma. Quando le RAR, proteine del peso di circa 50.000 dalton, si legano all'acido retinoico formano un complesso capace di interagire con sequenze nucleotidiche del DNA appartenenti a regioni di specifici geni, inducendo da questi la trascrizione di RNA messaggero. Questo processo è stato dimostrato sperimentalmente, per esempio nel caso della sintesi della laminina, una proteina che insieme al collagene di tipo IV e all'eparina solfato entra nella struttura della membrana basale delle cellule epiteliali[2].
Effetti farmacologici[modifica | modifica wikitesto]
Quando viene somministrato come farmaco, l'acido retinoico assume il nome di tretinoina. La tretinoina viene usata soprattutto in modo topico per curare varie patologie dermatologiche quali l'acne, la cheratosi follicolare, melasma e altre malattie riguardanti principalmente il viso, ma è anche nota la sua utilità per attenuare le rughe. È un farmaco che esiste da diversi anni, ed è principalmente ad azione esfoliante, rinnovando gli strati più superficiali del derma, togliendo in questa maniera acne, rughe ed eventuali macchie.
La tretinoina inoltre trova indicazione nel trattamento della leucemia promielocitica acuta (secondo WHO, M3 secondo FAB) quando caratterizzata da una lesione t(15;17), ed è l'unico caso nello spettro delle leucemie mieloidi acute in cui un singolo farmaco assume ruolo terapeutico, peraltro con un ruolo molecolare ben definito (agonista della porzione RARα della proteina chimerica PML-RARα). Storicamente ha costituito il primo caso di terapia oncologica mirata (targeted therapy), anche se la scoperta dell'azione terapeutica fu sostanzialmente casuale, e solo successivamente ne venne messa in luce l'azione specifica[3].
Note[modifica | modifica wikitesto]
- ^ G Duester, Retinoic Acid Synthesis and Signaling during Early Organogenesis, in Cell, vol. 134, n. 6, settembre 2008, pp. 921–31, DOI:10.1016/j.cell.2008.09.002, PMC 2632951, PMID 18805086.
- ^ ^ Edgar Wingender (1993). "Steroid/Thyroid Hormone Receptors". Gene Regulation in Eukaryotes. New York: VCH. pp. 316. ISBN 1-56081-706-2.
- ^ * Siddhartha Mukherjee, L'imperatore del male. Una biografia del cancro, Neri Pozza Editore, luglio 2011, pp. 613-614, ISBN 978-88-545-0331-1.
Voci correlate[modifica | modifica wikitesto]
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) retinoic acid, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.