Utente:D.russo23/Necrolisi epidermica tossica
| Necrolisi epidermica tossica | |
|---|---|
 | |
| Specialità | Dermatologia |
| Eziologia | farmaci; farmaci antibiotici sulfamidici; Micoplasma pneumoniae; citomegalovirus |
| Sede colpita | cute; mucosa orale, oculare e genitale |
| Mortalità mondiale | 20-50% |
| Incidenza mondiale | Più comune nelle donne che negli uomini |
| Classificazione e risorse esterne (EN) | |
| ICD-10 | L51.2 |
| OMIM | 608579 |
| MeSH | D004816 |
| eMedicine | med/2291 derm/405 emerg/599 med/2291 derm/405 |
| Sinonimi | |
| Sindrome di Lyell | |
La necrolisi epidermica tossica (NET) è una forma grave di reazione cutanea. [1]Assieme alla sindrome di Stevens – Johnson (SJS) forma uno spettro della patologia in cui la NET è molto più grave.[1] I primi sintomi includono febbre e sintomi simil-influenzali.[1] Dopo qualche giorno la cute comincia a coprirsi di vesciche e a desquamarsi, formando delle dolorose aree infiammate.[1] Le membrane mucose, come la bocca, sono tipicamente coinvolte.[1] Le complicazioni includono disidratazione, sepsi, polmonite e sindrome da insufficienza multiorgano.[1]
La causa più comune dipende da alcuni farmaci come lamotrigina, carbamazepina, allopurinolo, antibiotici sulfamidici e nevirapina.[1] Altre cause possono includere infezioni quali Micoplasma pneumoniae e citomegalovirus oppure la causa può restare sconosciuta.[2] [3]I fattori di rischio includono HIV/AIDS e lupus eritematoso sistemico.[1] La diagnosi si basa su una biopsia cutanea e sul coinvolgimento di più del 30% della cute.[2] La NET è un tipo di reazione avversa da farmaco (SCARs) grave, assieme alla SJS, la SJS/NET è una reazione da farmaco con eosinofilia e sintomi sistemici.[4] È detta SJS quando sono coinvolti meno del 10% della cute e una forma intermedia con un coinvolgimento che va dal 10 al 30%.[2] L’eritema multiforme (EM) è generalmente considerato un disturbo separato.[5]
ll trattamento solitamente è effettuato in ospedale, nel centro ustioni oppure nel reparto di terapia intensiva.[2][6] I tentativi comprendono l'arresto della causa, antidolorifici e antistaminici.[2][3] Possono essere somministrati anche antibiotici, immunoglobuline per via endovenosa (IVIG) o corticosteroidi.[2][3] Generalmente, i trattamenti non modificano il decorso della patologia preesistente.[2] Insieme alla SJS, la NET colpisce da 1 a 2 persone per milione all’anno.[1] È più comune nelle donne che negli uomini.[2] L’insorgenza tipica si manifesta superati i 40 anni.[2] La cute ricresce nuovamente dopo due o tre settimane; tuttavia, la guarigione può richiedere dei mesi e la maggior parte dei pazienti soffre di disturbi cronici.[2][3]
Sintomatologia[modifica | modifica wikitesto]
Prodromo[modifica | modifica wikitesto]
La NET fondamentalmente si traduce in un ampio coinvolgimento della cute con arrossamento, necrosi e distacco dello strato epidermico superiore e della mucosa. Prima dello sviluppo di questi gravi sintomi, i pazienti spesso hanno un prodromo simil – influenzale, con tosse, rinorrea, febbre, diminuzione dell’appetito e malessere. Una storia clinica di esposizione al farmaco si presenta in media 14 giorni (da una a quattro settimane) prima della comparsa dei sintomi, tuttavia può verificarsi fino a 48 ore in caso di riesposizione.[7]
Osservazioni delle lesioni cutanee[modifica | modifica wikitesto]
Le prime osservazioni delle lesioni cutanee includono papule rosso – violacee, scure e piatte note come macule che cominciano sul tronco e si estendono sul resto del corpo. Queste lesioni cutanee, in seguito, mutano in ampie vescicole epidermiche. La cute colpita successivamente può diventare necrotica o afflosciarsi dal corpo e desquamarsi in ampie strisce.[6]
-
necrolisi epidermica tossica su gambe
-
esempio di NET al quarto giorno con comparsa di vescicole
-
schiena di un paziente affetto da NET al decimo giorno, al picco della patologia
Osservazioni della mucosa[modifica | modifica wikitesto]
In quasi tutti i soggetti affetti da NET vi è un coinvolgimento della cavità orale, oculare e genitale. Su qualsiasi superficie mucosa possono svilupparsi croste cutanee dolorose ed erosioni.[8] L’alimentazione può diventare difficoltosa nel momento in cui la bocca si riempie di vesciche ed è erosa, ciò che delle volte richiede un’alimentazione tramite una sonda nasogastrica, attraverso il naso, oppure tramite una sonda gastrica, direttamente nello stomaco. Gli occhi possono gonfiarsi, formarvisi delle croste ed essere soggetti ad ulcere, che portano ad una potenziale cecità. Il disturbo più comune in relazione agli occhi è una grave congiuntivite.[9]
Complicazioni[modifica | modifica wikitesto]
I soggetti che superano la fase acuta di necrolisi epidermica tossica soffrono di complicazioni a lungo termine che interessano la cute e gli occhi. Le manifestazioni cutanee possono includere cicatrici, nevi melanocitici eruttivi, atrofia vulvovaginale e dispareunia. Il tessuto epiteliale della trachea, dei bronchi o del tratto gastrointestinale può essere coinvolto nella sindrome di Stevens-Johnson e nella NET.[10] I sintomi oculari rappresentano le complicazioni più frequenti nella necrolisi epidermica tossica, sperimentati dal 20-79% dei soggetti con NET, ma anche da soggetti che non manifestano sintomi oculari nell’immediato. Tra questi sintomi vi sono secchezza degli occhi, fotofobia, simblefaron, cicatrici della cornea o xerosi, fibrosi sottocongiuntivale, trichiasi, diminuzione della acuità visiva e cecità.[11]
Cause[modifica | modifica wikitesto]
L’80-95% dei casi di necrolisi epidermica tossica sono stati riscontrati a seguito di una reazione ai farmaci.[5]
I farmaci maggiormente coinvolti nella NET sono:
- antibiotici
- sulfamidici (sulfametossazolo, sulfadiazina, sulfapiridina)
- beta-lattamici (cefalosporine, penicillina, carbapenemi)
- farmaci anti-infiammatori non steroidei (FANS)
- allopurinolo
- antimetaboliti (metotrexato)
- farmaci antiretrovirali (nevirapina)
- corticosteroidi
- ansiolitici (clormezanone)
- anticonvulsivanti (fenobarbital, fenitoina, carbamazepina, lamotrigina e acido valproico).[12][10]
È stato osservato come la necrolisi epidermica tossica derivi da infezioni da Mycoplasma pneumoniae o virus dengue. Anche agenti di contrasto impiegati in studi di imaging, così come trapianto di midollo osseo o di organi, risultano collegati allo sviluppo della NET.[12][5]
HIV[modifica | modifica wikitesto]
I soggetti positivi all’HIV hanno un rischio mille volte superiore di sviluppare la sindrome di Stevens-Johnson e la NET rispetto alla popolazione generale. Il motivo di questo elevato rischio non è chiaro.[6]
Genetica[modifica | modifica wikitesto]
Alcuni fattori genetici sono associati ad un aumento del rischio di necrolisi epidermica tossica. Ad esempio, è stato osservato come alcuni antigeni leucocitari umani tra i quali HLA-B*1502,[13] HLA-A*3101,[14] HLA-B*5801[15] e HLA-B*57:01[16] siano collegati allo sviluppo della NET se esposti a farmaci specifici.
Patogenesi[modifica | modifica wikitesto]
Il ruolo svolto dal sistema immunitario nella patogenesi della necrolisi epidermica tossica non è chiaro. Sembra che un certo tipo di cellula immunitaria (linfocita T CD8+ citotossico) rappresenti la causa principale di apoptosi dei cheratinociti e il successivo distacco cutaneo. I cheratinociti sono cellule collocate nello strato basale dell’epidermide il cui compito è quello di tenere insieme le cellule della pelle circostante. È stato ipotizzato che i linfociti CD8+ diventino iperattivi se stimolati da farmaci o dai metaboliti dei farmaci. I linfociti CD8+, in seguito, mediano l’apoptosi dei cheratinociti attraverso il rilascio di un gran numero di molecole quali perforina, granzima B e granulisina. Altri agenti, incluso il TNFα e il FAS ligand, sembrano altresì essere coinvolti nella NET.[5]
Diagnosi[modifica | modifica wikitesto]
La diagnosi della NET è basata su osservazioni cliniche e istologiche. I primi sintomi della NET possono essere simili a reazioni da farmaco non specifiche, quindi gli specialisti dovrebbero mantenere un elevato indice di sospetto della NET. La presenza di mucosa orale, oculare e/o genitale è utile nella diagnosi poiché queste osservazioni sono presenti in quasi tutti i pazienti affetti da NET. Il segno di Nikolsky (o “Nikolsky diretto”, la separazione dello strato più superficiale del derma, il derma papillare, da quello più profondo dell'epidermide, lo strato basale, mediante una lieve pressione sul bordo laterale) e il segno di Absoe-Hensen (o “Nikolsky indiretto”, l’estensione di una bolla tramite pressione sul bordo laterale) sono due segni diagnostici validi, utilizzati in particolare in dermatologia, che si riscontrano nei pazienti con NET.[6][17][18]
Considerate le elevate morbilità e mortalità causate dalla NET, nonché il miglioramento in termini di esiti per i trattamenti tempestivi, si evidenzia un notevole interesse per la scoperta di biomarcatori sierici durante le prime diagnosi di NET. Alcuni marcatori sierici che hanno dato risultati promettenti nelle prime ricerche sono le proteine granulisina e HMGB1 (High-mobility group protein Box 1).[6]
Istologia[modifica | modifica wikitesto]
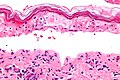
Per una diagnosi definitiva di NET spesso è richiesta una conferma a livello bioptico. Un esame istologico evidenzia come i primi sintomi della NET riguardino la presenza di cheratinociti necrotici diffusi. Si tratta di cellule presenti in tutti gli strati dell’epidermide e responsabili della cheratinizzazione, ivi alterate. In uno stato più avanzato della NET, si può notare la necrosi dell’intero spessore dell’epidermide ed anche la rottura di una bolla subepidermica e l’infiltrato infiammatorio di grado lieve nel derma papillare. La necrosi epidermica che si riscontra nell’esame istologico è un dato sensibile seppure non specifico per la NET.[6]
-
Necrosi epidermica confluente, con basso livello di magnesio
-
Necrosi epidermica confluente, con alto livello di magnesio
Diagnosi differenziale[modifica | modifica wikitesto]
- Sindrome della cute ustionata da stafilococco (detta anche “Malattia di Ritter”)
- Malattia da depositi lineari di immunoglobuline A (IgA) indotta dall’uso di farmaci
- Malattia acuta da rigetto (GVHD)
- Pustolosi esantematica acuta generalizzata (AGEP)
- Eritrodermia
- Reazione da farmaco con eosinofilia e sintomi sistemici (DRESS)
- Eruzione cutanea generalizzata di tipo morbilliforme[19]
Trattamenti[modifica | modifica wikitesto]
Il trattamento principale utilizzato per la NET riguarda l’interruzione dell’agente eziologico individuato (solitamente sulfamidici e altri antibiotici), la gestione iniziale nel centro ustioni o nel reparto di terapia intensiva, gli interventi assistenziali e il supporto nutrizionale.[6]
La letteratura vigente non sostiene in modo convincente l’uso di qualsiasi terapia sistemica adiuvante. L’interesse iniziale per le immunoglobuline per uso endovenoso (IVIG) deriva dalle ricerche in vitro che dimostrano la possibilità di inibire il recettore FAS, il quale causa l’apoptosi se attivato da specifici ligandi.[20] Sfortunatamente, dalle ricerche emerge un parere discordante riguardo l’uso del trattamento IVIG nei trattamenti della NET.[21] La possibilità di trarre conclusioni meno specifiche dalle ricerche finora è stata limitata dalla mancanza di controllo dei trial e dalle incoerenze evidenziate nei progetti di ricerca in termini di gravità della malattia, di dosi di IVIG e di frequenza della somministrazione di IVIG.[6] Sono necessari trial maggiori e di alta qualità per valutare i benefici reali che il trattamento IVIG può apportare ai pazienti con NET.
Diverse terapie adiuvanti sono state tentate per il trattamento della NET, compresi corticosteroidi, ciclosporine, ciclofosfamide, plasmaferesi, pentossifillina, acetilcisteina, ulinastatina, infliximab e il fattore di crescita granulocitario (G-CSF o GCSF), quest’ultimo se si verifica una combinazione della NET con la leucopenia. I dati non sono uniformi per quanto concerne l’uso di corticosteroidi e sono esigui per le altre terapie.[6] Una meta-analisi del 2002 ha concluso che non c’è un dato attendibile per il trattamento della NET.[22] La talidomide non manifesta alcun beneficio ed è stata associata ad un tasso di mortalità maggiore rispetto al trattamento con placebo.[22]
Prognosi[modifica | modifica wikitesto]
Il tasso di mortalità per la necrolisi epidermica tossica varia tra il 25% e il 30%.[6] La prognosi delle persone affette da SJS o NET provocate dai farmaci risulta migliore prima che il farmaco causale sia interrotto.[10] La desquamazione rende i pazienti vulnerabili alle infezioni causate da funghi e da batteri. Inoltre, può tradursi in sepsi, causa principale di decesso osservata nella malattia.[12] Il decesso è provocato dall’infezione o dalla dispnea, dovuta alla polmonite o a danni al lining delle vie respiratorie. Un’analisi microscopica del tessuto (specialmente del grado di infiammazione dell’infiltrato mononucleare nel derma e di infiammazione in generale) può essere significativa nella formulazione della prognosi di ogni singolo caso.[23]
Punteggio SCORTEN[modifica | modifica wikitesto]
Il “Punteggio della gravità della necrolisi epidermica tossica” (SCORTEN) è un sistema di punteggio elaborato per valutare la gravità della NET e pronosticare il tasso di mortalità nei pazienti in uno stato avanzato di NET.[24]
Ognuno dei seguenti fattori assegna un punto:[11][25]
- Età > 40
- Frequenza cardiaca > 120 battiti/min
- Diagnosi di tumore
- Percentuale di superficie cutanea sfaldata o compromessa ≥ 10%
- Azoto ureico presente nel sangue > 28 mg/dl
- Glucosio > 252 mg/dl (14 mmol/l)
- Bicarbonato < 20 mEq/l
Punteggio[modifica | modifica wikitesto]
- 0-1: 3,2% di mortalità
- 2: 12,2% di mortalità
- 3: 35,3% di mortalità
- 4: 58,3% di mortalità
- ≥5: 90% di mortalità
Degno di nota, questo sistema di punteggio è più valido se viene utilizzato il primo e il terzo giorno di ospedalizzazione. Può sottostimare il tasso di mortalità nei pazienti con problemi respiratori.[11]
Note[modifica | modifica wikitesto]
- ^ a b c d e f g h i April W. Armstrong, General Dermatology, Elsevier, 2009, pp. 23–28, ISBN 978-0-7020-3093-2. URL consultato il 7 maggio 2021.
- ^ a b c d e f g h i j Waleed M. Sweileh, Bibliometric analysis of literature on toxic epidermal necrolysis and Stevens-Johnson syndrome: 1940 – 2015, in Orphanet Journal of Rare Diseases, vol. 12, n. 1, 18 gennaio 2017, DOI:10.1186/s13023-017-0566-8. URL consultato il 7 maggio 2021.
- ^ a b c d Joseph Johnson, The Joseph Johnson Letterbook, Oxford University Press, 28 gennaio 2016, pp. 26–28, ISBN 978-0-19-964424-7. URL consultato il 7 maggio 2021.
- ^ N.R. Adler, A.K. Aung e E.N. Ergen, Recent advances in the understanding of severe cutaneous adverse reactions, in British Journal of Dermatology, vol. 177, n. 5, 29 settembre 2017, pp. 1234–1247, DOI:10.1111/bjd.15423. URL consultato il 7 maggio 2021.
- ^ a b c d Robert A. Schwartz, Patrick H. McDonough e Brian W. Lee, Toxic epidermal necrolysis, in Journal of the American Academy of Dermatology, vol. 69, n. 2, 2013-08, pp. 173.e1–173.e13, DOI:10.1016/j.jaad.2013.05.003. URL consultato il 7 maggio 2021.
- ^ a b c d e f g h i j Robert A. Schwartz, Patrick H. McDonough e Brian W. Lee, Toxic epidermal necrolysis, in Journal of the American Academy of Dermatology, vol. 69, n. 2, 2013-08, pp. 187.e1–187.e16, DOI:10.1016/j.jaad.2013.05.002. URL consultato il 7 maggio 2021.
- ^ Marion H. Jordan, Mark S. Lewis e James G. Jeng, Treatment of Toxic Epidermal Necrolysis by Burn Units, in Journal of Burn Care & Rehabilitation, vol. 12, n. 6, 1991-11-XX, pp. 579–581, DOI:10.1097/00004630-199111000-00015. URL consultato il 7 maggio 2021.
- ^ Jean Claude Roujeau e Robert S. Stern, Severe Adverse Cutaneous Reactions to Drugs, in New England Journal of Medicine, vol. 331, n. 19, 10 novembre 1994, pp. 1272–1285, DOI:10.1056/nejm199411103311906. URL consultato il 7 maggio 2021.
- ^ Marlene E. Morales, Gary F. Purdue e Steven M. Verity, Ophthalmic Manifestations of Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis and Relation to SCORTEN, in American Journal of Ophthalmology, vol. 150, n. 4, 2010-10, pp. 505–510.e1, DOI:10.1016/j.ajo.2010.04.026. URL consultato il 7 maggio 2021.
- ^ a b c Emanual Maverakis, Elizabeth A. Wang e Kanade Shinkai, Stevens-Johnson Syndrome and Toxic Epidermal Necrolysis Standard Reporting and Evaluation Guidelines, in JAMA Dermatology, vol. 153, n. 6, 1º giugno 2017, pp. 587, DOI:10.1001/jamadermatol.2017.0160. URL consultato il 7 maggio 2021.
- ^ a b c Gerard DeMers, William J. Meurer e Richard Shih, Tissue Plasminogen Activator and Stroke: Review of the Literature for the Clinician, in The Journal of Emergency Medicine, vol. 43, n. 6, 2012-12, pp. 1149–1154, DOI:10.1016/j.jemermed.2012.05.005. URL consultato il 7 maggio 2021.
- ^ a b c B Gerdts, AFPM Vloemans e RW Kreis, Toxic epidermal necrolysis; 15 years’ experience in a Dutch burns centre, in Journal of the European Academy of Dermatology and Venereology, vol. 21, n. 6, 6 febbraio 2007, pp. 781–788, DOI:10.1111/j.1468-3083.2006.02082.x. URL consultato il 7 maggio 2021.
- ^ Shuen-Iu Hung, Wen-Hung Chung e Shiou-Hwa Jee, Genetic susceptibility to carbamazepine-induced cutaneous adverse drug reactions, in Pharmacogenetics and Genomics, vol. 16, n. 4, 2006-04, pp. 297–306, DOI:10.1097/01.fpc.0000199500.46842.4a. URL consultato il 7 maggio 2021.
- ^ Mark McCormack, Ana Alfirevic e Stephane Bourgeois, HLA-A*3101 and Carbamazepine-Induced Hypersensitivity Reactions in Europeans, in New England Journal of Medicine, vol. 364, n. 12, 24 marzo 2011, pp. 1134–1143, DOI:10.1056/nejmoa1013297. URL consultato il 7 maggio 2021.
- ^ M Tohkin, N Kaniwa e Y Saito, A whole-genome association study of major determinants for allopurinol-related Stevens–Johnson syndrome and toxic epidermal necrolysis in Japanese patients, in The Pharmacogenomics Journal, vol. 13, n. 1, 13 settembre 2011, pp. 60–69, DOI:10.1038/tpj.2011.41. URL consultato il 7 maggio 2021.
- ^ Ana Alfirevic, Munir Pirmohamed e Branka Marinovic, Genetic testing for prevention of severe drug-induced skin rash, in Cochrane Database of Systematic Reviews, 17 luglio 2019, DOI:10.1002/14651858.cd010891.pub2. URL consultato il 7 maggio 2021.
- ^ Staff di Medicina OnLine, Segno Asboe-Hansen: indicazioni, esecuzione, positivo, su MEDICINA ONLINE, 28 settembre 2019. URL consultato il 7 maggio 2021.
- ^ (EN) Aneeqa Islam says, Che cosa è il derma?, su News-Medical.net, 2 dicembre 2016. URL consultato il 7 maggio 2021.
- ^ Robert A. Schwartz, Patrick H. McDonough e Brian W. Lee, Toxic epidermal necrolysis, in Journal of the American Academy of Dermatology, vol. 69, n. 2, 2013-08, pp. 187.e1–187.e16, DOI:10.1016/j.jaad.2013.05.002. URL consultato il 7 maggio 2021.
- ^ R. Zajicek, D. Pintar e L. Broz, Toxic epidermal necrolysis and Stevens-Johnson syndrome at the Prague Burn Centre 1998-2008, in Journal of the European Academy of Dermatology and Venereology, vol. 26, n. 5, 14 giugno 2011, pp. 639–643, DOI:10.1111/j.1468-3083.2011.04143.x. URL consultato il 7 maggio 2021.
- ^ R. Rajaratnam, C. Mann e P. Balasubramaniam, Toxic epidermal necrolysis: retrospective analysis of 21 consecutive cases managed at a tertiary centre, in Clinical and Experimental Dermatology, vol. 35, n. 8, 26 aprile 2010, pp. 853–862, DOI:10.1111/j.1365-2230.2010.03826.x. URL consultato il 7 maggio 2021.
- ^ a b Samit Majumdar, Maja Mockenhaupt e Jean-Claude Roujeau, Interventions for toxic epidermal necrolysis, in Cochrane Database of Systematic Reviews, 21 ottobre 2002, DOI:10.1002/14651858.cd001435. URL consultato il 7 maggio 2021.
- ^ Adam M. Quinn, Kimberly Brown e Brian K. Bonish, Uncovering Histologic Criteria With Prognostic Significance in Toxic Epidermal Necrolysis, in Archives of Dermatology, vol. 141, n. 6, 1º giugno 2005, DOI:10.1001/archderm.141.6.683. URL consultato il 7 maggio 2021.
- ^ Robert A. Schwartz, Patrick H. McDonough e Brian W. Lee, Toxic epidermal necrolysis, in Journal of the American Academy of Dermatology, vol. 69, n. 2, 2013-08, pp. 187.e1–187.e16, DOI:10.1016/j.jaad.2013.05.002. URL consultato il 7 maggio 2021.
- ^ Table: Punteggio della gravità della necrolisi epidermica tossica (Severity-of-Illness Score for Toxic Epidermal Necrolysis, SCORTEN), su Manuali MSD Edizione Professionisti. URL consultato il 7 maggio 2021.