Silodosina
| Silodosina | |
|---|---|
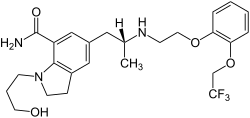 | |
| Nome IUPAC | |
| 1-(3-idrossipropil)-5-[(2R)-({2-[2-[2-(2,2,2-trifluoroethossi)phenossi]etil}ammino)propil]indoline-7-carbossamide | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C25H32F3N3O4 |
| Massa molecolare (u) | 495,534 g/mol |
| Numero CAS | |
| Numero EINECS | 814-909-2 |
| Codice ATC | G04 |
| PubChem | 5312125 |
| DrugBank | DB06207 |
| SMILES | FC(F)(F)COc3ccccc3OCCN[C@H](C)Cc1cc2c(c(c1)C(=O)N)N(CC2)CCCO |
| Dati farmacologici | |
| Modalità di somministrazione | Orale |
| Dati farmacocinetici | |
| Biodisponibilità | 32% |
| Metabolismo | Epatico, glucuronidazione UGT2B7-mediata; coinvolgimento minore di CYP3A4 |
| Emivita | 13±8 ore |
| Escrezione | Renale e fecale |
| Indicazioni di sicurezza | |
La silodosina (nella fase sperimentale conosciuta anche con la sigla KMD-3213)[1] è una molecola che viene utilizzata per il trattamento sintomatico dell'iperplasia prostatica benigna. Rientra nella classe degli α-litici. In Italia il farmaco è venduto nella forma di capsule rigide di gelatina dalla società farmaceutica Recordati con il nome commerciale di Urorec e dalla società farmaceutica Takeda Italia con il nome commerciale di Silodyx.
Storia[modifica | modifica wikitesto]
La silodosina è stata approvata per la commercializzazione in Giappone nel maggio 2006 con il nome commerciale di Urief, dalle compagnie farmaceutiche Kissei Pharmaceutical e Daiichi Sankyo Pharmaceutical. Nell'ottobre 2008, Watson Pharmaceuticals che ne aveva comprato i diritti, ricevette l'approvazione della Food and Drug Administration per la commercializzazione negli USA. Negli Stati Uniti la silodosina è venduta con il nome commerciale di Rapaflo, in Europa con quello di Silodyx e Urorec, e in India con quello di Rapilif.
Farmacodinamica[modifica | modifica wikitesto]
La silodosina è un antagonista adrenergico selettivo per gli α1A-adrenorecettori[2] localizzati in particolare nella prostata, nel fondo e nel collo della vescica urinaria, nella capsula e nell'uretra prostatica. Il blocco recettoriale determina rilassamento della muscolatura liscia delle stazioni indicate e comporta un miglioramento del flusso urinario e una riduzione della sintomatologia propria dell'ipertrofia prostatica benigna. La selettività del farmaco fa sì che silodosina causi raramente ipotensione ortostatica,[3] diversamente da quanto avviene con altri farmaci α1 antagonisti. D'altro canto la sua alta selettività sembra poter causare con maggior frequenza problemi di eiaculazione retrograda.[4][5][6]
Farmacocinetica[modifica | modifica wikitesto]
Dopo somministrazione per via orale la silodosina viene ben assorbita dal tratto gastrointestinale. La biodisponibilità assoluta è pari a circa il 32%. L'assunzione contemporanea con cibo riduce la concentrazione plasmatica massima (Cmax) e aumenta la Tmax. Il legame con le proteine plasmatiche è pari al 97%. Nell'organismo la silodosina viene metabolizzata principalmente tramite glucuronazione (UGT2B7 mediata, UDP-Glucuronosiltransferasi-2B7) e per opera del citocromo P450 isoforma 3A4 (CYP 3A4). La silodosina non sembra avere attività di inibizione o induzione del citocromo P450. Il farmaco viene escreto principalmente sotto forma di diversi metaboliti, per il 30% circa nelle urine e per il 55% nelle feci.[7][8][9]
Usi clinici[modifica | modifica wikitesto]
La silodosina è indicata nel trattamento dei sintomi urinari in soggetti affetti da iperplasia prostatica benigna: difficoltà a dare inizio alla minzione, sensazione di incompleto svuotamento della vescica, necessità frequente di urinare particolarmente di notte (nicturia).[10][11][12][13]
Effetti collaterali e indesiderati[modifica | modifica wikitesto]
Nel corso del trattamento con silodosina si possono verificare: eiaculazione retrograda e aneiaculazione,[14][15] disfunzione erettile,[16] capogiro, ipotensione ortostatica, diarrea, nausea e secchezza delle fauci, riduzione della libido.[5] In alcuni pazienti sottoposti a intervento di cataratta è stata riscontrata la comparsa di sindrome intraoperatoria dell’iride a bandiera, cioè di una sindrome che affligge durante tali interventi alcuni pazienti in trattamento con α1-bloccanti o precedentemente trattati con α1-bloccanti, e che comporta maggiori complicazioni legate alla procedura dell'intervento stesso.
Controindicazioni[modifica | modifica wikitesto]
La silodisina è controindicata nei soggetti con ipersensibilità nota al principio attivo oppure a uno qualsiasi degli eccipienti. Inoltre il farmaco è sconsigliato nei pazienti con insufficienza renale grave (clearance della creatinina inferiore a 30 mL/min)
Dosi terapeutiche[modifica | modifica wikitesto]
Nell'adulto la dose consigliata è di 8 mg al giorno. La capsula, deglutita intera, preferibilmente con un bicchiere d'acqua, deve essere assunta con il cibo, ogni giorno, meglio se sempre alla stessa ora. Nei soggetti affetti da insufficienza renale lieve (clearance della creatinina minore di 80 mL/min) non è necessario alcun aggiustamento della posologia. Nei soggetti con insufficienza renale moderata (clearance della creatinina minore di 50 mL/min) è utile cominciare la terapia con 4 mg una volta al giorno. A giudizio del medico, se necessario, trascorsa una settimana di trattamento il dosaggio può essere successivamente aumentato a 8 mg.
Note[modifica | modifica wikitesto]
- ^ K. Akiyama, M. Hora; S. Tatemichi; N. Masuda; S. Nakamura; R. Yamagishi; M. Kitazawa, KMD-3213, a uroselective and long-acting alpha(1a)-adrenoceptor antagonist, tested in a novel rat model., in J Pharmacol Exp Ther, vol. 291, n. 1, Ott 1999, pp. 81-91, PMID 10490890.
- ^ S. Yamada, T. Okura; R. Kimura, In vivo demonstration of alpha(1A)-adrenoceptor subtype selectivity of KMD-3213 in rat tissues., in J Pharmacol Exp Ther, vol. 296, n. 1, gennaio 2001, pp. 160-7, PMID 11123376.
- ^ M. Yoshida, Y. Homma; K. Kawabe, Silodosin, a novel selective alpha 1A-adrenoceptor selective antagonist for the treatment of benign prostatic hyperplasia., in Expert Opin Investig Drugs, vol. 16, n. 12, Dic 2007, pp. 1955-65, DOI:10.1517/13543784.16.12.1955, PMID 18042003.
- ^ A. Nagai, R. Hara; T. Yokoyama; Y. Jo; T. Fujii; Y. Miyaji, Ejaculatory dysfunction caused by the new alpha1-blocker silodosin: A preliminary study to analyze human ejaculation using color Doppler ultrasonography., in Int J Urol, vol. 15, n. 10, Ott 2008, pp. 915-918, DOI:10.1111/j.1442-2042.2008.02136.x, PMID 18721206.
- ^ a b R. Furuya, N. Masumori; S. Furuya; H. Ogura; M. Mutoh; K. Kobayashi; S. Hisasue; T. Tsukamoto, [Investigation of adverse events and the continuance rate of silodosin in all patients who received silodosin for lower urinary tract symptoms suggestive of benign prostatic hyperplasia]., in Nihon Hinyokika Gakkai Zasshi, vol. 101, n. 1, gennaio 2010, pp. 13-7, PMID 20158073.
- ^ K. Kobayashi, N. Masumori; S. Hisasue; R. Kato; K. Hashimoto; N. Itoh; T. Tsukamoto, Inhibition of Seminal emission is the main cause of anejaculation induced by a new highly selective alpha1A-blocker in normal volunteers., in J Sex Med, vol. 5, n. 9, Set 2008, pp. 2185-90, DOI:10.1111/j.1743-6109.2008.00779.x, PMID 18399947.
- ^ Y. Matsubara, T. Kanazawa; Y. Kojima; Y. Abe; K. Kobayashi; H. Kanbe; H. Harada; Y. Momose; S. Terakado; Y. Adachi; I. Midgley, [Pharmacokinetics and disposition of silodosin (KMD-3213)]., in Yakugaku Zasshi, 126 Spec no., marzo 2006, pp. 237-45, PMID 16518089.
- ^ T. Shimizu, I. Miyashita; Y. Matsubara; M. Ikeda; M. Yamaguchi, [Pharmacokinetic profile of silodosin in clinical practice]., in Yakugaku Zasshi, 126 Spec no., marzo 2006, pp. 257-63, PMID 16518091.
- ^ MA. Cantrell, HR. Bream-Rouwenhorst; P. Hemerson; JS. Magera, Silodosin for benign prostatic hyperplasia., in Ann Pharmacother, vol. 44, n. 2, febbraio 2010, pp. 302-10, DOI:10.1345/aph.1M320, PMID 20071497.
- ^ M. Rossi, T. Roumeguère, Silodosin in the treatment of benign prostatic hyperplasia., in Drug Des Devel Ther, vol. 4, 2010, pp. 291-7, DOI:10.2147/DDDT.S10428, PMID 21116335.
- ^ MP. Curran, Silodosin in the treatment of the signs and symptoms of benign prostatic hyperplasia: profile report., in Drugs Aging, vol. 28, n. 10, Ott 2011, pp. 843-5, DOI:10.2165/11207800-000000000-00000, PMID 21970311.
- ^ M. Yoshida, J. Kudoh; Y. Homma; K. Kawabe, Safety and efficacy of silodosin for the treatment of benign prostatic hyperplasia., in Clin Interv Aging, vol. 6, 2011, pp. 161-72, DOI:10.2147/CIA.S13803, PMID 21753871.
- ^ M. Yoshida, J. Kudoh; Y. Homma; K. Kawabe, New clinical evidence of silodosin, an α(1A) selective adrenoceptor antagonist, in the treatment for lower urinary tract symptoms., in Int J Urol, vol. 19, n. 4, aprile 2012, pp. 306-16, DOI:10.1111/j.1442-2042.2011.02957.x, PMID 22251148.
- ^ Y. Homma, K. Kawabe; M. Takeda; M. Yoshida, Ejaculation disorder is associated with increased efficacy of silodosin for benign prostatic hyperplasia., in Urology, vol. 76, n. 6, Dic 2010, pp. 1446-50, DOI:10.1016/j.urology.2010.03.015, PMID 20472263.
- ^ F. Shimizu, M. Taguri; Y. Harada; Y. Matsuyama; K. Sase; M. Fujime, Impact of dry ejaculation caused by highly selective alpha1A-blocker: randomized, double-blind, placebo-controlled crossover pilot study in healthy volunteer men., in J Sex Med, vol. 7, n. 3, marzo 2010, pp. 1277-83, DOI:10.1111/j.1743-6109.2009.01663.x, PMID 20102447.
- ^ Silodosin: erectile and ejaculatory disorders., in Prescrire Int, vol. 21, n. 127, Mag 2012, p. 129, PMID 22844684.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su silodosina
Wikimedia Commons contiene immagini o altri file su silodosina