Neuroradiologia della regione sellare
La neuroradiologia della regione sellare si avvale principalmente dell'imaging a risonanza magnetica ed in secondo luogo della tomografia computerizzata. La regione della sella turcica comprende al suo interno varie strutture anatomiche di cui la più importante è l'ipofisi. Essendo questa regione anatomicamente complessa e di dimensioni ridotte è importante che le metodiche radiologiche impiegate per indagarla abbiano un'elevata risoluzione spaziale. Gli adenomi ipofisari costituiscono più del 90% delle masse occupanti spazio a livello di questa regione, che tuttavia può nel suo contesto mostrare molte altre anomalie fisiologiche e patologiche anche a carico di altre strutture qui localizzate o confinanti[1].
Metodiche neuroradiologiche
[modifica | modifica wikitesto]L'imaging a risonanza magnetica è come già detto la metodica di prima istanza per studiare le lesioni occupanti spazio in sede sellare. Di solito per indagare questa regione si usano matrici di acquisizione ad alta definizione (512x512 pixel) e strati sottili (2-3 millimetri). Obbiettivo della RM è definire in primo luogo sia l'estensione sia i rapporti della lesione con le strutture vicine e quindi diagnosticare l'eventuale causa di ipersecrezione di ormoni ipofisari. Il protocollo standard per questa regione prevede acquisizioni mediante sequenze T1 pesate nei piani sagittale e coronale sia in condizioni basali che dopo somministrazione di mezzo di contrasto, oltre a sequenze T2 pesate nei pieni coronali. In aggiunta possono essere eseguite sequenze Gradient Echo per ricercare depositi di calcio o sostanze paramagnetiche, FLAIR per lo studio di lesioni a contenuto liquido come i dermoidi, SPIR con tecnica di soppressione del grasso per lo studio post-operatorio, di teratomi e lipomi. Le sequenze pesate in diffusione sono utili per la diagnosi di ischemia e della apoplessia pituitaria, mentre gli studi dinamici con mezzo di contrasto consentono di evidenziare anche adenomi molto piccoli (in tal caso usare intervalli di acquisizione brevi di circa 10-20 secondi per evidenziare la tipica impregnazione transitoria caratteristica degli adenomi).
La TC è impiegata per ricercare eventuali calcificazioni intralesionali e per studiare l'osso sfenoide sia nel sospetto di suo interessamento da parte della lesione sia in vista di un intervento neurochirurgico. Le metodiche Angio-TC ed Angio-RM sono in rari casi utilizzate per lo studio della patologia vascolare in tale sede. In caso di sindrome di Cushing con quadro RM negativo è possibile eseguire un prelievo ematico per via endovascolare a livello dei seni petrosi inferiori (IPSS) per la ricerca di gradienti centro-periferia o laterolaterali nella secrezione di ormone adrenocorticotropo utili all'eventuale localizzazione di un microadenoma non rilevato dalle tecniche di imaging[2].
Quadro di normalità
[modifica | modifica wikitesto]La neuroipofisi in condizioni normali appare iperintensa nelle sequenze T1 pesate per via del suo elevato contenuto di vasopressina mentre l'adenoipofisi mostra intenso potenziamento dopo somministrazione di mezzo di contrasto in quanto sprovvista di barriera emato-encefalica, per tali motivi la RM è estremamente accurata per lo studio di questa regione. L'iperintensità in T1 tipica della neuroipofisi come anche le dimensioni della ghiandola (anche fino a 12 mm) sono maggiori nei soggetti giovani e nei neonati, come anche durante la gravidanza e subito dopo il parto[3].
Patologie congenite
[modifica | modifica wikitesto]Nel nanismo ipofisario l'ipofisi o il suo peduncolo possono apparire normali all'imaging oppure essere di dimensioni ridotti o assenti. È possibile osservare anche ectopia ipofisaria associata ad altre malformazioni.
L'amartoma ipofisario è costituito da sostanza grigia ectopica localizzata a livello del tuber cinereum, pertanto mostra lo stesso segnale RM della corteccia normale e non si potenzia dopo somministrazione di mezzo di contrasto.
La cisti di Rathke origina dalla tasca di Rathke ed è una metaplasia ipofisaria caratterizzata da segnale iperintenso nelle sequenze T1 pesate ed ipointenso in quelle T2 pesate a causa del suo alto contenuto in proteine. Non mostra potenziamento dopo somministrazione di mezzo di contrasto.
Dermoidi e teratomi di solito insorgono in sede mediana anteriormente ai corpi mammillari e sono iperintensi nelle sequenze T1 pesate in modo simile al grasso (nelle sequenze SPIR si osserva caduta di questo segnale)[4].
Adenomi ipofisari
[modifica | modifica wikitesto]
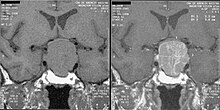
Gli adenomi ipofisari costituiscono il 10-15% di tutti i tumori primitivi cerebrali ed il 90% di quelli ipofisari. La classificazione WHO li distingue in tipici, atipici, associati a coristomi ed in carcinomi. Le forme invasive sono caratterizzate da comportamento aggressivo, indice Ki-67 di proliferazione maggiore del 3% e presenza della proteina P53 a livello del nucleo. Clinicamente e neuroradiologicamente queste lesioni sono distinte in micro e macroadenomi oltre che in secernenti e non secernenti (i microadenomi di solito sono secernenti, i macroadenomi no). In tutti i casi la prima linea di trattamento e medica o chirurgica, volto ad eliminare la causa della secrezione ormonale o a controllarla per quanto riguarda le forme secernenti e ad eliminare l'effetto massa per i macroadenomi. Le forme non secernenti una volta operate spesso tendono a recidivare ed in tali casi è indicata la radiochirurgia.
I microadenomi possono modificare la forma della ghiandola rendendola asimmetrica, slivellando il pavimento sellare o deviando il peduncolo, tuttavia più spesso si manifestano clinicamente per la secrezione ormonale. Di solito queste lesioni appaiono ipointense nelle sequenze T1 pesate basali, tuttavia nel 25% dei casi possono apparire isointensi, motivo per cui è indispensabile completare l'imaging con acquisizioni dopo mezzo di contrasto (che aumenta il segnale a livello dell'adenoipofisi sana incrementandone quindi il contrasto con la lesione). In alcuni casi possono sanguinare spontaneamente e quindi mostrare segnale iperintenso nelle sequenze T1 pesate (comportamento tipico del prolattinoma). L'80% dei microprolattinomi appare iperintenso anche nelle sequenze T2 pesate, mentre gli adenomi secernenti ormone della crescita sono di solito iso-ipointensi in T2. Lo studio dinamico con mezzo di contrasto è particolarmente indicato per la ricerca di microadenomi secernenti ACTH che di solito hanno dimensioni inferiori ai 3 mm (picoadenomi).
I macroadenomi di solito sono non secernenti, tuttavia le forme secernenti GH sono particolarmente aggressive e recidivanti. Queste lesioni hanno forma policiclica o ovalare e deformano la regione sellare ampliandola e comprimendo il chiasma ottico (ben visibile nelle sequenze T2 pesate). L'invasione laterale del seno cavernoso è un fattore prognostico sfavorevole in quanto rende più complicato il trattamento chirurgico (tale quadro radiologico non è di semplice interpretazione e di solito il seno si considera sicuramente invaso se la carotide è completamente circondata dalla lesione). Il segnale in T1 di queste lesioni è sempre ipointenso, anche se meno rispetto ai microadenomi e rispetto a questi si presenta eterogeneo per la presenza nel loro contesto di aree ischemiche e necrotiche. Dopo somministrazione del mezzo di contrasto è possibile distinguere agevolmente il parenchima sano (spesso dislocato e compresso in periferia) dal corpo della lesione. Nel 20% dei casi i macroadenomi possono sanguinare mostrando segnale iperintenso alle sequenze T1 pesate ed ipointenso in quelle T2 pesate per la presenza di prodotti di degradazione dell'emoglobina, oltre ad un possibile livello in fase subacuta per sedimentazione della componente corpuscolata. I prolattinomi trattati con bromocriptina sono spesso soggetti a sanguinamenti e spesso questi episodi clinicamente si manifestano con cefalea. Un macroadenoma può anche manifestarsi clinicamente con un quadro di apoplessia ipofisaria. La RM può essere utilizzata anche per la ricerca di recidive post-chirurgiche, che presentano lo stesso segnale del tumore che dovrebbe essere stato asportato (le acquisizioni in caso di interventi molto invasivi vanno eseguite dopo 3 mesi dall'intervento per evitare falsi positivi dovuti al materiale riassorbibile inserito nel cavo sellare, secrezioni ed aderenze. In tali casi le sequenze SPIR possono essere di aiuto, come anche per delimitare al meglio la neuroipofisi)[5].
Altre neoplasie sellari
[modifica | modifica wikitesto]


Il craniofaringioma può originare lungo tutto il decorso del dotto nasofaringeo (dal III ventricolo alla faringe) quindi anche in sede sellare. Alla RM appare come una massa disomogenea composta da componenti solide e cistiche. Tali cisti contengono metaemoglobina, cheratina, colesterolo e proteine e pertanto appaiono iperintense nelle sequenze T1 pesate, mentre la TC è perfetta per evidenziare le tipiche calcificazioni nodulari o lineari localizzate alla periferia della lesione. L'aspetto neuroradiologico di queste lesioni è quasi patognomonico, tuttavia diagnosi differenziale può essere fatta con i dermoidi, le cisti dermoidi e quelle del Rathke mediante le mappe ADC che mostrano valori più elevati per i craniofaringiomi.
I carcinomi ipofisari sono molto rari e di solito originano da adenomi invasivi secernenti spesso prolattina o ACTH. Neuroradiologicamente sono identici alle loro controparti benigne da cui possono essere distinti solo per la presenza di metastasi lungo l'asse craniospinale o a organi distanti per via ematica (osso e fegato).
L'astrocitoma ipofisario è un tumore raro ad origine dalla neuroipofisi (di solito è un astrocitoma pilocitico) e ha aspetto neuroradiologico spesso aspecifico. Tali masse sono a volte isointense in T1 con la corteccia ed iperintense nelle sequenze T2 pesate, inoltre mostrano potenziamento dopo somministrazione di mezzo di contrasto. In molti casi tuttavia l'unico segno radiologico che può aiutare nella diagnosi è la dislocazione anteriore della neuroipofisi.
Il germinoma è un tumore tipico dell'infanzia causato da cellule staminali totipotenti che di solito ha doppia localizzazione a livello dell'ipofisi e dell'epifisi. Tale dato assieme alla clinica ed alla produzione di marker specifici come alfa-fetoproteina e gonadotropina corionica è importante per la diagnosi. La lesione primitiva è ipointensa nelle sequenze T1 pesate, iperintensa in quelle T2 pesate e si potenzia in modo omogeneo dopo somministrazione di mezzo di contrasto. È indispensabile studiare tutto l'asse cranio-spinale in quanto questo tumore da spesso metastasi endoliquorali.
Il linfoma primitivo ipofisario è un tumore rarissimo spesso evidente come lesione ipointensa nelle sequenze T2 pesate per via dell'alta cellularità. Di solito è costituito da lesioni secondarie a partenza da altre zone dell'encefalo per via endoliquorale.
Praticamente tutti i tumori solidi possono dare metastasi ipofisarie, in particolare il tumore del polmone ed il tumore della mammella. Il loro aspetto RM è molto vario. e di solito interessano il lobo posteriore dell'ipofisi dando distruzione ossea dello sfenoide[6].
Neoplasie parasellari
[modifica | modifica wikitesto]Il secondo tumore più frequente dopo l'adenoma nella regione parasellare è il meningioma.
ll neurinoma del nervo, del chiasma o del tratto ottico può entrare in diagnosi differenziale con il craniofaringioma.
I gliomi dell'ipotalamo di solito sono più aggressivi di quelli del chiasma ottico ed infiltrano il terzo ventricolo
Il cordoma origina dai residui della notocorda e si presenta con segnale disomogeneo nelle sequenze T1 e T2 pesate. Le calcificazioni sono ben evidenti alla TC o alle sequenze GRE.
Il carcinoma del rinofaringe può diffondere fino all'ipofisi per via neuronale o per continuità. Per localizzare l'origine precisa della lesione possono essere utili le sequenze T1 SPIR dopo mezzo di contrasto
Gli epidermoidi dell'angolo ponto-cerebellare possono raggiungere la sella turcica per continuità dal terzo ventricolo. Presentano segnale simil-liquorale e le sequenze FLAIR permettono di distinguerli dalle cisti aracnoidee[7].
Lesioni vascolari
[modifica | modifica wikitesto]È possibile rilevare a livello della sella turcica aneurismi della carotide intracavernosa o fistole carotido-cavernose, queste ultime di origine traumatica ed associate ad esoftalmo, soffio intracranico e chemosi congiuntivale (triade caratteristica)[8].
Ipofisite
[modifica | modifica wikitesto]L'ipofisite è una rara malattia infiammatoria che può avere varia eziologia e prognosi:
L'ipofisite linfocitaria ha genesi autoimmune e microscopicamente è caratterizzata da infiltrazione dell'organo in toto o in parte da parte di linfociti e plasmacellule. Alla RM si osserva ingrandimento ghiandolare, intensa impregnazione dopo somministrazione di mezzo di contrasto, scomparsa della fisiologica iperintensità in T1 della neuroipofisi ed associato interessamento delle meningi, dello sfenoide e dell'infundibolo. L'interessamento infundibolare e l'assenza di slargamento sellare permettono di distinguere questa condizione dall'adenoma.
L'istiocitosi a cellule di Langerhans può interessare anche l'ipofisi dando clinicamente un diabete insipido e neuroradiologicamente vivace impregazione del mezzo di contrasto a carico dell'organo.
Tubercolosi e sarcoidosi possono anch'esse interessare l'ipofisi dando un quadro RM simile a quello descritto in precedenza con diffusa impregnazione del mezzo di contrasto a livello dell'organo, del peduncolo e delle meningi adiacenti[9].
Note
[modifica | modifica wikitesto]- ^ Manuale di Neuroradiologia, Poletto Editore, p. 546-547.
- ^ Manuale di Neuroradiologia, Poletto Editore, p. 547-548.
- ^ Manuale di Neuroradiologia, Poletto Editore, p. 548.
- ^ Manuale di Neuroradiologia, Poletto Editore, p. 549-550.
- ^ Manuale di Neuroradiologia, Poletto Editore, p. 550-555.
- ^ Manuale di Neuroradiologia, Poletto Editore, p. 555-557.
- ^ Manuale di Neuroradiologia, Poletto Editore, p. 558-559.
- ^ Manuale di Neuroradiologia, Poletto Editore, p. 560-561.
- ^ Manuale di Neuroradiologia, Poletto Editore, p. 562.
Bibliografia
[modifica | modifica wikitesto]- Massimo Gallucci, Cosma Andreula, Sossio Cirillo e Tommaso Scarabino, Manuale di Neuroradiologia, Poletto Editore, 2016, ISBN 978-88-95033-61-7.
- Shanika Samarasinghe, Mary Ann Emanuele e Alaleh Mazhari, Neurology of the pituitary, in Neurologic Aspects of Systemic Disease Part II, Elsevier, 2014, DOI:10.1016/b978-0-7020-4087-0.00047-4, ISSN 0072-9752.
- Donald W. Pfaff e Marian Joëls, Hormones, brain, and behavior, Amsterdam [Netherlands], 2016, ISBN 978-1-78684-205-3, OCLC 980555610.