Acido gluconico: differenze tra le versioni
m r2.7.1) (Bot: Aggiungo: uk:Глюконова кислота |
→Collegamenti esterni: Update link |
||
| Riga 94: | Riga 94: | ||
==Collegamenti esterni== |
==Collegamenti esterni== |
||
*[http://webbook.nist.gov/cgi/cbook.cgi?Name=Gluconic+acid&Units=SI Gluconic acid on NIST.gov] |
*[http://webbook.nist.gov/cgi/cbook.cgi?Name=Gluconic+acid&Units=SI Gluconic acid on NIST.gov] |
||
*[http://chemsub.online.fr/ |
*[http://chemsub.online.fr/name/acido_gluconico.html ChemSub Online : Acido gluconico.] |
||
{{Portale|chimica}} |
{{Portale|chimica}} |
||
Versione delle 16:49, 29 mag 2011
| Acido gluconico | |
|---|---|
 | |
 | |
| Nomi alternativi | |
| acido 2,3,4,5,6-pentaidrossiesanoico | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H12O7 |
| Massa molecolare (u) | 196,16 |
| Aspetto | cristalli incolore |
| Numero CAS | |
| Numero EINECS | 208-401-4 |
| PubChem | 10690 |
| DrugBank | DBDB13180 |
| SMILES | C(C(C(C(C(C(=O)O)O)O)O)O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,24 |
| Temperatura di fusione | 404,15 (131 °C) |
| Temperatura di ebollizione | 690,15 (417 °C) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
| Frasi R | 36/37/38 |
| Frasi S | 26-28-37/39-45 |
L'acido gluconico è un composto organico con formula bruta C6H12O7 e formula molecolare HOCH2(CHOH)4COOH. In soluzione acquosa a pH neutro, l'acido carbossilico è presente in forma dissociata, determinando lo ione gluconato; i corrispettivi sali sono chiamati gluconati. L'acido gluconico e i gluconati sono molto presenti in natura poiché questi composti hanno origine dall'ossidazione del glucosio.
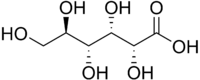
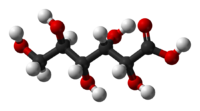
Struttura chimica
L'acido gluconico è composto da una catena formata da sei atomi di carbonio con cinque gruppi idrossilici e, a un'estremità, un gruppo carbossilico. In soluzione acquosa l'acido gluconico è i equilibrio con il proprio estere ciclico (glucono-δ-lattone).
Utilizzo
L'acido gluconico è presente naturalmente nella frutta, miele e vino. È aggiunto come additivo come regolatore di acidità. È anche utilizzato in prodotti per la pulizia: l'acido gluconico è in grado di dissolvere depositi di minerali, soprattutto in presenza di pH basico. Lo ione gluconato, con una carica netta negativa (anione), chela Ca2+, Fe2+, Al3+, e altri metalli pesanti. Il gluconato di calcio è utilizzato nel trattamento di ustioni da acido fluoridrico.
Bibliografia
- The Merck Index. 9th ed. Rahway, New Jersey: Merck & Co., Inc., 1976., p. 575
- Budavari, S. (ed.). The Merck Index - Encyclopedia of Chemicals, Drugs and Biologicals. Rahway, NJ: Merck and Co., Inc., 1989., p. 699
- Weast, R.C. and M.J. Astle. CRC Handbook of Data on Organic Compounds. Volumes I and II. Boca Raton, FL: CRC Press Inc. 1985., p. V1 661
- Kirk-Othmer Encyclopedia of Chemical Technology. 4th ed. Volumes 1: New York, NY. John Wiley and Sons, 1991-Present., p. V8 265