Vaccino anti-morbillo
Il vaccino del morbillo è una preparazione liofilizzata di un adatto ceppo vivo attenuato di virus morbilloso che viene utilizzato per indurre immunità attiva contro il morbillo. Il vaccino stimola risposta immunitaria adattativa e fornisce protezione a lungo termine contro la malattia. L'inizio della protezione è lento, ma l'effetto è di lunga durata. Il vaccino è sulla lista dei farmaci essenziali redatta dall'Organizzazione Mondiale della Sanità (OMS). Alla fine degli anni Ottanta a causa del morbillo morivano ancora più di un milione di bambini ogni anno.[1][2] In commercio sono disponibili il vaccino bivalente del morbillo e della parotite e il vaccino trivalente del morbillo, della parotite e della rosolia (cosiddetto vaccino MPR).
Farmacodinamica
[modifica | modifica wikitesto]Il virus morbilloso viene coltivato su cellule di embrioni di pollo (provenienti da allevamenti di animali sani ed esenti da leucosi aviaria) o su altre cellule adatte. Durante la preparazione del vaccino al mezzo di coltura possono essere aggiunti adatti antibiotici, alla minima concentrazione efficace. Il vaccino deve essere iniettato immediatamente dopo essere stato ricostituito con un idoneo solvente. Il titolo del virus non deve essere inferiore a 103,0CCID503 (ovvero la quantità di virus che infetta il 50% delle colture cellulari) per ogni singola dose di vaccino. Il vaccino divalente è una preparazione liofilizzata sterile ottenuta da adatti ceppi vivi attenuati di virus del morbillo e da adatti ceppi vivi attenuati di virus della parotite. Anche in questo caso al vaccino può essere aggiunto un adatto agente antimicrobico. Il vaccino trivalente è una preparazione liofilizzata mista contenente adatti ceppi vivi attenuati di virus del morbillo, della parotite (Paramyxovirus parotitidis) e della rosolia. I virus sono coltivati in embrioni di pollo, in cellule di embrioni di pollo o in altre adatte colture cellulari. Il vaccino, a cui non deve essere aggiunto alcun conservante antimicrobico, deve essere ricostituito immediatamente prima dell'uso. Ogni dose deve contenere non meno di 103,0CCID503 di virus infettivi del morbillo, non meno di 103,7CCID503 di virus infettivi della parotite e non meno di 103CCID503 di virus infettivi della rosolia. La preparazione riportata nella U.S. Pharmacopeial Convention (USP) può contenere un adatto agente antimicrobico. Quando viene neutralizzato con un antisiero specifico, il vaccino non è in grado di infettare le colture di cellule sensibili. Quando viene mescolato con una miscela di antisieri specifici dei virus del morbillo, della parotite e della rosolia, il vaccino trivalente non è più in grado di infettare colture di cellule sensibili.
Usi clinici
[modifica | modifica wikitesto]
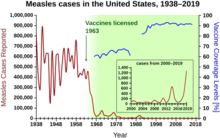

Il vaccino del morbillo viene utilizzato per indurre immunità attiva contro il morbillo. In Gran Bretagna e negli USA la vaccinazione di routine contro il morbillo è raccomandata per tutti i bambini durante il secondo anno di vita (si utilizza generalmente il vaccino MPR, ovvero il vaccino trivalente del morbillo, della parotite e della rosolia). Somministrare il vaccino prima di quest'età non appare vantaggioso in quanto gli anticorpi della madre contro il morbillo, acquisiti passivamente dal bambino, possono ostacolare lo sviluppo dell'immunità. Studi recenti sembrano indicare una preferenza della somministrazione del vaccino al quindicesimo mese d'età in quanto nei bambini più piccoli la sieroconversione si svilupperebbe in modo più lento.
Dosi terapeutiche
[modifica | modifica wikitesto]Negli Stati Uniti viene consigliata la somministrazione di due dosi di vaccino per quei bambini che vivono in aree dove la trasmissione del morbillo è ricorrente. La prima dose viene somministrata al nono mese d'età come vaccino monocomponente e la seconda circa al quindicesimo mese. Se i bambini vengono vaccinati con la prima dose dopo aver già compiuto l'anno d'età si ricorre al vaccino trivalente. Normalmente la prima dose viene somministrata a 12-18 mesi e la seconda dose viene somministrata in età scolare. Uno studio australiano ha confermato che una singola dose di vaccino morbillo-parotite-rosolia è insufficiente a garantire l'eradicazione del morbillo dalla regione.[3] Un ulteriore studio ha evidenziato che non vi sarebbe alcun vantaggio nel ritardare la vaccinazione fino al compimento dei 15 mesi e che le attuali raccomandazioni per la vaccinazione in età dai 12 ai 15 mesi dovrebbe rimanere.[4] Oggi c'è la tendenza a rivaccinare gli individui esposti in caso di focolaio di morbillo nelle scuole o nei collegi.
In Gran Bretagna vengono impiegati vaccini contro il morbillo preparati sia dal ceppo Schwarz che dal ceppo Edmonston di Enders, più attenuato. Entrambi sono somministrati alla dose di 0,5 ml (non meno di 1000 CCID50) per via sottocutanea o intramuscolare.
Nei Paesi in via di sviluppo il vaccino viene normalmente somministrato ai bambini di nove mesi.[5][6][7] In alcuni casi è stato somministrato a bambini di sei mesi un vaccino ad alta attività ottenuto da ceppi Edmonston-Zagreb.[8][9] Il vaccino singolo contro il morbillo può essere impiegato anche a scopo profilattico somministrandolo entro 72 ore dall'esposizione al virus del morbillo. Durante un'epidemia di morbillo la vaccinazione può essere eseguita anche in bambini di età inferiore ai 6 mesi.[10][11] Tuttavia in tutti coloro che sono stati vaccinati prima di aver compiuto un anno, è opportuno eseguire una nuova vaccinazione all'età normalmente raccomandata. In caso sia richiesto di vaccinare i bambini prima del compimento dell'anno di vita (ad esempio per l'improvvisa necessità di un viaggio non rinviabile in regioni endemiche), una seconda dose di vaccino deve essere somministrata non prima di quattro settimane ed entro tre mesi dopo la prima dose, comunque non dopo il compimento del secondo anno di vita.[12]
Effetti collaterali e indesiderati
[modifica | modifica wikitesto]In seguito alla somministrazione del vaccino del morbillo si possono manifestare febbre e rash cutanei. La febbre (39,4 °C o più) generalmente compare 5-10 giorni dopo l'iniezione, perdura per circa 1-2 giorni e talora è accompagnata da crisi convulsive. Possono manifestarsi inoltre coriza, congiuntivite, faringite e tosse.[13] Vi sono state alcune segnalazioni di deficit dell'udito da cause neurosensoriali a seguito della vaccinazione contro il morbillo, sia utilizzando il vaccino monovalente, sia il bivalente (morbillo e rosolia), sia il trivalente (MPR).[14][15][16][17] Molto più raramente sono stati associati all'uso del vaccino effetti più gravi, ed in particolare porpora trombocitopenica[18][19][20] e encefalite.[21] A proposito di quest'ultima va ricordato che l'incidenza di encefalite o di encefalopatia a seguito di vaccinazione (frequenza inferiore a 1 ogni 10 milioni di dosi) è decisamente inferiore al tasso di incidenza di panencefalite subacuta sclerosante, una nota complicanza di diverse malattie naturali (frequenza in caso di morbillo: 1 ogni 1000–2000 casi; in caso di parotite: 2–4 ogni 1000 casi; in caso di rosolia circa 1 ogni 6000 casi).[22][23]
Nei soggetti che vengono vaccinati contro il morbillo e sono successivamente esposti all'infezione è possibile che si manifesti una sindrome morbillosa atipica, caratterizzata da febbre elevata e da rash atipici (vescicole, papule e piccole emorragie),[24] dolore addominale e polmonite.[25][26] La prima segnalazione della sindrome risale al 1965 ed era stata descritta in soggetti ai quali era stato somministrato il vaccino inattivato (non più in uso).[27][28][29] Tuttavia la sindrome è possibile che si manifesti anche in pazienti immunizzati con vaccino vivo.[30][31][32] Non vi sono evidenze mediche che collegano la vaccinazione antimorbillo al verificarsi di autismo.[33][34][35][36]
Controindicazioni
[modifica | modifica wikitesto]Una volta ai bambini con un passato di convulsioni o i cui genitori o fratelli presentavano epilessia idiopatica all'anamnesi, si raccomandava la somministrazione contemporanea del vaccino del morbillo e di un'immunoglobulina umana normale diluita in modo particolare; oggi si consiglia che tali bambini vengano vaccinati nello stesso modo dei bambini sani, associando però un adatto trattamento profilattico contro le convulsioni febbrili. Il vaccino non dovrebbe essere somministrato ai bambini con meno di un anno d'età, nei quali gli anticorpi della madre potrebbero diminuire la risposta immunitaria. Il vaccino del morbillo può ridurre temporaneamente la risposta alla tubercolina o ad altri test cutanei.
La somministrazione del vaccino monocomponente e del trivalente è consigliata nei bambini HIV-positivi sintomatici, compresi quelli in AIDS conclamato, poiché non causa gravi effetti collaterali ed evita la morte del bambino per morbillo.[37]
Precauzioni per la conservazione
[modifica | modifica wikitesto]Il vaccino del morbillo in forma liofilizzata e il vaccino trivalente devono essere conservati a temperatura compresa tra 2 e 8 °C, evitandone il congelamento. Sia la forma liofilizzata che il vaccino ricostituito dovrebbero essere protetti dalla luce che può inattivare il virus. In tali condizioni di conservazione sia il vaccino vivo del morbillo che il vaccino trivalente hanno validità di un anno dalla data dell'ultima determinazione virale.
Note
[modifica | modifica wikitesto]- ^ Aaby P, Clements CJ, Measles immunization research: a review, in Bulletin of the World Health Organization, vol. 67, n. 4, 1989, pp. 443–8, PMC 2491276, PMID 2680141.
- ^ Morley D, Saving children's lives by vaccination, in BMJ (Clinical Research Ed.), vol. 299, n. 6715, 1989, pp. 1544–5, PMC 1838768, PMID 2514892.
- ^ Levy MH, Bridges-Webb C, "Just one shot" is not enough--measles control and eradication, in The Medical Journal of Australia, vol. 152, n. 9, maggio 1990, pp. 489–91, PMID 2381342.
- ^ Kakakios AM, Burgess MA, Bransby RD, Quinn AA, Allars HM, Optimal age for measles and mumps vaccination in Australia, in The Medical Journal of Australia, vol. 152, n. 9, maggio 1990, pp. 472–4, PMID 2381338.
- ^ Hall AJ, Greenwood BM, Whittle H, Modern vaccines. Practice in developing countries, in Lancet, vol. 335, n. 8692, marzo 1990, pp. 774–7, PMID 1969519.
- ^ Cutts FT, Dabis F, [Measles control in developing countries], in Santé (Montrouge, France), vol. 4, n. 3, 1994, pp. 163–71, PMID 7921681. URL consultato il 13 dicembre 2014.
- ^ Tulchinsky TH, Ginsberg GM, Abed Y, Angeles MT, Akukwe C, Bonn J, Measles control in developing and developed countries: the case for a two-dose policy, in Bulletin of the World Health Organization, vol. 71, n. 1, 1993, pp. 93–103, PMC 2393424, PMID 8440043.
- ^ Markowitz LE, Sepulveda J, Diaz-Ortega JL, Valdespino JL, Albrecht P, Zell ER, Stewart J, Zarate ML, Bernier RH, Immunization of six-month-old infants with different doses of Edmonston-Zagreb and Schwarz measles vaccines, in The New England Journal of Medicine, vol. 322, n. 9, marzo 1990, pp. 580–7, DOI:10.1056/NEJM199003013220903, PMID 2304505. URL consultato il 13 dicembre 2014.
- ^ Whittle HC, Campbell H, Rahman S, Armstrong JR, Antibody persistence in Gambian children after high-dose Edmonston-Zagreb measles vaccine, in Lancet, vol. 336, n. 8722, ottobre 1990, pp. 1046–8, PMID 1977029.
- ^ de Serres G, Boulianne N, Ratnam S, Corriveau A, Effectiveness of vaccination at 6 to 11 months of age during an outbreak of measles, in Pediatrics, vol. 97, n. 2, febbraio 1996, pp. 232–5, PMID 8584383.
- ^ Berger R, Just M, Glück R, Grassi M, Wegmann A, Measles vaccination in early infancy, in Lancet, vol. 335, n. 8688, marzo 1990, pp. 540, PMID 1968549.
- ^ Hill DR, Pearson RD, Measles prophylaxis for international travel, in Annals of Internal Medicine, vol. 111, n. 9, novembre 1989, pp. 699–701, PMID 2552886. URL consultato il 13 dicembre 2014.
- ^ Advisory Committee on Immunization Practices (ACIP), Update: vaccine side effects, adverse reactions, contraindications, and precautions. Recommendations of the Advisory Committee on Immunization Practices (ACIP), in MMWR. Recommendations and Reports : Morbidity and Mortality Weekly Report. Recommendations and Reports / Centers for Disease Control, vol. 45, RR-12, settembre 1996, pp. 1–35, PMID 8801442. URL consultato il 14 dicembre 2014.
- ^ Brodsky L, Stanievich J, Sensorineural hearing loss following live measles virus vaccination, in International Journal of Pediatric Otorhinolaryngology, vol. 10, n. 2, novembre 1985, pp. 159–63, PMID 4093255.
- ^ Nabe-Nielsen J, Walter B, Unilateral total deafness as a complication of the measles-mumps-rubella vaccination, in Scandinavian Audiology. Supplementum, vol. 30, 1988, pp. 69–70, PMID 3227284.
- ^ Jayarajan V, Sedler PA, Hearing loss following measles vaccination, in The Journal of Infection, vol. 30, n. 2, marzo 1995, pp. 184–5, PMID 7636291.
- ^ Asatryan A, Pool V, Chen RT, Kohl KS, Davis RL, Iskander JK, Live attenuated measles and mumps viral strain-containing vaccines and hearing loss: Vaccine Adverse Event Reporting System (VAERS), United States, 1990--2003, in Vaccine, vol. 26, n. 9, febbraio 2008, pp. 1166–72, DOI:10.1016/j.vaccine.2007.12.049, PMID 18255204. URL consultato il 14 dicembre 2014.
- ^ Bachand AJ, Rubenstein J, Morrison AN, Thrombocytopenic purpura following live measles vaccine, in American Journal of Diseases of Children (1960), vol. 113, n. 2, febbraio 1967, pp. 283–5, PMID 6066937.
- ^ Mantadakis E, Farmaki E, Buchanan GR, Thrombocytopenic purpura after measles-mumps-rubella vaccination: a systematic review of the literature and guidance for management, in The Journal of Pediatrics, vol. 156, n. 4, aprile 2010, pp. 623–8, DOI:10.1016/j.jpeds.2009.10.015, PMID 20097358. URL consultato il 14 dicembre 2014.
- ^ Cecinati V, Principi N, Brescia L, Giordano P, Esposito S, Vaccine administration and the development of immune thrombocytopenic purpura in children, in Human Vaccines & Immunotherapeutics, vol. 9, n. 5, maggio 2013, pp. 1158–62, DOI:10.4161/hv.23601, PMC 3899154, PMID 23324619. URL consultato il 14 dicembre 2014.
- ^ Duclos P, Ward BJ, Measles vaccines: a review of adverse events, in Drug Safety, vol. 19, n. 6, dicembre 1998, pp. 435–54, PMID 9880088.
- ^ Anonimo, SSPE in the developing world, in Lancet, vol. 336, n. 8715, settembre 1990, pp. 600, PMID 1975383.
- ^ Zilber N, Rannon L, Alter M, Kahana E, Measles, measles vaccination, and risk of subacute sclerosing panencephalitis (SSPE), in Neurology, vol. 33, n. 12, dicembre 1983, pp. 1558–64, PMID 6685828.
- ^ Smith H, Measles again, in British Medical Journal, vol. 280, n. 6216, marzo 1980, pp. 766–7, PMC 1600552, PMID 7370649.
- ^ Laptook A, Wind E, Nussbaum M, Shenker IR, Pulmonary lesions in atypical measles, in Pediatrics, vol. 62, n. 1, luglio 1978, pp. 42–6, PMID 683782.
- ^ Hall WJ, Hall CB, Atypical measles in adolescents: evaluation of clinical and pulmonary function, in Annals of Internal Medicine, vol. 90, n. 6, giugno 1979, pp. 882–6, PMID 443684. URL consultato il 13 dicembre 2014.
- ^ Rauh Lw, Schmidt R, Measles immunization with killed virus vaccine. Serum antibody titers and experience with exposure to measles epidemic, in American Journal of Diseases of Children (1960), vol. 109, marzo 1965, pp. 232–7, PMID 14246070.
- ^ Gokiert JG, Beamish WE, Altered reactivity to measles virus in previously vaccinated children, in Canadian Medical Association Journal, vol. 103, n. 7, ottobre 1970, pp. 724–7, PMC 1930557, PMID 5506106.
- ^ Cherry JD, Feigin RD, Lobes LA, Shackelford PG, Atypical measles in children previously immunized with attenuated measles virus vaccines, in Pediatrics, vol. 50, n. 5, novembre 1972, pp. 712–7, PMID 5084185.
- ^ Nichols EM, Atypical measles syndrome: a continuing problem, in American Journal of Public Health, vol. 69, n. 2, febbraio 1979, pp. 160–2, PMC 1619057, PMID 760575.
- ^ Chatterji M, Mankad V, Failure of attenuated viral vaccine in prevention of atypical measles, in Jama, vol. 238, n. 24, dicembre 1977, pp. 2635, PMID 579203. URL consultato il 13 dicembre 2014.
- ^ Henderson JA, Hammond DI, Delayed diagnosis in atypical measles syndrome, in Canadian Medical Association Journal, vol. 133, n. 3, agosto 1985, pp. 211–3, PMC 1346153, PMID 4016627.
- ^ Maglione MA, Das L, Raaen L, Smith A, Chari R, Newberry S, Shanman R, Perry T, Goetz MB, Gidengil C, Safety of vaccines used for routine immunization of U.S. children: a systematic review, in Pediatrics, vol. 134, n. 2, agosto 2014, pp. 325–37, DOI:10.1542/peds.2014-1079, PMID 25086160. URL consultato il 14 dicembre 2014.
- ^ Peltola H, Patja A, Leinikki P, Valle M, Davidkin I, Paunio M, No evidence for measles, mumps, and rubella vaccine-associated inflammatory bowel disease or autism in a 14-year prospective study, in Lancet, vol. 351, n. 9112, maggio 1998, pp. 1327–8, DOI:10.1016/S0140-6736(98)24018-9, PMID 9643797. URL consultato il 14 dicembre 2014.
- ^ DeStefano F, MMR vaccine and autism: a review of the evidence for a causal association, in Molecular Psychiatry, 7 Suppl 2, 2002, pp. S51–2, DOI:10.1038/sj.mp.4001181, PMID 12142951. URL consultato il 14 dicembre 2014.
- ^ D'Souza J, Todd T, Measles-mumps-rubella vaccine and the development of autism or inflammatory bowel disease: the controversy should end, in The Journal of Pediatric Pharmacology and Therapeutics : JPPT : the Official Journal of PPAG, vol. 8, n. 3, luglio 2003, pp. 187–99, DOI:10.5863/1551-6776-8.3.187, PMC 3469143, PMID 23118678.
- ^ Krasinski K, Borkowsky W, Measles and measles immunity in children infected with human immunodeficiency virus, in Jama, vol. 261, n. 17, maggio 1989, pp. 2512–6, PMID 2704110. URL consultato il 13 dicembre 2014.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Vaccino del morbillo
Wikimedia Commons contiene immagini o altri file su Vaccino del morbillo