Desossicorticosterone
| Desossicorticosterone | |
|---|---|
 | |
| Nome IUPAC | |
| (1S,2R,10S,11S,14S,15S)-14-(2-idrossiacetil)-2,15-dimetiltetraciclo[8.7.0.02,7.011,15]eptadec-6-en-5-one | |
| Nomi alternativi | |
| DOC | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C21H30O3 |
| Massa molecolare (u) | 330,461 |
| Numero CAS | |
| Numero EINECS | 200-596-4 |
| Codice ATC | H02 |
| PubChem | 6166 |
| DrugBank | DB15972 |
| SMILES | CC12CCC3C(C1CCC2C(=O)CO)CCC4=CC(=O)CCC34C |
| Indicazioni di sicurezza | |
Il desossicorticosterone (DOC) detto anche 11-deossicorticosterone o 21-idrossiprogesterone) è un ormone steroide prodotto dalla ghiandola surrenale che possiede attività mineralcorticoide e agisce come un precursore dell'aldosterone. Come suggerito dal nome, esso può essere inteso come la variante 21-idrossi del progesterone o la variante 11-desossi del corticosterone. Questo ormone non ha una significativa attività glucocorticoide.[1]
È noto anche come cortexone, deossicortone, desossicortone e composto B.
Galleria d'immagini[modifica | modifica wikitesto]
Fisiologia del desossicorticosterone[modifica | modifica wikitesto]
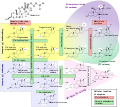
L'11-desossicorticosterone è una molecola precursore necessaria per la produzione di aldosterone. La via principale per la produzione di aldosterone si trova localizzata anatomicamente nella zona glomerulare surrenalica della ghiandola surrenale. È prodotto a partire dal progesterone ad opera della 21β-idrossilasi e viene convertito in corticosterone attraverso la 11β-idrossilasi. Il corticosterone viene poi convertito in aldosterone dalla aldosterone sintasi.[2]
La maggior parte del deossicorticosterone è secreta dalla zona fascicolata della corteccia surrenale che secerne anche il cortisolo, e una piccola quantità dalla zona glomerulare, che secerne aldosterone. Il DOC stimola i tubuli collettori renali (i tubuli della porzione terminale del nefrone)[3] a continuare ad espellere potassio, azione questa simile a quella dell'aldosterone. Diversamente dall'aldosterone stesso il sito d'azione non è rappresentato dalla parte distale del tubulo distale.[4] Nello stesso tempo il DOC non è così efficace come l'aldosterone nella sua azione sodio ritentiva,[5] risultando circa 20 volte meno potente.[6] Il DOC infatti è normalmente responsabile solo dell'1% della ritenzione di sodio[7] Oltre alla sua intrinseca mancanza di forza nell'azione sodio ritentiva va detto che esiste anche un meccanismo di "fuga" dall'azione del DOC, verosimilmente mediato da un ormone non steroideo.[8] Questa "fuga" nel giro di pochi gironi fa venire meno il potere sodio ritentivo del DOC, proprio come accade anche per l'aldosterone.[9] L'ormone responsabile del meccanismo di "fuga" potrebbe essere l'ormone peptidico callicreina,[10] che è aumentata dal DOC e soppressa dall'aldosterone.[11] Se la concentrazione di sodio diventa molto alta, il DOC aumenta il flusso di urina.[3] Il DOC ha circa 1/20 del potere sodio ritentivo dell'aldosterone.[12] Dal momento che il DOC ha circa 1/5 della potenza d'escrezione di potassio rispetto all'aldosterone[12] probabilmente necessita della cooperazione dell'aldosterone, se il contenuto di potassio sierico diventa troppo elevato.[13] Ciò è probabilmente legato al fatto che l'aldosterone sta già stimolando l'escrezione di potassio. Quando il sodio è basso il DOC probabilmente non avrebbe nemmeno dovuto essere presente, ma quando il sodio sale l'aldosterone cala considerevolmente, ed il DOC probabilmente tende a prendere il sopravvento.
Il DOC e l'aldosterone hanno un feedback simile rispetto al potassio. Un aumento del potassio sierico provoca un aumento della secrezione di DOC.[14] Tuttavia, il sodio ha un effetto limitato,[15] e l'effetto che ha è diretto..[12] L'angiotensina (ormone correlato alla pressione arteriosa) ha invece scarsi effetti sul DOC,[16] ma il DOC causa una rapida caduta della renina, e quindi della angiotensina I, il precursore della angiotensina II.[17] Perciò il DOC deve avere indirettamente un effetto inibente sull'aldosterone, in quanto l'aldosterone dipende dalla angiotensina II. La regolazione della concentrazione del sodio, e quindi del volume del sangue, è di difficile regolazione. In altre parole, quando la concentrazione di sodio diviene elevata e conseguentemente tende ad incrementare la pressione arteriosa, il problema non può essere semplicemente risolto con il trasferimento del sodio nel comparto intracellulare. Al contrario, questo meccanismo di spostamento nel comparto intracellulare è attivabile per il potassio, ed è proprio quanto sembra verificarsi grazie al DOC nei conigli.[17] Quindi il problema di una elevazione del potassio può essere risolto dall'organismo senza ricorrere ad una eliminazione renale di quello che è un minerale pericolosamente scarso e che non può essere processato da un meccanismo di "pompa attiva" indipendentemente dal sodio. Si ricorda che le concentrazioni di potassio vanno mantenute entro un range adeguato, poiché una sua diminuzione può causare una perdita delle capacità di pompa della attività del cuore.[18] La penetrazione del potassio all'interno delle cellule può incrementare un eventuale problema di aumentata concentrazione del sodio, in quanto tale penetrazione si associa ad una fuoriuscita "compensatoria" dalla cellula di una analoga quantità di sodio.[19]
L'ACTH ha maggiore effetto di stimolazione sulla secrezione di DOC che di aldosterone. Probabilmente questo fatto è dovuto alla necessità di un più fine controllo sulla regolamentazione degli elettroliti durante episodi di diarrea[20] ed è rafforzato dall'evidenza che durante la disidratazione l'aldosterone praticamente scompare,[21] perfino quando la renina e l'angiotensina si elevano. È per questo motivo (la scomparsa dell'aldosterone) che supplementare il potassio con integratori durante la disidratazione può essere molto pericoloso, e non dovrebbe essere attuato almeno fino ad un'ora dopo la reidratazione per dare il tempo agli ormoni di raggiungere il nucleo delle cellule ed esplicare i loro effetti.
Lo scopo primario del DOC è la regolazione degli elettroliti, anche se questo ormone ha altri effetti, come la capacità di rimuovere il potassio dai leucociti[22] e dalle cellule muscolari.[23] Inoltre il DOC inibisce la formazione di glicogeno,[24] stimola l'enzima lisil ossidasi[25] ed il tessuto connettivo[26] e queste proprietà possono essere utilizzate dall'organismo per limitare i danni legati alle marcate perdite di potassio correlate ad alcune malattie intestinali.[27]
La maggiore efficienza del DOC nello stimolare l'escrezione di sodio (o forse sarebbe meglio dire la minore efficienza di ritenzione) deve essere in parte legata a cambiamenti nella morfologia delle cellule renali, poiché l'effetto di fuga dalla ritenzione di sodio indotta dal DOC richiede alcuni giorni per materializzarsi. Il Progesterone previene in parte la perdita di potassio stimolata dal DOC.[28]
Note[modifica | modifica wikitesto]
- ^ Costanzo, Linda S., Physiology, Hagerstwon, MD, Lippincott Williams & Wilkins, 2007, ISBN 0-7817-7311-3.
- ^ Mark's Basic Medical Biochemistry: A Clinical Approach
- ^ a b O'Neil RG & Helmans SI, Transport characteristics of renal collecting tubules: influence of DOCA and diet, in American Journal of Physiology, vol. 233, 1977, pp. 544–558.
- ^ Peterson L & Wright FS (1977) Effect of sodium intake on renal potassium excretion. American Journal of Physiology 233; 225-234.
- ^ Ellinghaus K (1971) Sodium and potassium balance during the administration of desoxycorticosterone in dogs with differing intakes. Pfluegers Arch. 322; 347-354.
- ^ From a lost reference by Brommer.
- ^ Ruch TC Fulton JF (1960) Medical Physiology and Biophysics. W.B. Saunders and Co., Phijl & London.
- ^ Pearce JW et al. (1969) Evidence for a humoral factor modifying the renal response to blood volume expansion in the rat. Can. Journal of Physiological Pharm. 47; 377-386.
- ^ Schacht RG et al. (1971) Renal mechanism for DOCA escape in man BulL. N.ew York Academy of Medicine 47; 1233.
- ^ Majima, M I Hayashi T Fujita H Ito S Nakajima (1999) Kallikrein-kinin system prevents the development of hypertension by inhibiting sodium retention. Immunopharmacology 44 issue 1+2; 145-152.
- ^ Bonner G Autenreith R Mari-Grez M Rascher W & Gross F (1981) Horm. Res. 14; 87.
- ^ a b c Oddie CJ et al. 1972 Plasma deoxycorticosterone levels in man with simultaneous measurement of aldosterone corticosterone, cortisol and eoxyotisol. Journal of Clinical Endocrinol. Metab. 34; 1039-54.
- ^ Bauer JH & Gauntner WC (1974) Effect of potassium chloride on plasma renin activity and plasma aldosterone during sodium restriction in normal man. Kidney International 15; Kidney Int. 15; 286.
- ^ Brown RD & Strott CA Liddle GW (1972) Site of stimulation of aldosterone biosynthesis by angiotensin and potassium. Journal of Clinical Investigation 51; 1413-1418.
- ^ Schambelan M & Biglieri EC (1972) Deoxycorticosterone production and regulation in man. Journal of Clinical Endocrinology and Metabolism 34; 695-703.
- ^ Brown RD & Strott CA Liddle GW (1972) del sito di stimolazione della biosintesi di aldosterone da parte dell'angiotensina e potassio. . Journal of Clinical Investigation 51; 1413-1418
- ^ a b Grekin RJ Terris JM Bohr DF 1980 Electrolyte and hormonal effects of deoxycorticosterone acetate in young pigs. Hypertension 2; 326-332.
- ^ Abbrecht PH (1972) Cardiovascular effects of chronic potassium deficiency in the dog. American Journal of Physiology 223; 555-560.
- ^ Rubini ME Chojnocki RF (1972) J. Clin. Nutr. 25;96.
- ^ Weber CE 1998 Cortisol's purpose Medical Hypotheses 51; 289-292.
- ^ Merrill DC Skelton MM Cowley AWJr. (1986) Humoral control of water and electrolyte excretion during water restriction. Kidney International 29; 1152-1161.
- ^ Wilson, D.L. (1957) Direct effects of adrenal corticosteroids on the electrolyte content of rabbit leucocytes. American Journal of Physiology. 190: 104.
- ^ Tobian, L., Jr.; Binion, J.T. (1954) Artery Wall Electrolytes in Renal and DCA Hypertension. Journal of Clinical Investigation 23: 1407.
- ^ Bartlett, G.R>; MacKay, E.M. (1949) Insulin stimulation of glycogen formation in rat abdominal muscle. Proc. Exp. Biological Medicine 71: 493, 1949.
- ^ Weber, C.E. (1984) Copper response to rheumatoid arthritis. Medical Hypotheses 15: 333, 1984.
- ^ Pospisilova, J.; Pospisil, M. (1970) Influence of mineralocorticoids on collagen synthesis in subcutaneous granuloma in adrenalectomized and nonadrenalectomized mice. Physiologia Bohemoslovaca 19: 539,
- ^ Weber CE (1998) Cortisol's purpose. Medical Hypotheses. 51: 289-292.
- ^ Wambach G & Higgins JR (1979) Effect of progesterone on serum and tissue electrolyte concentration in DOCA-treated rats. Hormone Metabolism Research 11; 258-259.
Collegamenti esterni[modifica | modifica wikitesto]
- desossicorticosteróne, su sapere.it, De Agostini.