Bis(difenilfosfino)metano
| Bis(difenilfosfino)metano | |
|---|---|
 | |
 | |
| Nomi alternativi | |
| dppm | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C25H22P2 |
| Massa molecolare (u) | 384,39 |
| Aspetto | polvere cristallina bianca |
| Numero CAS | |
| Numero EINECS | 218-194-2 |
| PubChem | 74952 |
| SMILES | C1=CC=C(C=C1)P(CP(C2=CC=CC=C2)C3=CC=CC=C3)C4=CC=CC=C4 |
| Proprietà chimico-fisiche | |
| Solubilità in acqua | insolubile |
| Temperatura di fusione | 118-119 °C (391-392 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| Frasi H | 315-319-335 |
| Consigli P | 261-305+351+338-302+352-321-405-501 |
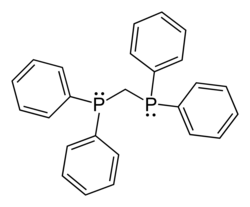
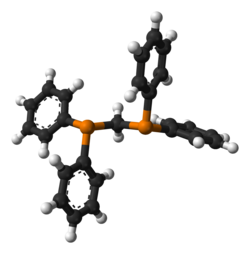
Il bis(difenilfosfino)metano è una fosfina con formula Ph2P-CH2-PPh2 (Ph = fenile). Il nome è generalmente abbreviato come dppm. In condizioni normali è un solido cristallino di colore bianco sensibile all'ossigeno atmosferico. Viene comunemente usato come legante bidentato in chimica inorganica e chimica metallorganica. Il dppm funziona nella maggior parte dei casi come legante a ponte, portando alla formazione di complessi bimetallici, ma può fungere anche da legante chelato.[1]
Sintesi e reattività[modifica | modifica wikitesto]
Per preparare il dppm si parte da trifenilfosfina (PPh3) e sodio, che formano difenilfosfuro di sodio (NaPPh2); quest'ultimo viene quindi trattato con diclorometano (CH2Cl2) per ottenere dppm:[2]
- PPh3 + 2Na → NaPPh2 + NaPh
- 2NaPPh2 + CH2Cl2 → Ph2PCH2PPh2 + 2NaCl
Il gruppo metilene (CH2) è leggermente acido nel dppm e specialmente nei suoi complessi. Il legante può essere ossidato per arrivare ai corrispondenti ossidi e solfuri Ph2P(E)CH2P(E)Ph2 (E = O, S). In questi derivati il gruppo metilene è ancora più acido.
Chimica di coordinazione[modifica | modifica wikitesto]

Come legante chelato il dppm può formare cicli a quattro termini MP2C che sono alquanto tensionati. Il legante preferisce legarsi a ponte formando complessi bimetallici; in tal caso si formano cicli a cinque termini M2P2C termodinamicamente favoriti. Un esempio è il dimero di palladio Pd2Cl2(dppm)2. Il ddpm dà luogo ad una famiglia di composti di coordinazione noti come complessi con struttura ad A.[4]
Indicazioni di sicurezza[modifica | modifica wikitesto]
Il composto è disponibile in commercio. È irritante per gli occhi, la pelle e le vie respiratorie. Non ci sono dati che indichino proprietà cancerogene. È considerato poco pericoloso per l'ambiente.[5]
Note[modifica | modifica wikitesto]
- ^ Cotton et al. 1999
- ^ Hewertson e Watson 1962
- ^ Besenyei et al. 2002
- ^ Albéniz ed Espinet 2006
- ^ Alfa Aesar, Scheda di dati di sicurezza del dppm (PDF), su alfa.com. URL consultato il 21 novembre 2011.
Bibliografia[modifica | modifica wikitesto]
- A. C. Albéniz e P. Espinet, Palladium: Inorganic & Coordination Chemistry, in Encyclopedia of Inorganic Chemistry, Wiley, 2006, DOI:10.1002/0470862106.ia178.
- G. Besenyei, L. Párkányia, E. Gács-Baitza e B. R. James, Crystallographic characterization of the palladium(I) dimers, syn-Pd2Cl2(dppmMe)2 and Pd2Cl2(dppm)2; solution conformational behavior of syn- and anti-Pd2Cl2(dppmMe)2 and their (μ-Se) adducts [dppmMe=μ-1,1-bis(diphenylphosphino)ethane, and DPPM=μ-bis(diphenylphosphino)methane], in Inorg. Chim. Acta, vol. 327, n. 1, 2002, pp. 179–187, DOI:10.1016/S0020-1693(01)00682-X. URL consultato il 18 novembre 2011.
- F. A. Cotton, G. Wilkinson, C. A. Murillo e M. Bochmann, Advanced Inorganic Chemistry, 6ª ed., Wiley, 1999, ISBN 978-0-471-19957-1.
- W. Hewertson e H. R. Watson, 283. The preparation of di- and tri-tertiary phosphines, in J. Chem. Soc., 1962, pp. 1490–1494, DOI:10.1039/JR9620001490. URL consultato il 14 novembre 2011.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su bis(difenilfosfino)metano
Wikimedia Commons contiene immagini o altri file su bis(difenilfosfino)metano