Sesquisolfuro di fosforo
| Trisolfuro di tetrafosforo | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| trisolfuro di tetrafosforo | |
| Nomi alternativi | |
| sesquisolfuro di fosforo | |
| Caratteristiche generali | |
| Formula bruta o molecolare | P4S3 |
| Massa molecolare (u) | 220,093 |
| Aspetto | solido giallo |
| Numero CAS | |
| Numero EINECS | 215-245-0 |
| PubChem | 14818 |
| SMILES | P12P3P1SP(S2)S3 |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,08 |
| Temperatura di fusione | 172,5 °C (445,7 K) |
| Temperatura di ebollizione | 408 °C (681,2 K) |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −154 |
| Indicazioni di sicurezza | |
| Temperatura di autoignizione | 100 °C (373 K) |
| Simboli di rischio chimico | |
  
| |
| pericolo | |
| Frasi H | 228 - 260 - 302 - 400 [1] |
| Consigli P | --- |
Sesquisolfuro di fosforo è il nome più comune del composto inorganico di formula P4S3. Il nome più corretto è trisolfuro di tetrafosforo. È uno dei due solfuri di fosforo di importanza commerciale. È un solido giallo, ma quando non è puro il colore del composto può essere verdino o grigio. Il composto fu descritto nel 1864 dal chimico francese Clément Georges Lemoine, e fu prodotto per la prima volta industrialmente nel 1898 dalla ditta Albright and Wilson. Viene usato per la produzione dei fiammiferi accendibili ovunque.
Struttura molecolare[modifica | modifica wikitesto]
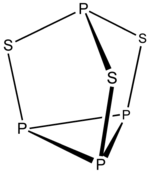
P4S3 è un composto molecolare; la molecola ha simmetria C3v e deriva dall'inserzione dello zolfo nella struttura tetraedrica di P4, lasciando intatto uno dei cicli P3. Le distanze P−S e P−P sono rispettivamente 209,0 e 223,5 pm. P4S3 e P4Se3 hanno la medesima struttura.[2]
Sintesi[modifica | modifica wikitesto]
P4S3 viene prodotto riscaldando a più di 180 °C una opportuna miscela di zolfo e fosforo rosso. In presenza di un eccesso di zolfo si forma invece P4S10. Il P4S3 grezzo viene quindi purificato per distillazione o per ricristallizzazione da toluene. Si stima che nel 1989 ne siano state prodotte 150 tonnellate.[3]
Reattività[modifica | modifica wikitesto]
P4S3 è il più stabile dei solfuri di fosforo, è un solido insolubile in acqua fredda, ma molto solubile in disolfuro di carbonio (100g in 100mL a 17 °C) e benzene (11,1 g in 100 mL a 30 °C). A temperatura ambiente non reagisce con l'acqua, a differenza degli altri solfuri di fosforo che vengono idrolizzati. Ad alta temperatura reagisce con acqua e vapore formando ossidi di fosforo e solfuro di idrogeno, H2S; quest'ultimo è particolarmente pericoloso in quanto tossico e infiammabile. P4S3 è facilmente infiammabile per riscaldamento e per frizione. Per combustione in aria produce fumi tossici di diossido di zolfo, SO2.
Usi[modifica | modifica wikitesto]
Una miscela 1:2 di P4S3 e clorato di potassio, KClO3, insieme ad altri materiali, è usata nella testa dei fiammiferi accendibili ovunque.[4]
Note[modifica | modifica wikitesto]
- ^ Scheda del composto su GESTIS [1] consultata il 16.03.2023.
- ^ Y. C. Leung, J. Waser, S. van Houten, A. Vos, G. A. Wiegers, E. H. Wiebenga, The crystal structure of P4S3, in Acta Crystallographica, vol. 10, 1957, pp. 574-582, DOI:10.1107/S0365110X57002042. URL consultato il 26 novembre 2010.
- ^ G. Bettermann, W. Krause, G. Riess, T. Hofmann, Phosphorus Compounds, Inorganic in Ullmann's Encyclopedia of Industrial Chemistry, Weinheim, Wiley-VCH, 2002, DOI:10.1002/14356007.a19_527.
- ^ D. E. C. Corbridge, Phosphorus: an outline of its chemistry, biochemistry, and technology, 5ª ed., Amsterdam, Elsevier, 1995, I fiammiferi sono discussi alle pagine 115-116, ISBN 0-444-89307-5.
Bibliografia[modifica | modifica wikitesto]
- N. N. Greenwood, A. Earnshaw, Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Sesquisolfuro di fosforo
Wikimedia Commons contiene immagini o altri file su Sesquisolfuro di fosforo