Saponificazione

La saponificazione è il processo di idrolisi di un estere trattato con idrossidi di metalli alcalini e successivamente con acidi, con conseguente formazione di un acido carbossilico (o di un anione carbossilato) e di un alcol. Solitamente si impiega l'idrossido di sodio (o soda caustica, NaOH), oppure l'idrossido di potassio (KOH), in base alla consistenza finale desiderata, con un trigliceride per produrre il corrispettivo sale sodico (carbossilato, più propriamente). Assieme al sapone, i tradizionali processi di saponificazione producono glicerolo. Si definiscono “saponificabili” tutte le sostanze convertibili in sapone. A quest'ultimo si possono aggiungere additivi per conferirgli particolari caratteristiche (ad esempio sabbia e pomice per renderlo abrasivo).[1]
Saponificazione dei trigliceridi[modifica | modifica wikitesto]
Gli oli vegetali e i grassi animali sono le principali sostanze solitamente saponificate. Questi materiali oleosi, chiamati trigliceridi, sono miscugli di diversi acidi grassi. I trigliceridi possono essere convertiti in saponi con due diversi processi. Il processo tradizionale avviene in un passaggio: il trigliceride è trattato con una base forte (ad esempio NaOH), che accelera la scissione dei legami carbonilici e produce glicerolo e il sale dell'acido grasso costituente. Questo è il metodo più largamente utilizzato a livello industriale per la produzione di glicerolo. Se necessario, i saponi possono essere precipitati per “salting out” con una soluzione satura di cloruro di sodio. Il numero di saponificazione è la quantità di base richiesta per saponificare un campione di grasso. Per la produzione di sapone, i trigliceridi sono opportunamente purificati, ma la saponificazione include anche altre idrolisi basiche di trigliceridi non puri, come ad esempio la conversione dei lipidi di un cadavere in adipocera. Questo processo è più comune in corpi dove la quantità di tessuto adiposo è maggiore, non aggrediti da agenti decompositori e sepolti in terreni particolarmente alcalini.
Meccanismo dell'idrolisi basica[modifica | modifica wikitesto]
Il meccanismo di lisi degli esteri prevede una serie di reazioni di equilibrio.[2] L'anione idrossido si addiziona (“attacca”) al gruppo carbonilico dell'estere. L'intermedio di reazione si chiama ortoestere:
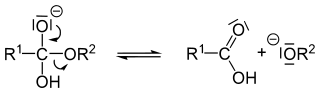
L'espulsione dell'alcossido genera un acido carbossilico:
L'alcossido è una base più forte della base coniugata dell'acido carbossilico, quindi il trasferimento del protone è favorito:
Nella classica procedura di laboratorio, il trigliceride trimiristina è ottenuto per estrazione dalla noce moscata con etere dietilico.[3] La saponificazione dell'acido miristico si verifica con NaOH in acqua. L'acido stesso può essere ottenuto aggiungendo HCl diluito all'estratto.[4]
Idrolisi a vapore[modifica | modifica wikitesto]
I trigliceridi possono anche essere saponificati con un processo a due stadi che parte dall'idrolisi a vapore del triestere. Questo trattamento produce l'acido carbossilico, e non il suo sale, oltre al glicerolo. Successivamente l'acido grasso viene neutralizzato con una base per avere il sapone. Il vantaggio del processo a due stadi consiste nella possibile purificazione degli acidi così ottenuti in modo da migliorare la qualità del prodotto finito. L'idrolisi a vapore procede attraverso una meccanismo simile a quello esposto precedentemente e prevede l'attacco di molecole d'acqua (non di idrossido) sul centro del carbonile. La reazione è più lenta, perché richiede la produzione di vapore.
Applicazioni[modifica | modifica wikitesto]
La conoscenza della saponificazione è attinente a molti campi delle tecnologie e della vita di ogni giorno.
Saponi liquidi e solidi[modifica | modifica wikitesto]
A seconda del tipo di base utilizzata nella loro preparazione, i saponi acquistano proprietà differenti. L'idrossido di sodio (NaOH) genera saponi solidi, mentre se si impiega idrossido di potassio (KOH), si formano saponi liquidi.
Grasso al litio[modifica | modifica wikitesto]
I derivati del 12-idrossistearato e del litio e molti altri acidi carbossilici sono importanti costituenti di grassi lubrificanti. Nello specifico, i carbossilati di litio fungono da addensanti. Anche i “saponi complessi” sono piuttosto comuni, essendo combinazioni di saponi metallici, come saponi di litio e calcio.[5]
Estintori[modifica | modifica wikitesto]
Gli incendi di grassi di cottura e olii (classificati come classe K (USA) o F (Australia / Europa / Asia)) bruciano a temperature maggiori di quelli causati da liquidi infiammabili, rendendo inefficace un normale estintore di classe B. I liquidi infiammabili hanno un punto di fiamma inferiore a 50 °C. L'olio alimentare è un liquido combustibile, in quanto ha un punto di infiammabilità superiore ai 50 gradi. Incendi del genere dovrebbero essere spenti con un estintore chimico. I dispositivi di questo tipo sono progettati per estinguere i grassi e gli oli di cottura attraverso la saponificazione. L'agente estinguente converte rapidamente la sostanza che sta bruciando in un sapone non-combustible. Questo processo è endotermico, cioè assorbe l'energia termica dall'ambiente circostante inibendo ulteriormente il fuoco.
La saponificazione e la conservazione dei beni culturali[modifica | modifica wikitesto]
Nel corso del tempo possono verificarsi fenomeni di saponificazione sui dipinti a olio, causando danni visibili e deformazioni. Il substrato o gli strati di pittura dei quadri a olio contengono spesso metalli pesanti usati come pigmenti: il bianco di piombo, il minio e l'ossido di zinco sono fra i più diffusi. Se tali metalli reagiscono con gli acidi grassi liberi nella matrice oleosa che lega insieme i pigmenti, possono formarsi dei saponi nello strato di vernice che migrano verso la superficie del dipinto.[6]
La saponificazione dei dipinti a olio è stata descritta per la prima volta nel 1997.[7] Si crede sia un fenomeno diffuso, essendo stato osservato in molte opere databili fra il XV e il XX secolo di diversa origine geografica e su vari supporti, come ad esempio tela, carta, legno e rame. L'analisi chimica può rivelare principi di saponificazione negli strati più profondi di un dipinto prima ancora che ne appaiano i segni in superficie, anche in dipinti antichi di secoli.[8]
Le aree saponificate possono deformare la superficie del dipinto attraverso la formazione di grumi visibili o sporgenze che diffondono la luce. Questi grumi di sapone possono interessare solo alcune parti della tela oppure anche l'intera opera. Nel famoso Ritratto di Madame X di John Singer Sargent, per esempio, i coaguli appaiono solo sulle aree più scure e possono essere causati dall'uso di pennellate più grasse in quei punti, da parte dell'artista, per compensare la tendenza all'essiccazione dei pigmenti neri.[9] Il processo può anche formare depositi gessosi bianchi sulla superficie di un dipinto, una deformazione spesso descritta come "fioritura" o "efflorescenza", e può inoltre contribuire ad aumentare la trasparenza di alcuni strati di vernice nel corso del tempo.[10]
Il processo non è ancora pienamente compreso. La saponificazione non si verifica in tutti i quadri a olio contenenti i materiali noti per innescarla. Ancora non si conosce la causa né i fattori che ne determinano il peggioramento, di conseguenza non esiste ancora un modo per arrestare il processo.[11] Allo stato attuale, il ritocco è l'unico metodo di restauro possibile.
Note[modifica | modifica wikitesto]
- ^ K. Schumann, K. Siekmann, Soaps, in: Ullmann's Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim
- ^ John McMurry, Organic Chemistry (2nd Edition).
- ^ Organic Syntheses 1:538 Link
- ^ Organic Syntheses 1:379 Link
- ^ Thorsten Bartels et al. Lubricants and Lubrication, in: Ullmann's Encyclopedia of Industrial Chemistry, 2005, Weinheim. DOI: 10.1002/14356007.a15 423
- ^ Silvia A. Centeno and Dorothy Mahon, The Chemistry of Aging in Oil Paintings: Metal Soaps and Visual Changes. The Metropolitan Museum of Art Bulletin, Summer 2009, pp. 12-19.
- ^ Scoperta nei Paesi Bassi da ricercatori che analizzavano il dipinto Lezione di anatomia del dottor Tulp, di Rembrandt, (1632). Vedi Centeno, p. 14.
- ^ Centeno, p. 16.
- ^ Centeno, pp. 12-13, 15.
- ^ Centeno, pp. 16, 19.
- ^ Centeno, p. 19.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «saponificazione»
Wikizionario contiene il lemma di dizionario «saponificazione» Wikimedia Commons contiene immagini o altri file su saponificazione
Wikimedia Commons contiene immagini o altri file su saponificazione
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) saponification, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.