Acidificazione degli oceani
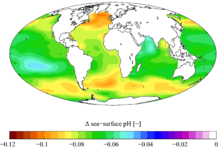
L'acidificazione degli oceani è dovuta alla decrescita del valore del pH oceanico causato dall'assunzione di anidride carbonica di origine antropica dall'atmosfera.[1]
Circa un quarto della CO2 presente nell'atmosfera finisce negli oceani dove, a contatto con l'acqua, viene trasformata in acido carbonico (H2CO3). All'aumentare della CO2 nell'atmosfera, corrisponde anche un innalzamento di quella disciolta nell'acqua marina; per cui l'incremento delle emissioni di CO2 determina effetti devastanti sugli ecosistemi marini.[2] In particolare, secondo il Gruppo intergovernativo sul cambiamento climatico (IPCC), dal 1750 al 2014, una percentuale pari al 30% della CO2 emessa come conseguenza di attività umane (emissioni antropogeniche) è stata assorbita dagli oceani.[2]
È stato stimato che tra il 1751 e il 1994, il pH superficiale delle acque oceaniche si sia abbassato da 8,25 a 8,14,[3] con un corrispondente aumento della concentrazione di ioni H+,[4] pari al 26%.[2]
Il processo di continua acidificazione delle acque oceaniche porta indubbiamente ad effetti sulla catena alimentare[5] e, in particolar modo, può influire sul lisoclino e sulla profondità di compensazione dei carbonati; con conseguente scioglimento dei gusci calcarei delle conchiglie, dei molluschi e del plancton calcareo, costituiti da carbonato di calcio (CaCO3).
Il ciclo del carbonio[modifica | modifica wikitesto]

Il ciclo del carbonio descrive il flusso dell'anidride carbonica tra gli oceani, la biosfera terrestre, la litosfera[6] e l'atmosfera. Le attività antropiche come l'impiego di combustibili fossili, le emissioni in atmosfera e il cambiamento nell'utilizzo della terra, hanno modificato il flusso della CO2 nell'atmosfera. Circa il 45% di questo gas è rimasto nell'atmosfera, mentre la parte rimanente è stata assorbita dagli oceani[7] e dalle piante terrestri.[8]
Il ciclo del carbonio coinvolge sia composti organici sia composti inorganici del carbonio, come la stessa CO2 e i carbonati. I composti inorganici in particolare hanno una influenza significativa per quanto riguarda l'acidificazione delle acque oceaniche causata dalla CO2.[9]
Gli oceani in particolare riescono ad assorbire la CO2 dall'atmosfera e così facendo si acidificano.[10] Quando la CO2 viene disciolta per produrre CO2 acquosa si viene a formare anche acido carbonico che si dissocerà rapidamente producendo così ioni bicarbonato che a sua volta possono dissociarsi in ione carbonato. queste reazioni sono in grado di produrre protoni abbassando così il valore di pH della soluzione.
Nell'acqua di mare, però, la situazione cambia. Questo perché la CO2 nell'acqua di mare non si dissocia completamente in ioni carbonato e quindi il numero di ioni prodotti sarà inferiore. Ciò è dovuto alla capacità di tamponare le variazioni di pH dell'acqua di mare: tale capacità tuttavia diminuisce man mano che viene aggiunta più CO2, raggiungendo velocemente livelli di saturazione molto alti.
Effetti e ripercussioni sull'uomo[modifica | modifica wikitesto]
La storia della Terra ha visto susseguirsi numerosi cicli di migliaia di anni tra un periodo glaciale e l’altro, durante i quali le concentrazioni di CO2 atmosferica hanno continuato ad oscillare tra le 180 e le 290 parti per milione: si tratta di valori assai inferiori a quelli attuali. Inoltre, non esistono prove geologiche a sostegno dell’ipotesi che un netto cambiamento nel sistema dei carbonati oceanici sia già avvenuto in passato. Siamo dunque di fronte ad una situazione nuova ed incerta.[11]

Continuando con questo regime di emissioni, si pensa che nel 2100 gli oceani si abbasseranno ancora di 0,43 unità di pH, con effetti inevitabili sia per l'essere umano che per gli ecosistemi. Gli organismi marini sensibili alle variazioni di pH, infatti, potrebbero riprodursi e prosperare con sempre maggiore difficoltà in futuro, con una netta diminuzione del cibo disponibile nei nostri mercati.[12] Il settore ittico rimarrebbe gravemente colpito e le popolazioni che sfruttano la pesca come fonte primaria di cibo si ritroverebbero in gravi situazioni di carestia.
Effetti e ripercussioni sugli organismi[modifica | modifica wikitesto]
A causa dell’acidificazione degli oceani, la fauna marina viene messa in serio pericolo. L’abbassamento del pH marino crea il fenomeno di sbiancamento dei coralli; il carbonato di calcio che costituisce le conchiglie, i molluschi, i crostacei e perfino il corallo, diminuisce in relazione all’aumento dell’acidità, perdendo così le alghe che vivono sopra la superficie dell’organismo, portandolo alla morte.


Nonostante molti organismi risentano di questa acidificazione sempre maggiore, alcuni organismi fotosintetici ne traggono beneficio. Un caso è rappresentato dalle diatomee; ossia alghe microscopiche appartenenti al fitoplancton. Per questi organismi, l’aumento di CO2 in acqua, aumenta la loro capacità di svolgere i propri processi di fotosintesi. Questi processi possono essere svolti se in presenza di determinate condizioni ambientali.
Prospettive future[modifica | modifica wikitesto]
Secondo i dati attuali, l’IPCC prevede un ulteriore abbassamento del pH dello 0,3-0,4 entro la fine di questo secolo con conseguente aumento fino al 150% dell’acidità e abbassamento della quantità di ione carbonato.[13] I risultati a lungo termine dovuti all’impatto dell’acidificazione degli oceani necessitano di ulteriori studi, ma certamente continueranno ad aumentare gli effetti negativi sugli organismi viventi. Il problema è il fatto che il processo di acidificazione oceanica sta avvenendo troppo velocemente non permettendo l’adattamento delle specie presenti.[14] Numerose sono le proposte per ridurre l’acidificazione degli oceani ancora in via di sperimentazione che inoltre saranno molto costose. Sicuramente i processi naturali riusciranno a ricreare le condizioni di equilibrio ma questo avverrà in tempi lunghissimi dell’ordine delle centinaia di migliaia di anni.
Note[modifica | modifica wikitesto]
- ^ K. Caldeira, Wickett, M.E., Anthropogenic carbon and ocean pH (PDF), in Nature, vol. 425, n. 6956, 2003, pp. 365–365, Bibcode:2001AGUFMOS11C0385C, DOI:10.1038/425365a, PMID 14508477.
- ^ a b c (EN) IPCC, 2014: Climate Change 2014: Synthesis Report. Contribution of Working Groups I, II and III to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change - Core Writing Team, R.K. Pachauri and L.A. Meyer. IPCC (Ginevra).
- ^ M.Z. Jacobson, Studying ocean acidification with conservative, stable numerical schemes for nonequilibrium air-ocean exchange and ocean equilibrium chemistry, in Journal of Geophysical Research – Atmospheres, vol. 110, 2005, pp. D07302, Bibcode:2005JGRD..11007302J, DOI:10.1029/2004JD005220.
- ^ Hall-Spencer JM, Rodolfo-Metalpa R, Martin S, et al., Volcanic carbon dioxide vents show ecosystem effects of ocean acidification, in Nature, vol. 454, n. 7200, luglio 2008, pp. 96–9, Bibcode:2008Natur.454...96H, DOI:10.1038/nature07051, PMID 18536730.
- ^ Cornelia Dean, Rising Acidity Is Threatening Food Web of Oceans. New York Times, January 30, 2009
- ^ carbon cycle, su Encyclopædia Britannica Online. URL consultato l'11 febbraio 2010.
- ^ J.A. Raven, Falkowski, P.G., Oceanic sinks for atmospheric CO2, in Plant, Cell & Environment, vol. 22, n. 6, 1999, pp. 741–755, DOI:10.1046/j.1365-3040.1999.00419.x.
- ^ W. Cramer et al., Global response of terrestrial ecosystem structure and function to CO2 and climate change: results from six dynamic global vegetation models, in Global Change Biology, vol. 7, n. 4, 2001, pp. 357–373, DOI:10.1046/j.1365-2486.2001.00383.x.
- ^ Lee R. Kump, James F. Kasting e Robert G. Crane, The Earth System, 2nd, Upper Saddle River: Prentice Hall, 2003, pp. 162–164, ISBN 0-613-91814-2.
- ^ (EN) Ocean Acidification | Learn Science at Scitable, su www.nature.com. URL consultato l'8 aprile 2022.
- ^ Scott C. Doney, Victoria J. Fabry e Richard A. Feely, Ocean Acidification: The Other CO2 Problem, in Annual Review of Marine Science, vol. 1, n. 1, 1º gennaio 2009, pp. 169–192, DOI:10.1146/annurev.marine.010908.163834. URL consultato il 9 aprile 2022.
- ^ Agathe Euzen, Laurence Eymard e Françoise Gaill, Introduction générale, CNRS Éditions, pp. 18–19. URL consultato il 9 aprile 2022.
- ^ Copia archiviata, su 1ocean.org. URL consultato il 14 aprile 2022 (archiviato dall'url originale il 27 gennaio 2022).
- ^ https://www.nasa.gov/topics/earth/features/climate_acidocean.html
Bibliografia[modifica | modifica wikitesto]
- Ridgwell, A. & Zeebe, R.E.,: The role of the global carbonate cycle in the regulation and evolution of the Earth system. Earth and Planetary Science Letters, 234: p. 299– 315. 2005.
- Sarmiento, J.L. & Gruber, N.,: Ocean Biogeochemical Dynamics. Princeton University Press. 2006.
- Butler, J. N., 1991: Carbon Dioxide Equilibria and Their Applications. CRC Press, 1982 ISBN 978-0-87371-624-6
- Stephen Barker e Andy Ridgwell © 2012 Educazione alla natura, S. & Ridgwell, A. (2012) Acidificazione degli oceani. Conoscenza dell'educazione alla natura 3( 10 ) :21
- Eds. Euzen, A., Gaill, F., Lacroix, D., Cury, P. (2017). The Ocean revealed. CNRS Editions 66-67.
- The Royal Society (2005). Ocean acidification due to increasing atmospheric carbon dioxide
- Doney, S.C., et al. (2009). Ocean Acidification: The Other CO2 Problem. Annual Review of Marine Science 1:169-192.
- Bachelor Thesis World Bachelor in Business Program: “How Private Vessels Can Aid Marine Scientific Research”, April 2020
- Climate change seeps into the sea Rosemary Sullivant/Global Climate Change NASA
- Clark, TD, Raby, GD, Roche, DG et al. L'acidificazione degli oceani non pregiudica il comportamento dei pesci della barriera corallina. Natura 577, 370–375 (2020)
Voci correlate[modifica | modifica wikitesto]
- Profondità di compensazione dei carbonati
- Lisoclino
- Cambiamento climatico
- Buco nell'ozono
- Deossigenazione degli oceani
- Effetti del cambiamento climatico sugli oceani
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Acidificazione degli oceani
Wikimedia Commons contiene immagini o altri file su Acidificazione degli oceani
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) John P. Rafferty, ocean acidification, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | LCCN (EN) sh2010010083 |
|---|