Fotosensibilizzante

I fotosensibilizzanti sono molecole in grado di alterare il corso di una reazione fotochimica grazie alla possibilità di assorbire radiazione luminosa. Di solito queste specie sono anche catalizzatori.[1] Sono stati studiati diversi meccanismi di funzionamento, tra questi spiccano quelli che includono un trasferimento elettronico o viceversa un trasferimento protonico. Al termine di questo processo, il fotosensibilizzante ritorna al suo stato fondamentale, dove ritorna chimicamente inalterato rispetto alla situazione di partenza.[2][3][4] Un ramo della chimica che utilizza frequentemente i fotosensibilizzatori è la chimica dei polimeri, che utilizza i fotosensibilizzatori in reazioni come la fotopolimerizzazione, la fotoreticolazione e la fotodegradazione.[5] I fotosensibilizzatori sono anche usati per generare stati elettronici eccitati duraturi nel tempo in molecole organiche con usi nella fotocatalisi, nell'upconversion dei fotoni e nella terapia fotodinamica. In generale, i fotosensibilizzatori assorbono la radiazione elettromagnetica costituita da radiazione infrarossa, radiazione luminosa visibile e radiazione ultravioletta e trasferiscono l'energia assorbita alle molecole vicine. Questo assorbimento della luce è reso possibile da grandi sistemi π delocalizzati, che abbassano l'energia degli orbitali HOMO e LUMO per promuovere la fotoeccitazione. Mentre molti fotosensibilizzatori sono composti organici o organometallici, ci sono anche esempi di punti quantici di semiconduttori usati come fotosensibilizzatori.[6]
Teoria[modifica | modifica wikitesto]

Considerazioni meccanicistiche[modifica | modifica wikitesto]
I fotosensibilizzatori assorbono la luce (hν) e trasferiscono l'energia dalla luce incidente ad un'altra molecola vicina direttamente oppure mediante una reazione chimica. Dopo aver assorbito fotoni provenienti dalla radiazione luminosa incidente, i fotosensibilizzatori passano in uno stato di singoletto eccitato. Il singolo elettrone nello stato di singoletto eccitato inverte il suo spin e passa in uno stato di tripletto attraverso incrocio intersistema. Gli stati di tripletto in genere hanno un'emivita maggiore rispetto ai singoletti eccitati. Questo aumenta la probabilità di prendere parte a reazioni con altre molecole vicine. I fotosensibilizzatori sono caratterizzati da diversi livelli di efficienza per la realizzazione di intersystem crossing a diverse lunghezze d'onda in base alla struttura elettronica interna della molecola.[2][7]
Parametri[modifica | modifica wikitesto]
Affinché una molecola sia considerata un fotosensibilizzante:
- Il fotosensibilizzante deve impartire un cambiamento fisico-chimico su un substrato dopo aver assorbito la luce incidente.
- Dopo aver impartito un cambiamento chimico, il fotosensibilizzante ritorna alla sua forma chimica originale.
È importante differenziare i fotosensibilizzatori da altre sostanze e meccanismi che sono caratterizzati da interazioni fotochimiche, come i fotoiniziatori, fotocatalizzatori, fotoacidi e la fotopolimerizzazione. I fotosensibilizzatori utilizzano la luce per attuare un cambiamento chimico in un substrato; dopo il cambiamento chimico, il fotosensibilizzante ritorna al suo stato iniziale, rimanendo chimicamente inalterato nel processo. I fotoiniziatori assorbono radiazione luminosa per diventare una specie reattiva, comunemente un radicale o uno ione e poi va a reagire con un'altra specie chimica. Questi fotoiniziatori sono spesso irreversibilmente modificati dopo aver preso parte alla reazione. I fotocatalizzatori accelerano le reazioni chimiche che richiedono l'assorbimento di fotoni. Mentre alcuni fotosensibilizzatori possono agire come fotocatalizzatori, non tutti i fotocatalizzatori possono agire come fotosensibilizzatori. I fotoacidi (o fotobasi) sono molecole che diventano più acide (o basiche) in seguito all'assorbimento della luce. I fotoacidi aumentano la propria acidità quando assorbono la luce e ritornano alla loro forma originale, durante un rilassamento di tipo termico. I generatori di fotoacidi, invece, subiscono un cambiamento irreversibile per diventare una specie acida dopo l'assorbimento della luce. La fotopolimerizzazione può avvenire in due modi: può avvenire direttamente se i monomeri assorbono la luce incidente e iniziano a polimerizzare, oppure può avvenire attraverso un processo che è mediato da un fotosensibilizzante, in cui questo assorbe la luce e trasferisce, poi, energia alle specie monomeriche.[8][9]
Storia[modifica | modifica wikitesto]
I fotosensibilizzatori esistono in natura per moltissimo tempo; basti pensare alla clorofilla o ad altre molecole all'interno del metabolismo delle piante. Gli studi sui fotosensibilizzatori sono iniziati, però, nel 1900, quando gli scienziati hanno osservato la fotosensibilizzazione nei substrati biologici e nel trattamento del cancro. Gli studi meccanicistici relativi ai fotosensibilizzatori sono iniziati con l'analisi dei prodotti delle reazioni chimiche in cui i fotosensibilizzatori fotoossidavano l'ossigeno molecolare per dare specie di perossidi. I risultati sono stati elaborati in termine di efficienze quantiche e di resa di fluorescenza, considerando diverse lunghezze d'onda della luce e confrontando i risultati dei calcoli con la resa delle specie reattive dell'ossigeno. Tuttavia, solo negli anni '60 il meccanismo di donazione degli elettroni è stato confermato attraverso vari metodi spettroscopici, tra cui gli studi sull'intermedio di reazione e sulla luminescenza.[8][10][11]
Il termine fotosensibilizzante non compare nella letteratura scientifica fino agli anni '60. Fino ad allora, gli scienziati si erano riferiti ai fotosensibilizzatori come sensibilizzanti utilizzati nei processi di fotoossidazione o fotoossigenazione. Gli studi condotti durante questo periodo di tempo hanno utilizzato fotosensibilizzatori organici, costituiti da molecole di idrocarburi aromatici, che avevano come prospettiva un'applicazione nel facilitare le reazioni di sintesi organica. in seguito, negli anni '70 e '80, i fotosensibilizzatori è stata posta maggiore attenzione all'interno della comunità scientifica al loro ruolo all'interno dei processi biologici e dei processi enzimatici.[12][13] Attualmente, i fotosensibilizzatori sono studiati per i loro contributi in campi come l'energetica, la catalisi fotoredox nella chimica sintetica e il trattamento del cancro.[11][14]

Tipi di processi di fotosensibilizzazione[modifica | modifica wikitesto]
Esistono due percorsi principali per le reazioni fotosensibilizzate.[2]
Tipo I[modifica | modifica wikitesto]
Nelle reazioni fotosensibilizzate di tipo I, il fotosensibilizzante viene eccitato da una sorgente luminosa e così produce uno stato di tripletto. Il fotosensibilizzante allo stato eccitato reagisce quindi con una molecola di substrato per formare un prodotto e riformare il fotosensibilizzante. Le reazioni di tipo I provocano l'estinzione del fotosensibilizzante alla fine del processo, senza bisogno dell'intervento di ossigeno molecolare.[2][15]

Tipo II[modifica | modifica wikitesto]
Nelle reazioni fotosensibilizzate di tipo II, il fotosensibilizzante viene eccitato da una sorgente luminosa per dare uno stato di tripletto. Il fotosensibilizzatore eccitato reagisce quindi con una molecola di ossigeno di tripletto allo stato fondamentale. Questo eccita la molecola di ossigeno che passa in uno stato di singoletto, rendendola una specie reattiva dell'ossigeno. Dopo l'eccitazione, la molecola di ossigeno singoletto reagisce con un substrato per concludere la reazione. Un processo di tipo II coinvolge quindi anche una molecola di ossigeno nell'inattivazione del fotosensibilizzante ed è sempre l'ossigeno a portare il substrato a prodotto.[2][16][17]
Composizione di fotosensibilizzatori[modifica | modifica wikitesto]
I fotosensibilizzatori possono essere inseriti in 3 domini, sulla base della loro struttura molecolare: organometallici, organici e nanomateriali.
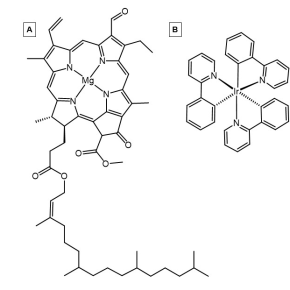
Organometallici[modifica | modifica wikitesto]

I fotosensibilizzatori organometallici contengono un atomo di metallo chelato da uno o più ligandi organici. Le capacità fotosensibilizzanti di queste molecole derivano dalle interazioni elettroniche tra il metallo e i ligandi. I centri metallici più usati per questo tipo di complessi sono iridio, rutenio e rodio. Questi metalli, sono centri metallici comuni per i fotosensibilizzatori a causa dei loro orbitali d quasi pieni o per l'alto numero di elettroni in questi orbitali. Queste situazioni sono utili per promuovere il trasferimento di carica da metallo a ligando a partire da ligandi che accettano elettroni pi. Questa interazione tra il centro metallico e il ligando porta a un ampio continuum di orbitali cosicché sia attraverso l'orbitale molecolare occupato a più alta energia (HOMO) sia l'orbitale molecolare non occupato a più bassa energia (LUMO) è possibile che gli elettroni eccitati cambino la propria molteplicità attraverso incrocio intersistema.[18]
Anche se molti dei composti fotosensibilizzanti organometallici sono prodotti sinteticamente, esistono anche fotosensibilizzatori organometallici presenti in natura e sono definiti composti light-harvesting . Alcuni esempi rilevanti presenti in natura includono la clorofilla A e la clorofilla B.[18][19]
Organici[modifica | modifica wikitesto]
I fotosensibilizzatori appartengono alla classe degli organici se sono molecole prevalentemente a base di carbonio. I primi fotosensibilizzatori studiati erano idrocarburi aromatici che assorbivano la luce in presenza di ossigeno per produrre specie reattive dell'ossigeno.[20] Questi sono costituiti da sistemi altamente coniugati che promuovono la delocalizzazione degli elettroni. A causa della loro elevata coniugazione, questi sistemi hanno un gap minore tra gli orbitali di frontiera, nonché un continuum di orbitali all'interno dell' HOMO e del LUMO. Queste due caratteristiche consentono a questi composti di entrare nel loro stato di tripletto in modo più efficiente, rendendoli migliori fotosensibilizzatori. Alcuni importanti fotosensibilizzatori organici ampiamente studiati includono benzofenoni, blu di metilene e rosa bengala.[21]
Nanomateriali[modifica | modifica wikitesto]
Punti quantici[modifica | modifica wikitesto]
I punti quantici in fase colloidale sono materiali semiconduttori su scala nanometrica caratterizzati da proprietà ottiche ed elettroniche altamente regolabili. I punti quantici seguono lo stesso meccanismo dei fotosensibilizzatori organometallici e di quelli organici, ma le loro proprietà su scala nanometrica consentono un maggiore controllo su determinati aspetti. Alcuni vantaggi dell'uso dei punti quantici come fotosensibilizzatori includono il loro band gap ridotto che consente transizioni efficienti allo stato di tripletto ed è anche regolabile. Inoltre, la loro insolubilità in molti solventi consente un facile recupero a partire da una miscela di reazione sintetica.[17]
Nanotubi[modifica | modifica wikitesto]
I nanotubi sono caratterizzati anche loro proprietà ottiche ed elettroniche regolabili e possiedono dimensioni simili ai punti quantici. In base alla loro grandezza e alla composizione del materiale, è possibile regolare il picco massimo di assorbimento per i nanotubi durante la loro sintesi. Questo controllo ha ispirato la creazione di nanotubi fotosensibilizzanti.[22]
Applicazioni[modifica | modifica wikitesto]
Medico[modifica | modifica wikitesto]
Terapia fotodinamica[modifica | modifica wikitesto]
La terapia fotodinamica utilizza fotosensibilizzatori di tipo II per raccogliere la luce per degradare tumori o masse cancerose. Questo fenomeno fu osservato per la prima volta nel 1907 da Hermann von Tappeiner quando utilizzò l'eosina per trattare i tumori della pelle.[11] Il processo fotodinamico è prevalentemente una tecnica non invasiva in cui i fotosensibilizzatori vengono iniettati all'interno di un paziente, in modo che possano accumularsi sul sito target. Quando il fotosensibilizzante raggiunge il tumore o il cancro, il paziente è irradiato dall'esterno con luce della lunghezza d'onda specifica che promuove il processo. Questa luce si trova preferibilmente nel vicino infrarosso in quanto consente la penetrazione della pelle senza tossicità acuta. Gli elettroni del fotosensibilizzante sono eccitati nello stato di tripletto dalla radiazione luminosa e, dopo l'eccitazione, il fotosensibilizzatore inizia a trasferire energia a un tripletto di ossigeno allo stato fondamentale per generare ossigeno singoletto eccitato. Le risultanti specie di ossigeno eccitato degradano quindi selettivamente il tumore o la massa cancerosa.[16][22][23]
Nel febbraio 2019, alcuni medici hanno annunciato che l'iridio attaccato all'albumina costituisce una molecola fotosensibilizzata che può penetrare nelle cellule tumorali e, in seguito all'irraggiamento con la luce, può distruggere le cellule tumorali.[24][25]

Fonti di energia[modifica | modifica wikitesto]
Celle solari sensibilizzate con colorante[modifica | modifica wikitesto]
Nel 1972, fu scoperto che la clorofilla poteva assorbire la luce solare e trasferire energia a delle celle elettrochimiche.[26] Questa scoperta ha portato all'uso di fotosensibilizzatori in qualità di materiali per la raccolta della luce nelle celle fotovoltaiche, grazie all'uso di coloranti fotosensibilizzanti. Le celle solari sensibilizzate con coloranti utilizzano questi coloranti fotosensibilizzanti per assorbire i fotoni e trasferire elettroni ricchi di energia a materiale semiconduttore posto nelle vicinanze, con lo scopo di generare energia elettrica. Questi coloranti agiscono da droganti sulle superfici dei semiconduttori, consentendo il trasferimento dell'energia luminosa dal fotosensibilizzatore all'energia elettrica all'interno del semiconduttore. Le specie utilizzabili non sono limitate ai coloranti, tuttavia. Teoricamente si potrebbe utilizzare qualsiasi composto fotosensibilizzante, pur con un occhio di riguardo al materiale semiconduttore a cui sono attaccati.[14][15][27][28]
Catalizzatori per la generazione di idrogeno[modifica | modifica wikitesto]
Tramite l'assorbimento della luce, i fotosensibilizzatori possono utilizzare il trasferimento dello stato di tripletto per ridurre piccole molecole, come l'acqua nella generare di idrogeno gassoso. In tempi recenti, questa applicazione è stata osservata con successo su piccola scala di laboratorio.[29][30]
Chimica sintetica[modifica | modifica wikitesto]
Chimica fotoredox[modifica | modifica wikitesto]
All'inizio del 20º secolo, i chimici osservarono che vari idrocarburi aromatici in presenza di ossigeno potevano assorbire la luce specifica della lunghezza d'onda per generare una specie perossido, ovvero il fotosensibilizzatore era in grado di ridurre l'ossigeno.[12] Questa scoperta ha portato i chimici a studiare i fotosensibilizzatori come catalizzatori fotoredox nella catalisi delle reazioni pericicliche e di altre reazioni di riduzione e ossidazione. I fotosensibilizzatori nella sintesi organica consentono la manipolazione delle transizioni elettroniche all'interno delle molecole, rispondendo all'applicazione di radiazione luminosa dall'esterno. Anche per questa applicazione, i fotosensibilizzatori possono essere di varie classi (organici, organometallici o nanomateriali) a seconda delle proprietà fisiche e spettrali richieste per la reazione.[15][21]
Effetti biologici dei fotosensibilizzatori[modifica | modifica wikitesto]
I fotosensibilizzatori che possono venire incorporati dai tessuti biologici esterni possono aumentare la velocità con cui vengono generate specie reattive dell'ossigeno in seguito all'esposizione alla luce UV, tra cui anche la componente UV della luce solare. Alcuni agenti fotosensibilizzanti naturali, come l'erba di San Giovanni, sembrano aumentare l'incidenza di condizioni infiammatorie della pelle negli animali e si è osservato che riducono leggermente l'abbronzatura negli esseri umani.[31][32]
Alcuni esempi di farmaci fotosensibilizzanti sono:
Note[modifica | modifica wikitesto]
- ^ Photosensitization, su IUPAC Gold Book, International Union of Pure and Applied Chemistry.
- ^ a b c d e f g Gómez Alvarez E, Wortham H, Strekowski R, Zetzsch C, Gligorovski S, Atmospheric photosensitized heterogeneous and multiphase reactions: from outdoors to indoors, in Environmental Science & Technology, vol. 46, n. 4, febbraio 2012, pp. 1955–63, Bibcode:2012EnST...46.1955G, DOI:10.1021/es2019675, PMID 22148293.
- ^ a b Zhang Y, Lee TS, Petersen JL, Milsmann C, A Zirconium Photosensitizer with a Long-Lived Excited State: Mechanistic Insight into Photoinduced Single-Electron Transfer, in Journal of the American Chemical Society, vol. 140, n. 18, maggio 2018, pp. 5934–5947, DOI:10.1021/jacs.8b00742, PMID 29671586.
- ^ Photosensitization, in IUPAC Compendium of Chemical Terminology, 2009, DOI:10.1351/goldbook.P04652, ISBN 978-0-9678550-9-7.
- ^ 2nd, ISBN 978-0412608704.
- ^ vol. 351, DOI:10.1126/science.aad4011, PMID 26798010, https://oadoi.org/10.1126/science.aad4011.
- ^ ISBN 978-3-540-40394-4, OCLC 56798940.
- ^ a b ISBN 0-8053-9353-6, OCLC 4417476.
- ^ 3rd, ISBN 0-13-065056-0, OCLC 51096012.
- ^ vol. 86, DOI:10.1021/cr00072a005, ISSN 0009-2665, https://oadoi.org/10.1021/cr00072a005.
- ^ a b c vol. 61, DOI:10.1111/j.1445-2197.1991.tb00230.x, PMID 2025186, https://oadoi.org/10.1111/j.1445-2197.1991.tb00230.x.
- ^ a b (EN) Gollnick K, Type II Photooxygenation Reactions in Solution, in Advances in Photochemistry, John Wiley & Sons, Ltd, 1968, pp. 1–122, DOI:10.1002/9780470133361.ch1, ISBN 978-0-470-13336-1.
- ^ (EN) Julliard M, Chanon M, Photoelectron-transfer catalysis: its connections with thermal and electrochemical analogs, in Chemical Reviews, vol. 83, 1º agosto 1983, pp. 425–506, DOI:10.1021/cr00056a003, ISSN 0009-2665.
- ^ a b (EN) O'Regan B, Grätzel M, A low-cost, high-efficiency solar cell based on dye-sensitized colloidal TiO 2 films, in Nature, vol. 353, ottobre 1991, pp. 737–740, DOI:10.1038/353737a0, ISSN 1476-4687.
- ^ a b c vol. 6, DOI:10.1021/am501192f, PMID 24758570, https://oadoi.org/10.1021/am501192f.
- ^ a b Karimi M, Sahandi Zangabad P, Baghaee-Ravari S, Ghazadeh M, Mirshekari H, Hamblin MR, Smart Nanostructures for Cargo Delivery: Uncaging and Activating by Light, in Journal of the American Chemical Society, vol. 139, n. 13, aprile 2017, pp. 4584–4610, DOI:10.1021/jacs.6b08313, PMID 28192672.
- ^ a b Jiang Y, Weiss EA, Colloidal Quantum Dots as Photocatalysts for Triplet Excited State Reactions of Organic Molecules, in Journal of the American Chemical Society, vol. 142, n. 36, settembre 2020, pp. 15219–15229, DOI:10.1021/jacs.0c07421, PMID 32810396.
- ^ a b vol. 140, DOI:10.1021/jacs.8b00742, PMID 29671586, https://oadoi.org/10.1021/jacs.8b00742.
- ^ Prier CK, Rankic DA, MacMillan DW, Visible light photoredox catalysis with transition metal complexes: applications in organic synthesis, in Chemical Reviews, vol. 113, n. 7, luglio 2013, pp. 5322–63, DOI:10.1021/cr300503r, PMID 23509883.
- ^ Bowen EJ, The Photochemistry of Aromatic Hydrocarbon Solutions, in Advances in Photochemistry, 1963, pp. 23–42, DOI:10.1002/9780470133316.ch2, ISBN 978-0-470-13331-6.
- ^ a b Romero NA, Nicewicz DA, Organic Photoredox Catalysis, in Chemical Reviews, vol. 116, n. 17, settembre 2016, pp. 10075–166, DOI:10.1021/acs.chemrev.6b00057, PMID 27285582.
- ^ a b Jang B, Park JY, Tung CH, Kim IH, Choi Y, Gold nanorod-photosensitizer complex for near-infrared fluorescence imaging and photodynamic/photothermal therapy in vivo, in ACS Nano, vol. 5, n. 2, febbraio 2011, pp. 1086–94, DOI:10.1021/nn102722z, PMID 21244012.
- ^ vol. 58, PMID 9721863.
- ^ University of Warwick, https://www.eurekalert.org/pub_releases/2019-02/uow-ssl013119.php.
- ^ Zhang P, Huang H, Banerjee S, Clarkson GJ, Ge C, Imberti C, Sadler PJ, Nucleus-Targeted Organoiridium-Albumin Conjugate for Photodynamic Cancer Therapy, in Angewandte Chemie, vol. 58, febbraio 2019, pp. 2350–2354, DOI:10.1002/anie.201813002, PMID 30552796.
- ^ (EN) vol. 16, DOI:10.1111/j.1751-1097.1972.tb06297.x, ISSN 1751-1097, https://oadoi.org/10.1111/j.1751-1097.1972.tb06297.x.
- ^ vol. 38, DOI:10.1016/j.tibtech.2020.04.004, PMID 32448469, https://oadoi.org/10.1016/j.tibtech.2020.04.004.
- ^ vol. 22, DOI:10.1021/cm9036988, ISSN 0897-4756, https://oadoi.org/10.1021/cm9036988.
- ^ McCullough BJ, Neyhouse BJ, Schrage BR, Reed DT, Osinski AJ, Ziegler CJ, White TA, Visible-Light-Driven Photosystems Using Heteroleptic Cu(I) Photosensitizers and Rh(III) Catalysts To Produce H2, in Inorganic Chemistry, vol. 57, n. 5, marzo 2018, pp. 2865–2875, DOI:10.1021/acs.inorgchem.7b03273, PMID 29446925.
- ^ Zhou Q, Shi G, Conducting Polymer-Based Catalysts, in Journal of the American Chemical Society, vol. 138, n. 9, marzo 2016, pp. 2868–76, DOI:10.1021/jacs.5b12474, PMID 26863332.
- ^ Kumper H. [Hypericum poisoning in sheep]. Tierarztl Prax 1989;17:257-261.
- ^ a b Brockmoller J, et al. Hypericin and pseudohypericin: Pharmacokinetics and effects on photosensitivity in humans. Pharmacopsychiatry 1997;30(Suppl 2): 94-101.
- ^ (EN) Mechanisms of DNA damage by photoexcited 9-methyl-β-carbolines, in Organic & Biomolecular Chemistry, vol. 11, n. 32, 24 luglio 2013, pp. 5300–5309, DOI:10.1039/C3OB40344K, ISSN 1477-0539, PMID 23842892.
- ^ a b c (EN) Wisconsin Department of Health Services, https://www.dhs.wisconsin.gov/radiation/medications.htm. URL consultato il 1º novembre 2022.
Voci correlate[modifica | modifica wikitesto]
- Fotosintesi artificiale
- Fotosensibilità
- Terapia fotodinamica
- Fotocatalisi
- Cella solare sensibilizzata con colorante
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su fotosensibilizzante
Wikimedia Commons contiene immagini o altri file su fotosensibilizzante
| Controllo di autorità | GND (DE) 4386873-3 · NDL (EN, JA) 00576416 |
|---|