Coordinata di reazione
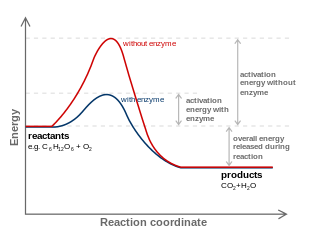
In chimica, una coordinata di reazione[1] è una coordinata monodimensionale che rappresenta l'evoluzione di un processo chimico lungo un dato "cammino di reazione". Solitamente è un parametro geometrico che varia durante la trasformazione di una o più entità che prendono parte a una data reazione chimica.
Il concetto[modifica | modifica wikitesto]
Queste coordinate possono talvolta rappresentare un sistema di coordinate reali (come la lunghezza di legame, l'angolo di legame...), sebbene, specialmente per reazioni più complesse, ciò può essere difficoltoso (e vengono utilizzati parametri non geometrici, ad esempio l'ordine di legame).
Le coordinate di reazione sono spesso riportate in rappresentazione grafica contro l'energia libera per dimostrare schematicamente il profilo dell'energia potenziale (una intersezione di una superficie di energia potenziale) associata alla reazione.
Nel formalismo della teoria dello stato di transizione la coordinata di reazione è quella coordinata facente parte di un insieme di coordinate curvilinee ottenute da quelle convenzionali per i reagenti che, per ogni stadio della reazione, conduce dalla configurazione dei reagenti a quella dei prodotti passando attraverso lo stato di transizione. La coordinata di reazione viene tipicamente scelta per seguire il percorso lungo il gradiente di energia potenziale dai reagenti ai prodotti.
Per esempio, nella dissociazione omolitica dell'idrogeno molecolare, un opportuno sistema di coordinate da scegliere sarebbe la coordinata corrispondente alla lunghezza di legame.
Esempi di coordinate di reazione[modifica | modifica wikitesto]
Possono essere scelte diverse grandezze come coordinate di reazione. Alcune di queste sono:
- il grado di avanzamento della reazione
- il quoziente di reazione
- la conversione di un dato reagente in un dato istante
- il tempo trascorso dal momento in cui ha inizio la reazione.
Note[modifica | modifica wikitesto]
- ^ (EN) Definizione IUPAC Archiviato il 5 dicembre 2008 in Internet Archive.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su coordinata di reazione
Wikimedia Commons contiene immagini o altri file su coordinata di reazione