Alcol polivinilico
| Alcol polivinilico | |
|---|---|
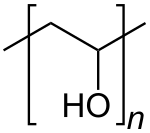 | |
| Nome IUPAC | |
| Polivinil alcol | |
| Abbreviazioni | |
| PVOH PVA | |
| Nomi alternativi | |
| Poliviolo Vinolo Alkotex Covol Gelvatol Lemol | |
| Caratteristiche generali | |
| Formula bruta o molecolare | (C2H4O)n |
| Aspetto | solido incolore, tendente al bianco |
| Numero CAS | |
| Numero EINECS | 618-340-9 |
| DrugBank | DB11060 |
| Proprietà chimico-fisiche | |
| Densità (g/l, in c.s.) | 1,19 - 1,31 |
| Temperatura di fusione | 230 °C (503,15 K) decomposizione |
| Indicazioni di sicurezza | |
| Punto di fiamma | 79,44 °C (352,59 K) |
| Frasi H | --- |
| Consigli P | ---[1] |
L'alcol polivinilico (PVA) è un composto chimico ottenuto per idrolisi, di norma alcalina, degli esteri polivinilici.
Caratteristiche[modifica | modifica wikitesto]
Solubile in acqua e insolubile nei solventi organici, non possiede permeabilità ai gas.
Data la natura del composto, è utilizzato in medicina per drenaggi e tubi, in contattologia quale composto di lubrificanti per lenti a contatto, nell'industria tessile per l'incollaggio di fibre naturali.
Applicato in soluzione acquosa sulla superficie di uno stampo per produzione a freddo di manufatti in vetroresina è un ottimo agente antiadesivo (distaccante).
Usi[modifica | modifica wikitesto]
Le principali applicazioni in termini di quantitativi nel mercato europeo sono:
- Polivinil acetali: vengono preparati facendo reagire aldeidi con alcol polivinilico. Il polivinilbutirrale (PVB) e il polivinil formale (PVF) sono esempi di questa famiglia di polimeri. Sono preparati da polivinil alcol per reazione con aldeide butirrica e formaldeide, rispettivamente.
- Emulsioni. Il PVA viene utilizzato come colloide protettore nella polimerizzazione in emulsione per ottenere dispersioni di polivinilacetato.
- Carta. Il PVA viene usato nelle produzione di diversi tipi di carte (p. es. patinata, release, inkjet). Grazie ai suoi gruppi ossidrile (-OH), che instaurano ponti idrogeno con gruppi analoghi presenti sulle fibre, massimizza l'effetto dato dagli imbiancanti ottici (OBA optical brightness adjuster), fissandoli nella corretta posizione sterica. È altresì utilizzato come coadiuvante barrierante.
Altre applicazioni del PVA:
- Tessile. Il PVA in soluzione viene usato negli appretti.
- Adesivi. Il PVA viene usato come modificatore reologico, addensante in diversi tipi di colle
- Film idrosolubile. Il PVA, insieme a plastificanti ed opportuni additivi, viene granulato e poi estruso per ottenere film idrosolubile utilizzabile per svariate applicazioni (sacchetti per lavanderia, sacchetti per additivi per cementi, sacchetti per detergenti, film per ricamo, pesca(carpfishing), ecc.)
- Barriera. Grazie alla sua elevata impermeabilità ai gas e a qualsiasi solvente diverso dall'acqua, il PVA trova applicazione come coating barrierante su carta o nei film plastici per imballaggio (comprese bottiglie in PET) e come strato barrierante in strutture multilayer (p.es. pavimentazioni in PVC, guanti protettivi)
- Distaccante. Il PVA viene usato come release agent nel processo di formatura di certi materiali ai quali non si appiccica (p.es. epossidiche, vetroresina, ecc.)
- Stampa a iniezione
- Stampa 3D. Fili a base PVA vengono usati nella stampa 3D come supporto idrosolubile per diversi materiali (PLA, PVB, PA, TPU, PETG)
- Farmacologico: presente in alcuni farmaci (compresse)
Il PVA è usato come materia prima nella produzione delle Fibre di PVA[2][3] che, a seconda del processo produttivo utilizzato, possono essere sia solubili che insolubili in acqua.
Grazie alle proprietà elastiche, di stabilità dimensionale, resistenza chimica e affinità con diversi tipi di gomme, le fibre di PVA trovano applicazione:
- come rinforzo nella produzione di tubi (per uso automotive o industriale), nastri trasportatori, pneumatici.
- come rinforzo di cementi e calcestruzzi.
- come rinforzo delle plastiche
- nella produzione di carte speciali
- produzione Non-Wovens
Note[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Alcool polivinilico
Wikimedia Commons contiene immagini o altri file su Alcool polivinilico
Collegamenti esterni[modifica | modifica wikitesto]
- PVA applications KURARAY POVAL, su kuraray-poval.com.
- KURARAY POVAL datasheet (PDF), su kuraray.eu. URL consultato il 26 novembre 2014 (archiviato dall'url originale il 5 aprile 2015).
| Controllo di autorità | J9U (EN, HE) 987007530173305171 · NDL (EN, JA) 00569146 |
|---|