Utente:Bargyman/Sfintere urinario artificiale
Lo sfintere urinario artificiale (SUA) è un dispositivo impiantato per trattare l'incontinenza urinaria da moderata a grave, più comunemente negli uomini. Il SUA è progettato per integrare la funzione dello sfintere urinario naturale che limita il flusso di urina fuori dalla vescica.
Descrizione[modifica | modifica wikitesto]
Esistono due tipi di sfinteri urinari artificiali:
- Lo sfintere urinario artificiale con un serbatoio a palloncino (sfintere tri-componente): cuffia, pompa e palloncino. La cuffia è posizionata attorno all'uretra; la pompa viene inserita nello scroto e il serbatoio a palloncino viene impiantato nello spazio retropubico - tra la vescica e la vena iliaca. La pressione nel circuito idraulico è generata dal serbatoio a palloncino elastico e dalla pressione retropubica.Errore nelle note: L'apertura dell'etichetta
<ref>non è corretta o ha un nome errato.[1] - Lo sfintere urinario artificiale con una molla (sfintere bi-componente): cuffia e unità pompa.[2][3] La cuffia viene posizionata attorno all'uretra e l'unità pompa viene inserita nello scroto. La pressione nel circuito idraulico è generata dalla molla dell'unità pompa. La pressione nello spazio retropubico non ha alcuna influenza per questo tipo di sfintere.
Il principio comune tra le tipologie attualmente disponibili è un meccanismo di costrizione meccanica: un bracciale (cuffia) gonfiabile riempito con soluzione salina sterile e posizionato intorno all'uretra che mantiene chiuso il lume uretrale; ciò è dovuto alla pressione prodotta all'interno del dispositivo e ad un meccanismo di controllo a pompa accessibile dall'esterno posto tra due strati di pelle dello scroto (tasca sub-dartos) che consente all'utente di rilasciare manualmente la costrizione per consentire la minzione.
Storia[modifica | modifica wikitesto]

Frederic Foley fu il primo a descrivere uno sfintere urinario artificiale indossato esternamente per trattare l'incontinenza urinaria, pubblicato nel 1947.[4] Nel 1972, F. Brantley Scott e colleghi del Baylor College of Medicine progettarono il primo precursore dello sfintere urinario artificiale contemporaneo.[5][6] Il primo modello di SUA sul mercato è stato l'AMS 800 (Boston Scientific, Marlborough, MA), sviluppato 50 anni fa.[7][8] È un dispositivo tri-componente con un bracciale (cuffia) posizionato intorno all'uretra, una pompa inserita nello scroto e un serbatoio che genera di pressione posizionato nella pelvi, che viene fornito come kit da preparare e riempire prima dell'impianto.[9]
Un altro modello di SUA è lo ZSI 375 (Zephyr Surgical Implants, Ginevra, Svizzera), introdotto nel 2008.[10] È un dispositivo monoblocco in due parti con un bracciale (cuffia) e un'unità pompa con una molla integrata; viene fornito in un unico pezzo, pre-connesso e pre-riempito.[11] Lo ZSI 375 non prevede alcun componente addominale, che insieme alla sua configurazione pronta all'impianto riduce i tempi operatori.[12] Inoltre, poiché non esiste una componente addominale, non sono necessari interventi chirurgici nello spazio retroperitoneale. Precedenti interventi chirurgici, quali la prostatectomia radicale, possono portare a cicatrici e fibrosi post-operatorie nello spazio retroperitoneale. Pertanto, non dovendo procedere con la dissezione dei tessuti retroperitoneali, si evitano i rischi di complicanze chirurgiche.[13][14] Un ulteriore vantaggio del modello ZSI 375 è la possibilità di aumentare o diminuire la pressione all'interno del dispositivo dopo l'impianto per raggiungere il livello di continenza desiderato e la soddisfazione del paziente. Queste regolazioni sono particolarmente utili nel controllare la continenza in caso di atrofia uretrale post-impianto o di ritenzione urinaria (scarso flusso di urina).[15][16] La regolazione della pressione può essere eseguita in regime ambulatoriale aggiungendo o rimuovendo soluzione salina sterile tramite una siringa attraverso lo scroto. Al 2019 sono stati impiantati oltre 4.500 sfinteri urinari artificiali ZSI 375, in tutto il mondo.
In entrambi i modelli, la soluzione salina sterile all'interno del sistema viene utilizzata per generare pressione e comprimere l'uretra (per evitare perdite di urina). Il bracciale (cuffia) uretrale viene sgonfiato manualmente premendo la pompa di controllo, posizionata nello scroto, consentendo al paziente di svuotare la vescica. La cuffia uretrale si rigonfia quindi automaticamente per riempirsi ed impedire nuovamente la fuoriuscita di urina.[1][17]
L'elenco include i modelli di SUA disponibili nel 2020:
| Prodotto | Azienda | Paese d'origine | Introdotto nel | Design | Preconnesso e preriempito | Pressione erogata | Pressione regolabile |
|---|---|---|---|---|---|---|---|
| AMS 800 | Boston Scientific (precedentemente American Medical Systems) | Stati Uniti d'America | 1988 | 3 componenti: cuffia, pompa, serbatoio a palloncino | No | Serbatoio flessibile inserito nel pavimento pelvico | No |
| ZSI 375 | Zephyr Surgical Implants | Svizzera | 2008 | 2 componenti: cuffia, unità pompa | sì | Molla in acciaio inossidabile all'interno dell'unità pompa inserita nello scroto | sì |
Uso medico[modifica | modifica wikitesto]

La deficienza intrinseca dello sfintere che porta all'incontinenza da stress è l'indicazione più comune per l'impianto di SUA.[8] L'Associazione Europea di Urologia raccomanda l'impianto di SUA per l'incontinenza da stress, da moderata a grave, negli uomini.[18] Inoltre, nonostante le nuove opzioni di trattamento (bendarelle, iniezioni di volumizzanti uretrali, terapia con cellule staminali), il SUA è considerato la gestione chirurgica standard, sia per l'incontinenza da stress negli uomini, sia per l'incontinenza urinaria sviluppata quale complicanza della chirurgia, come prostatectomia, cistectomia e TURP.[7][3][2]
Esistono diversi casi clinici pubblicati in letteratura sull'impianto di SUA nei bambini per incontinenza secondaria, derivante da una lesione uretrale traumatica.[19][20]
I dati sull'utilizzo di SUA nelle donne sono limitati, inoltre non tutti i prodotti disponibili sul mercato sono stati concepiti per l'utilizzo nelle donne.[21][22] L'Associazione Europea di Urologia fornisce raccomandazioni limitate sull'utilizzo del SUA nelle donne, affermando che sebbene il trattamento sia possibile, il rischio di complicanze è elevato.[18] Tuttavia, il SUA è stato utilizzato come ultima opzione per il trattamento dell'incontinenza urinaria nelle donne, dovuta a cause congenite e secondarie a malattie neurologiche.
Risultati[modifica | modifica wikitesto]
Tassi di successo[modifica | modifica wikitesto]
Sono stati pubblicati numerosi studi sugli esiti di pazienti sottoposti a impianto di sfintere urinario artificiale. Il tasso di successo, generalmente definito come raggiungimento della continenza totale (nessun uso di assorbenti) o della continenza sociale (uso di assorbenti/giorno ≤1) con il dispositivo impiantato, varia in letteratura dal 61% al 100%.[3] Anche il miglioramento della qualità della vita è stato considerato quale successo, anche qualora sia stato necessario più di 1 assorbente/giorno. Il tasso di successo è stato riportato al 78% con un follow-up a 3 anni,[23] e oltre il 72% con follow-up da 5 a 7 anni.[24] In una recente revisione sistematica, il tasso di successo è stato riportato essere del 79% con un periodo di follow-up compreso tra 5 mesi e 16 anni.[25] Uno studio comparativo tra pazienti impiantati con diversi modelli di sfintere urinario artificiale e continenza sociale raggiunta non ha mostrato alcuna differenza tra due gruppi per quanto riguarda i test urodinamici, quali la portata, la pressione uretrale, ecc.[1]
Soddisfazione[modifica | modifica wikitesto]
In diversi studi con un follow-up medio a oltre 6 anni,[26][27] almeno il 73% degli uomini con uno sfintere urinario artificiale impiantato era soddisfatto o molto soddisfatto del dispositivo, mentre il 10-23% riferiva insoddisfazione. Con periodi più brevi di follow-up (2-4 anni) i tassi di soddisfazione hanno raggiunto oltre il 90%.[25][3] In un altro studio con un follow-up medio a oltre 7 anni, il tasso di soddisfazione complessivo ha ottenuto 3,9 su una scala da 0 a 5. Il tasso di soddisfazione nei pazienti, dopo la radioterapia, non sembra essere influenzato sfavorevolmente.[28] Con il modello ZSI 375 si riporta un miglioramento dell'iniziale soddisfazione del livello di continenza, regolando la pressione all'interno dell'impianto.[22]
I sondaggi condotti sui pazienti sottoposti all'intervento hanno rilevato che oltre il 90% raccomanderebbe l'intervento ad un amico o un parente con lo stesso problema e oltre il 90% si sottoporrebbe nuovamente all'impianto.[29][30] In aggiunta a tutto questo, il 14% dei pazienti ha riportato un miglioramento dell'attività sessuale.
La qualità della vita a seguito dell'impianto di SUA ha mostrato di essere significativamente migliorata in numerosi studi, utilizzando diverse scale di valori.[25][6] Inoltre la qualità della vita sembra non essere influenzata negativamente da eventuali reinterventi, a condizione che il dispositivo continui a funzionare dopo la revisione.
Reintervento[modifica | modifica wikitesto]
Nelle più grandi serie di dati disponibili, che valutano 1082 pazienti sottoposti a posizionamento primario di SUA, il tasso di sopravvivenza del dispositivo a 5 anni era del 74%, coerente con gli esiti riportati in letteratura, che variano dal 59% al 79%.[31] In particolare, in tutte le serie di dati, alcuni pazienti hanno dovuto sottoporsi nel corso del tempo ad un ripetuto intervento chirurgico, per incontinenza urinaria ricorrente o infezione del dispositivo. In un'analisi aggregata degli studi disponibili, il tasso di reintervento (per qualsiasi fattore) è stato di circa il 26%.[25] Significativamente, alcuni studi hanno dimostrato che i chirurghi, che eseguono questa procedura con maggior frequenza (chirurghi ad alto volume), hanno risultati migliori rispetto a quelli che la eseguono meno frequentemente.[22] In questa serie di dati, i tassi di reintervento sono infatti diminuiti di circa il 50% quando i chirurghi hanno raggiunto il loro 200° caso, sottolineando la necessità per i potenziali pazienti di cercare chirurghi ad alto volume, per aumentare le loro possibilità di successo.
Complicazioni[modifica | modifica wikitesto]
I possibili rischi derivanti dall'impianto di SUA includono:
- lesioni all'uretra o alla vescica durante il posizionamento di SUA;
- difficoltà di svuotamento della vescica che richiede l'auto-cateterizzazione temporanea;
- persistente incontinenza urinaria da stress;
- infezione del dispositivo che porta alla rimozione;
- incontinenza ricorrente dovuta a guasto del dispositivo o ad atrofia dei tessuti uretrali (nel qual caso un ulteriore intervento chirurgico può rimuovere il vecchio dispositivo e sostituirlo con uno nuovo).
Complessivamente il tasso di complicanze riportato nei maschi è del 37%.[32] Le complicanze postoperatorie più comuni sono:
- guasto meccanico (8-21%)
- erosione uretrale (4-15%)
- infezione (1-14%)
- atrofia uretrale (4-10%)
Altre complicazioni meno frequenti sono ematoma, stenosi uretrale, fistola urinaria.[33] I guasti meccanici e le complicanze non meccaniche possono portare a una revisione chirurgica rispettivamente nell'8-45% e nel 7-17% dei casi. La percentuale complessiva di espianto del dispositivo nei maschi è stata del 16-20%.[34]
Una delle cause di guasto meccanico sono le complicanze legate al serbatoio a palloncino. È stato riportato che il 26% degli uomini, con SUA impiantato, ha richiesto un reintervento al follow-up a 10 anni, al fine di regolare la pressione all'interno del dispositivo.
Follow-up[modifica | modifica wikitesto]
Dopo la dimissione[modifica | modifica wikitesto]
I rapporti sessuali dovrebbero essere evitati per le prime 6 settimane dopo l'impianto, per consentire alla ferita di guarire correttamente.[35] Anche le attività fisiche, che esercitano una pressione diretta sulla ferita, come l'equitazione e il ciclismo, dovrebbero essere evitate per almeno 6 settimane. Ai pazienti potrebbe essere prescritto un supporto scrotale, da indossare per 1 settimana dopo l'intervento.[36]
Avvertenze[modifica | modifica wikitesto]
Per ridurre al minimo il rischio di danni al loro SUA o all'uretra, è fondamentale che i pazienti informino il proprio medico di avere un SUA impiantato, prima di qualsiasi posizionamento di catetere urinario, cistoscopia o qualsiasi altro intervento medico sul tratto urinario.[37] La disattivazione del dispositivo durante la notte può essere raccomandata in particolare ai quei pazienti, che riportano di essere asciutti di notte, per ridurre al minimo i rischi di atrofia uretrale.[38][35]
Galleria di immagini[modifica | modifica wikitesto]
-
TAC (ricostruzione coronale), che mostra un AMS 800 in una donna
-
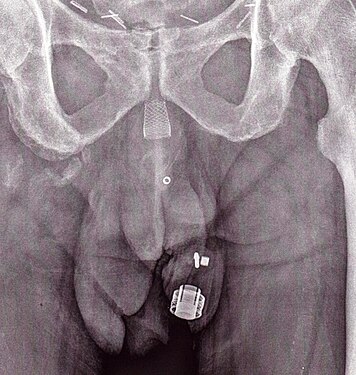
Un'immagine radiologica dello ZSI 375 impiantato. Il dispositivo è disattivato (la molla è compressa sotto la parte superiore del cilindro). Il paziente è incontinente.
-
Un'immagine radiologica dello ZSI 375 impiantato. Il dispositivo è attivato (la molla è decompressa nella parte superiore del cilindro). Il paziente è continente.
-
Una GIF animata, che mostra come il bracciale periuretrale dell'AUS restringe l'uretra
Guarda anche[modifica | modifica wikitesto]
- Incontinenza urinaria
- Incontinenza da stress
- prostatectomia
- Resezione transuretrale della prostata
- Sfintere uretrale interno
- Uretra
Riferimenti[modifica | modifica wikitesto]
- ^ a b Thomas Ripert e Jean Pierrevelcin, Comparative study of urodynamic tests after AMS 800 and ZSI 375 insertion, in Urologia Journal, vol. 85, n. 1, February 2018, pp. 15–18, DOI:10.5301/uj.5000271, PMID 28967063.
- ^ a b Ricarda M. Bauer, Christian Gozzi e Wilhelm Hübner, Contemporary Management of Postprostatectomy Incontinence, in European Urology, vol. 59, n. 6, June 2011, pp. 985–996, DOI:10.1016/j.eururo.2011.03.020, PMID 21458914. URL consultato il 24 January 2020.
- ^ a b c d Billy H Cordon, Nirmish Singla e Ajay K Singla, Artificial urinary sphincters for male stress urinary incontinence: current perspectives, in Medical Devices: Evidence and Research, vol. 2016, n. 9, 4 July 2016, pp. 175–183, DOI:10.2147/MDER.S93637, PMID 27445509.
- ^ Frederic E.B. Foley, An Artificial Sphincter: A New Device and Operation for Control of Enuresis and Urinary Incontinence, in Journal of Urology, vol. 58, n. 4, October 1947, pp. 250–259, DOI:10.1016/S0022-5347(17)69552-1, PMID 20266239. URL consultato il 5 February 2020.
- ^ F. Brantley Scott, William E. Bradley e Gerald W. Timm, Treatment of Urinary Incontinence By An Implantable Prosthetic Urinary Sphincter, in Journal of Urology, vol. 112, n. 1, July 1974, pp. 75–80, DOI:10.1016/S0022-5347(17)59647-0, PMID 4802066. URL consultato il 5 February 2020.
- ^ a b Faysal A. Yafi, Mary K. Powers e Jonathan Zurawin, Contemporary Review of Artificial Urinary Sphincters for Male Stress Urinary Incontinence, in Sexual Medicine Reviews, vol. 4, n. 2, April 2016, pp. 157–166, DOI:10.1016/j.sxmr.2015.11.004, PMID 27872025.
- ^ a b Oscar A. Suarez e Kurt A. McCammon, The Artificial Urinary Sphincter in the Management of Incontinence, in Urology, vol. 92, June 2016, pp. 14–19, DOI:10.1016/j.urology.2016.01.016, PMID 26845050. URL consultato il 24 January 2020.
- ^ a b F. B. Scott, W. E. Bradley e G. W. Timm, Treatment of urinary incontinence by an implantable prosthetic urinary sphincter, in The Journal of Urology, vol. 112, n. 1, 1º luglio 1974, pp. 75–80, DOI:10.1016/s0022-5347(17)59647-0, ISSN 0022-5347, PMID 4600662.
- ^ AMS 800™ Urinary Control System For Male Patients: Oerating Room Manual (PDF), Minnetonka, MN, Boston Scientific Corporation, 2017.
- ^ Zephyr Surgical Implants, ARTIFICIAL URINARY SPHINCTER ZSI 375 (PDF), Secondª ed., Geneva, Switzerland, Zephyr Surgical Implants, November 2019.
- ^ Ireneusz Ostrowski, Tomasz Golabek e Janusz Ciechan, Preliminary outcomes of the European multicentre experience with the ZSI 375 artificial urinary sphincter for treatment of stress urinary incontinence in men, in Central European Journal of Urology, vol. 72, n. 3, 2019, pp. 263–269, DOI:10.5173/ceju.2019.1920, PMID 31720028.
- ^ Ireneusz Ostrowski, Janusz Ciechan e Emil Sledz, Four-year follow-up on a ZSI 375 artificial urinary sphincter for male urinary incontinence from one urological centre in Poland, in Central European Journal of Urology, vol. 71, n. 3, 2018, pp. 320–325, DOI:10.5173/ceju.2018.1704, PMID 30386654.
- ^ Jaspreet S. Sandhu, Alexandra C. Maschino e Andrew J. Vickers, The Surgical Learning Curve for Artificial Urinary Sphincter Procedures Compared to Typical Surgeon Experience, in European Urology, vol. 60, n. 6, December 2011, pp. 1285–1290, DOI:10.1016/j.eururo.2011.05.048, PMID 21665357. URL consultato il 27 January 2020.
- ^ Frederic Staerman, Christophe G-Llorens e Priscilla Leon, ZSI 375 artificial urinary sphincter for male urinary incontinence: a preliminary study, in BJU International, vol. 111, 4b, April 2013, pp. E202–E206, DOI:10.1111/j.1464-410X.2012.11468.x, PMID 22937774.
- ^ Alejandro Carvajal Obando, Federico Gavira Gil e Álvaro Gutiérrez Martinez, EFFICACY OF THE ARTIFICIAL URINARY SPHINCTER ZSI 375 FOR TREATMENT OF POST-RADICAL PROSTATECTOMY INCONTINENCE IN PATIENTS WITH INTRINSIC SPHINCTER DEFICIENCY: A PRELIMINARY STUDY, in European Medical Journal, vol. 2, n. 2, 1º June 2017, pp. 22–26. URL consultato il 27 January 2020.
- ^ Ireneusz Ostrowski, Mariusz Blewniewski e Frank Neugart, Multicentre experience with ZSI 375 artificial urinary sphincter for the treatment of stress urinary incontinence in men, in Urologia Journal, vol. 84, n. 3, 1º August 2017, pp. 148–152, DOI:10.5301/uj.5000246, PMID 28574143.
- ^ Eric Chung, Contemporary surgical devices for male stress urinary incontinence: a review of technological advances in current continence surgery, in Translational Andrology and Urology, vol. 6, Supplement 2, July 2017, pp. S112–S121, DOI:10.21037/tau.2017.04.12, PMID 28791230.
- ^ a b F.C. Burkhard, J.L.H.R. Bosch e F. Cruz, EAU Guidelines on Urinary Incontinence in Adults (PDF), Arnhem, The Netherlands, European Association of Urology, 2018, ISBN 978-94-92671-01-1.
- ^ Jonathan C. Routh e Douglas A. Husmann, Long-term continence outcomes after immediate repair of pediatric bladder neck lacerations extending into the urethra, in The Journal of Urology, vol. 178, 4S, 1º October 2007, pp. 1816–1818, DOI:10.1016/j.juro.2007.05.094, PMID 17707005.
- ^ DK Kandpal, SK Rawat e S Kanwar, Single piece artificial urinary sphincter for secondary incontinence following successful repair of post traumatic urethral injury, in Journal of Indian Association of Pediatric Surgeons, vol. 18, n. 4, 2013, pp. 152–154, DOI:10.4103/0971-9261.121120, PMID 24347870.
- ^ MAR Islah, Sung Yong Cho e Hwancheol Son, The Current Role of the Artificial Urinary Sphincter in Male and Female Urinary Incontinence, in The World Journal of Men's Health, vol. 31, n. 1, April 2013, pp. 21–30, DOI:10.5534/wjmh.2013.31.1.21, PMID 23658862.
- ^ a b c Jaspreet S. Sandhu, Alexandra C. Maschino e Andrew J. Vickers, The Surgical Learning Curve for Artificial Urinary Sphincter Procedures Compared to Typical Surgeon Experience, in European Urology, vol. 60, n. 6, 2011, pp. 1285–1290, DOI:10.1016/j.eururo.2011.05.048, PMID 21665357.
- ^ Ireneusz Ostrowski, Mariusz Blewniewski e Frank Neugart, Multicentre Experience with ZSI 375 Artificial Urinary Sphincter for the Treatment of Stress Urinary Incontinence in Men, in Urologia Journal, vol. 84, n. 3, 29 May 2017, pp. 148–152, DOI:10.5301/uj.5000246, PMID 28574143.
- ^ Christophe Llorens e Tobias Pottek, Urinary Artificial Sphincter ZSI 375 for Treatment of Stress Urinary Incontinence in Men: 5 and 7 Years Follow-Up Report, in Urologia Journal, vol. 84, n. 4, 18 May 2017, pp. 263–266, DOI:10.5301/uj.5000243, PMID 28525665.
- ^ a b c d Frank Van der Aa, Marcus J. Drake e George R. Kasyan, The Artificial Urinary Sphincter After a Quarter of a Century: A Critical Systematic Review of Its Use in Male Non-neurogenic Incontinence, in European Urology, vol. 63, n. 4, April 2013, pp. 681–689, DOI:10.1016/j.eururo.2012.11.034, PMID 23219375. URL consultato il 25 January 2020.
- ^ Drogo K. Montague, Artificial Urinary Sphincter: Long-Term Results and Patient Satisfaction, in Advances in Urology, vol. 2012, Special Issue, 2012, pp. 1–4, DOI:10.1155/2012/835290, PMID 22536227.
- ^ Eric Chung, A state-of-the-art review on the evolution of urinary sphincter devices for the treatment of post-prostatectomy urinary incontinence: Past, present and future innovations, in Journal of Medical Engineering & Technology, vol. 38, n. 6, 17 June 2014, pp. 328–332, DOI:10.3109/03091902.2014.899400, PMID 24936961.
- ^ Sender Herschorn, The artificial urinary sphincter is the treatment of choice for post–radical prostatectomy incontinence, in Canadian Urological Association Journal, vol. 2, n. 5, 17 April 2013, pp. 536–9, DOI:10.5489/cuaj.924, PMID 18953453.
- ^ Boyd R. Viers, Brian J. Linder e Marcelino E. Rivera, Long-Term Quality of Life and Functional Outcomes among Primary and Secondary Artificial Urinary Sphincter Implantations in Men with Stress Urinary Incontinence, in The Journal of Urology, vol. 196, n. 3, 2016, pp. 838–843, DOI:10.1016/j.juro.2016.03.076, PMID 26997310.
- ^ Scott E. Litwiller, Kap B. Kim e Patricia D. Fone, Post-Prostatectomy incontinence and the Artificial Urinary Sphincter: A Long-Term Study of Patient Satisfaction and Criteria for Success, in Journal of Urology, vol. 156, n. 6, December 1996, pp. 1975–1980, DOI:10.1016/S0022-5347(01)65408-9, PMID 8911369. URL consultato il 2 February 2020.
- ^ Brian J. Linder, Marcelino E. Rivera e Matthew J. Ziegelmann, Long-term Outcomes Following Artificial Urinary Sphincter Placement: An Analysis of 1082 Cases at Mayo Clinic, in Urology, vol. 86, n. 3, 2015, pp. 602–607, DOI:10.1016/j.urology.2015.05.029, PMID 26135815.
- ^ Mahreen Hussain, Tamsin J. Greenwell e Suzie N. Venn, The current role of the artificial urinary sphincter for the treatment of urinary incontinence, in Journal of Urology, vol. 174, n. 2, 1º August 2005, pp. 418–424, DOI:10.1097/01.ju.0000165345.11199.98, PMID 23658862.
- ^ MAR Islah, Sung Yong Cho e Hwancheol Son, The Current Role of the Artificial Urinary Sphincter in Male and Female Urinary Incontinence, in The World Journal of Men's Health, vol. 31, n. 2, April 2013, pp. 21–30, DOI:10.5534/wjmh.2013.31.1.21, PMID 23658862.
- ^ Bastian Amend, Patricia Toomey e Karl-Dietrich Sievert, Artificial sphincter, in Current Opinion in Urology, vol. 23, n. 6, November 2013, pp. 520–527, DOI:10.1097/01.MOU.0000434591.02823.d0, PMID 24080811. URL consultato il 20 January 2020.
- ^ a b (EN) Drugs.com, https://www.drugs.com/cg/urinary-sphincter-replacement-discharge-care.html. URL consultato il 25 March 2020.
- ^ (EN) www.mskcc.org, Memorial Sloan Kettering Cancer Center, https://www.mskcc.org/cancer-care/patient-education/artificial-urinary-sphincter. URL consultato il 25 March 2020.
- ^ Deepak K Agarwal, Brian J Linder e Daniel S Elliott, Artificial urinary sphincter urethral erosions: Temporal patterns, management, and incidence of preventable erosions, in Indian Journal of Urology, vol. 0, n. 1, 2016, pp. 26–29, DOI:10.4103/0970-1591.195758, PMID 28197026.
- ^ Daniel S Elliott, David M Barrett e Mohamed Gohma, Does nocturnal deactivation of the artificial urinary sphincter lessen the risk of urethral atrophy?, in Urology, vol. 57, n. 6, June 2001, pp. 1051–1054, DOI:10.1016/s0090-4295(01)00963-3. URL consultato il 25 March 2020.
Errore nelle note: Il tag <ref> con nome "AU" definito nel <references> gruppo "" non ha alcun contenuto.
link esterni[modifica | modifica wikitesto]
[[Categoria:Protesi mediche]] [[Categoria:Strumenti medici]]