Ione arenio

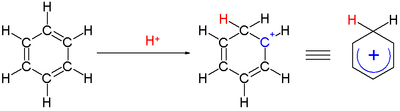
Uno ione arenio in chimica organica è un catione cicloesadienile che compare come intermedio di reazione in una sostituzione elettrofila aromatica.[1] Per ragioni storiche questo complesso viene anche chiamato intermedio di Wheland (da George Willard Wheland)[2] o complesso sigma o complesso-σ.
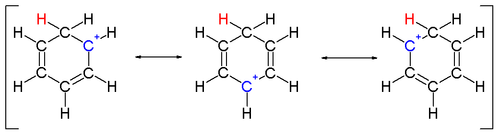
Due atomi di idrogeno legati ad un atomo di carbonio giacciono in un piano perpendicolare a quello dell'anello benzenico.[3] Lo ione arenio non è più una specie aromatica, è tuttavia relativamente stabile a causa della delocalizzazione per risonanza: la carica positiva viene delocalizzata su 5 atomi di carbonio attraverso il sistema π, come si vede nelle seguenti strutture di risonanza:
Un ulteriore contributo alla stabilità dello ione arenio è il guadagno energetico che risulta dal forte legame tra il benzene e l'elettrofilo complessato.
Lo ione arenio più piccolo è il benzene protonato C6H7+. Lo ione benzenio può essere isolato come composto stabile quando il benzene viene protonato dal carborano superacido H(CB11H(CH3)5Br6).[4] Il sale benzenio è cristallino e termicamente stabile fino a 150 °C. Le lunghezze di legame ricavate dalla cristallografia a raggi X sono consistenti con la struttura di un catione cicloesadienile.
Esistono diversi metodi per la generazione di uno ione arenio stabile. In uno studio uno ione metilen-arenio è stabilizzato dalla complessazione con un metallo:[5]
In questa sequenza di reazione il complesso di partenza R-Pd(II)-Br 1 stabilizzato dal TMEDA viene ossidato dal dtpp al complesso metallico 2. L'attacco elettrofilo del metiltriflato forma lo ione metilen-arenio 3 con una carica positiva localizzata sulla posizione aromatica para (basato su cristallografia a raggi X) e con il gruppo metilenico posizionato 6º fuori dal piano dell'anello. La reazione con acqua e poi con trietilammina idrolizza il gruppo etereo.
Note[modifica | modifica wikitesto]
- ^ Stable carbocations. CXVIII. General concept and structure of carbocations based on differentiation of trivalent (classical) carbenium ions from three-center bound penta- of tetracoordinated (nonclassical) carbonium ions. Role of carbocations in electrophilic reactions George A. Olah J. Am. Chem. Soc.; 1972; 94(3) pp 808 - 820; DOI: 10.1021/ja00758a020
- ^ A Quantum Mechanical Investigation of the Orientation of Substituents in Aromatic Molecules G. W. Wheland J. Am. Chem. Soc.; 1942; 64(4) pp 900 - 908; DOI: 10.1021/ja01256a047
- ^ A guidebook to mechanism in organic chemistry, Peter Sykes; pp 130-133
- ^ Isolating Benzenium Ion Salts Christopher A. Reed, Kee-Chan Kim, Evgenii S. Stoyanov, Daniel Stasko, Fook S. Tham, Leonard J. Mueller, and Peter D. W. Boyd J. Am. Chem. Soc.; 2003; 125(7) pp 1796 - 1804; DOI: 10.1021/ja027336o
- ^ Synthesis and Reactivity of the Methylene Arenium Form of a Benzyl Cation, Stabilized by Complexation Elena Poverenov, Gregory Leitus, and David Milstein J. Am. Chem. Soc.; 2006; 128(51) pp 16450 - 16451; (Communication) DOI: 10.1021/ja067298z
Collegamenti esterni[modifica | modifica wikitesto]
- IUPAC Gold Book, "arenium ions", su goldbook.iupac.org.