Utente:Chemr90/Sandbox/molecola1
In chimica e fisica, una molecola (dal latino scientifico molecula, derivato a sua volta da moles, che significa "mole", "piccola quantità"[1][non chiaro]) è un insieme elettricamente neutro e stabile di almeno due atomi (dello stesso elemento o di elementi diversi) uniti da un legame chimico covalente.[2][3]
Un insieme di atomi che presenta una carica elettrica (positiva o negativa), viene chiamato ione. Nel caso in cui un insieme di atomi abbia uno o più elettroni spaiati, si parla di radicale. Le molecole, gli ioni e i radicali sono chiamati in generale "entità molecolari".
In chimica organica e biochimica il termine "molecola" identifica talvolta gli ioni poliatomici, mentre nella teoria cinetica dei gas è spesso utilizzato per ogni particella gassosa, indipendentemente dalla sua composizione: secondo tale definizione anche i singoli atomi nella famiglia dei gas nobili possono essere considerati molecole.[4]
Storia[modifica | modifica wikitesto]
La definizione di molecola si è evoluta nel tempo parallelamente alla conoscenza della struttura della materia. Le prime definizioni erano meno precise, ad esempio la molecola era definita come la più piccola particella di una sostanza chimica pura che ne mantenga la composizione e le proprietà chimiche.[5] Questa definizione si rivela inefficace già dall'osservazione di sostanze di esperienza comune come le rocce, i sali e i metalli. Questi infatti sono composti da grandi reticoli cristallini di atomi o ioni e non da molecole discrete.
Rappresentazione delle molecole[modifica | modifica wikitesto]
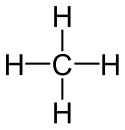

Le molecole possono essere rappresentate dalla loro formula chimica, che indica almeno il tipo (cioè l'elemento chimico al quale appartengono) e il numero di atomi che la costituiscono. Quando la formula chimica mostra anche il modo in cui gli atomi sono legati tra loro, si parla di formula di struttura, altrimenti si parla di formula bruta. Ad esempio la formula bruta CH4 (molecola del metano) indica una molecola costituita da un atomo di carbonio (simbolo: C) e 4 atomi di idrogeno (simbolo: H). Un esempio di formula di struttura della stessa molecola è quella mostrata a sinistra, dove sono indicati anche i legami tra i singoli atomi.
Legami[modifica | modifica wikitesto]
Legami intramolecolari[modifica | modifica wikitesto]

I legami che agiscono tra gli atomi della stessa molecola sono detti legami intramolecolari. Gli elettroni in un atomo isolato avvolgono il nucleo atomico, durante la formazione di un legame con un altro atomo gli elettroni di entrambi i gli atomi originari sono coinvolti e assumono una nuova disposizione. A seconda del tipo di nuclei atomici coinvolti nel legame, si avranno diverse disposizioni degli elettroni, sono identificate due classi di legami:
- legami covalenti, dove gli elettroni sono condivisi tra i due nuclei.
- legami ionici, dove gli elettroni sono nettamente polarizzati verso un nucleo, in questo caso si formano due ioni con cariche opposte.
Legami intermolecolari[modifica | modifica wikitesto]
La disposizione nello spazio di una molecola è influenzata anche da legami tra diverse molecole, detti "legami intermolecolari". Un esempio di legame intermolecolare è il legame idrogeno. Altre interazioni intermolecolari sono le interazioni di Van der Waals.
Struttura molecolare[modifica | modifica wikitesto]
La struttura di una molecola corrisponde al tipo di atomi che costituiscono la molecola e a come essi sono legati tra loro.
Una molecola può essere costituita da più atomi di un solo elemento chimico o da atomi di elementi diversi. Nel primo caso, le sostanze costituite da un insieme di tali molecole si dicono "sostanze semplici"[6] (ad esempio O2, O3, N2, H2), mentre nel secondo caso si dicono "sostanze composte" o più semplicemente "composti"[6] (ad esempio H2O, CO2, H2SO4).[7]
Isomeri[modifica | modifica wikitesto]
Famiglie di molecole costituite dagli stessi atomi, ovvero con la stessa formula molecolare, legati tra loro in maniera diversa sono dette "isomeri", e il modo in cui sono legati influisce sulle proprietà chimico-fisiche della sostanza.
Determinazione della struttura molecolare[modifica | modifica wikitesto]

Diverse tecniche possonon essere usate per ricavare informazioni sulla struttura di una molecola. Le più utilizzate sono la spettroscopia, la spettrometria di massa, e la risonanza magnetica nucleare. Le spettroscopie molecolari ricavano informazioni sulla struttura molecolare tramite l'analisi dettagliata delle proprietà di assorbimento della molecola. Una tecnica spettroscopica molto comune è la spettroscopia infrarossa, essa permette di ottenere informazioni strutturali grazie alla stimolazione delle transizioni vibrazionali con fotoni nel campo dell'infrarosso. Un altro esempio di tecnica spettroscopica utilizzata nell'analisi strutturale è la spettroscopia di risonanza magnetica nucleare, mostrata qui di fianco, che in questo caso studia le transizioni di spin magnetico nucleare.
Simmetria nelle molecole[modifica | modifica wikitesto]
Le proprietà simmetriche delle molecole hanno un'influenza su alcune proprietà chimico-fisiche, un esempio comune si trova nella spettroscopia infrarossa.
Dimensioni molecolari[modifica | modifica wikitesto]
Le dimensioni delle molecole variano dalle decine di picometri, come nel caso della molecola di idrogeno, fino a più di un metro, come nel caso del DNA umano.[8]
Chimica macromolecolare[modifica | modifica wikitesto]
Biomolecole[modifica | modifica wikitesto]
Note[modifica | modifica wikitesto]
- ^ Etimologia : molecola, molecula;, su www.etimo.it. URL consultato il 27 ottobre 2018.
- ^ Pauling, Linus
- ^ Ebbin, Darrell
- ^ Sulekh Chandra, Comprehensive Inorganic Chemistry, New Age Publishers, ISBN 8122415121.
- ^ General Chemistry Online: Glossary:, su antoine.frostburg.edu. URL consultato il 27 ottobre 2018.
- ^ a b Accademia Nazionale delle Scienze detta dei XL, "Atomi ed elementi"
- ^ Rolla, pp. 6-7
- ^ (EN) Glenn Elert, Length of a Human DNA Molecule - The Physics Factbook, su hypertextbook.com. URL consultato il 27 ottobre 2018.
Voci correlate[modifica | modifica wikitesto]
- Atomo
- Composto organico
- Formula chimica
- Macromolecola
- Molecola biatomica
- Interazione debole
- Isomeria
- Legame chimico
- Simmetria molecolare
- Storia della chimica
- Orbitale molecolare
Altri progetti[modifica | modifica wikitesto]
 Wikizionario contiene il lemma di dizionario «molecola»
Wikizionario contiene il lemma di dizionario «molecola» Wikimedia Commons contiene immagini o altri file su molecola
Wikimedia Commons contiene immagini o altri file su molecola
Collegamenti esterni[modifica | modifica wikitesto]
