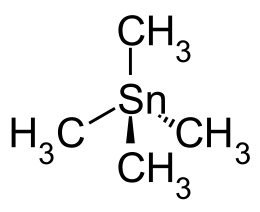
Tetrametilstagno
| Tetrametilstagno | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| tetrametilstannano | |
| Nomi alternativi | |
| stagno tetrametile | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C4H12Sn |
| Massa molecolare (u) | 178,850 |
| Aspetto | liquido incolore[1] |
| Numero CAS | |
| Numero EINECS | 209-833-6 |
| PubChem | 11661 |
| SMILES | C[Sn](C)(C)C |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,30[1] |
| Indice di rifrazione | 1,314[2] |
| Solubilità in acqua | praticamente insolubile |
| Temperatura di fusione | −53 °C (220 K)[1] |
| Temperatura di ebollizione | 78 °C (351 K)[1] |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | -52,3[2] |
| Indicazioni di sicurezza | |
| Punto di fiamma | 12 °C |
| Simboli di rischio chimico | |
  
| |
| pericolo | |
| Frasi H | 225 - 300+310+330 - 400+410 [1] |
| Consigli P | 210 - 233 - 273 - 280 - 303+361+353 - 304+340+310 [1] |
Il tetrametilstagno è il composto metallorganico con formula (CH3)4Sn. È uno dei più semplici stannani. In condizioni normali è un liquido incolore, volatile e quasi inodore.[1] Il composto viene usato industrialmente come intermedio nella sintesi di altri composti organo-stagno; può essere usato anche per la metilazione di alogenuri organici e inorganici.[3]
Sintesi
[modifica | modifica wikitesto]Il tetrametilstagno viene preparato partendo da tetracloruro di stagno, alchilandolo con reattivi di Grignard come lo ioduro di metilmagnesio:[4]
Usi
[modifica | modifica wikitesto]Precursore di composti metilstagno
[modifica | modifica wikitesto]Il tetrametilstagno è usato per produrre cloruro di trimetilstagno (CH3)3SnCl e altri alogenuri di metilstagno, a loro volta utili per ottenere altri composti organici dello stagno. A tale scopo (CH3)4Sn e SnCl4 sono fatti reagire a temperature tra 100 °C e 200 °C per ottenere (CH3)3SnCl:[3]
Un'altra possibilità è far reagire (CH3)4Sn con cloruro di mercurio(II):[4]
Vari composti metilstagno sono usati come precursori per ottenere stabilizzanti per polivinilcloruro (PVC).[5]
Funzionalizzazione di superfici
[modifica | modifica wikitesto]Il tetrametilstagno si decompone in fase gassosa a circa 277 °C; i vapori di (CH3)4Sn reagiscono con la silice producendo legami (CH3)3Sn-silice:
Questa reazione si può fare anche con altri sostituenti alchilici. In un processo simile il tetrametilstagno è stato usato per funzionalizzare alcune zeoliti a temperature fino a -90 °C.[6]
In sintesi organica
[modifica | modifica wikitesto]Il tetrametilstagno reagisce con gli alogenuri acilici per formare metil chetoni:[7]
Tossicità / Indicazioni di sicurezza
[modifica | modifica wikitesto]Il composto è disponibile in commercio; è facilmente infiammabile e forma miscele esplosive con l'aria. È fortemente tossico e può essere fatale per ingestione, per contatto con la pelle o per inalazione. È fortemente tossico anche per gli organismi acquatici.[1]
Note
[modifica | modifica wikitesto]- ^ a b c d e f g h GESTIS 2022, GESTIS.
- ^ a b Haynes 2015
- ^ a b Graf 2002
- ^ a b Scott et al. 2001
- ^ Thoonen et al. 2004
- ^ Davies 2008
- ^ Labadie e Stille 1983
Bibliografia
[modifica | modifica wikitesto]- (EN) A. G. Davies, Tin Organometallics, in R. H. Crabtree e D. M. P. Mingos (a cura di), Comprehensive Organometallic Chemistry III, Elsevier, 2008, pp. 809–883, DOI:10.1016/B0-08-045047-4/00054-6, ISBN 9780080450476.
- GESTIS, Tetramethyltin, su gestis.dguv.de, 2022. URL consultato il 5 ottobre 2022. Pagina del tetrametilstagno nel data base GESTIS.
- (EN) G. G. Graf, Tin, Tin Alloys, and Tin Compounds, in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, 2002, DOI:10.1002/14356007.a27_049.
- (EN) W. M. Haynes (a cura di), CRC Handbook of Chemistry and Physics, 96ª ed., Boca Raton, CRC Press, 2015, ISBN 978-1-4822-6097-7.
- (EN) J. W. Labadie e J. K. Stille, Mechanisms of the palladium-catalyzed couplings of acid chlorides with organotin reagents, in J. Am. Chem. Soc., vol. 105, n. 19, 1983, pp. 6129-6137, DOI:10.1021/ja00357a026.
- (EN) W.J. Scott, J.H. Jones e A.F. Moretto, Tetramethylstannane, in Encyclopedia of Reagents for Organic Synthesis, Wiley, 2001.
- (EN) S. H. L. Thoonen, B.-J. Deelman e G. van Koten, Synthetic aspects of tetraorganotins and organotin(IV) halides, in J. Organomet. Chem., vol. 689, n. 13, 2004, pp. 2145-2157, DOI:10.1016/j.jorganchem.2004.03.027.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su tetrametilstagno
Wikimedia Commons contiene immagini o altri file su tetrametilstagno




