Esametilfosforammide
| Esametilfosforammide | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| esametilfosforammide | |
| Nomi alternativi | |
| triammide esametilfosforica esametilfosfammide ossido di tri(dimetilammino)fosfina HMPA | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H18N3OP |
| Massa molecolare (u) | 179,20 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 211-653-8 |
| PubChem | 12679 |
| SMILES | CN(C)P(=O)(N(C)C)N(C)C |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,024 |
| Solubilità in acqua | completamente miscibile |
| Temperatura di fusione | 7,2 °C (280,35 K) |
| Temperatura di ebollizione | 233 °C (506,15 K) |
| Tensione di vapore (Pa) a 298,15 K | 9 |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 2.650 (orale, ratto) |
| Indicazioni di sicurezza | |
| Punto di fiamma | 105 °C (378,15 K) |
| Temperatura di autoignizione | 230 °C (503,15 K) |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 350 - 340 [1] |
| Consigli P | 201 - 308+313 [2] |
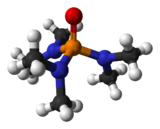
L'esametilfosforammide, spesso indicata con HMPA (abbreviazione dell'inglese Hexamethylphosphoramide), è l'ammide dell'acido fosforico con formula [(CH3)2N]3PO. A temperatura ambiente si presenta come un liquido incolore. Viene impiegata come solvente polare aprotico e come additivo nella sintesi organica.
Struttura e reattività[modifica | modifica wikitesto]
L'esametilfosforammide rappresenta l'ossido della fosfina terziaria altamente basica esametilfosfotriammide P(NMe2)3. Similmente ad altri ossidi di fosfina (per esempio l'ossido di trifenilfosfina), la molecola possiede un nucleo tetraedrico e un legame P-O altamente polarizzato, con una significativa carica negativa localizzata sull'atomo di ossigeno.
I composti che contengono un legame azoto-fosforo sono tipicamente degradati dall'acido cloridrico formando una ammina protonata e fosfato.
Applicazioni[modifica | modifica wikitesto]
L'HMPA è utilizzata come solvente per polimeri, gas e composti organometallici. Migliora la selettività delle reazioni di litiazione scindendo gli oligomeri formati dalle basi di litio come il butillitio. Dato che l'esametilfosforammide solvata selettivamente i cationi, questo solvente è in grado di accelerare alcune reazioni SN2 difficoltose. L'atomo basico di ossigeno nell'HMPA coordina fortemente il catione Li+.[3] Un complesso del perossido di molibdeno con l'esametilfosforammide viene utilizzato come ossidante nella sintesi organica.
Reagenti alternativi[modifica | modifica wikitesto]
Il dimetilsolfossido può essere spesso utilizzato come solvente in sostituzione dell'HMPA. Sono entrambi forti accettori di legame idrogeno, e i loro atomi di ossigeno legano i cationi metallici. Altre alternative all'HMPA includono le tetraalchiluree[4] e le alchiluree cicliche come DMPU.[5]
Tossicità[modifica | modifica wikitesto]
L'esametilfosforammide è tossica ed è stata dimostrata in grado di indurre il cancro nasale nei ratti.[3] L'HMPA può essere degradata a composti meno tossici per azione dell'acido cloridrico.
Note[modifica | modifica wikitesto]
- ^ Scheda IFA-GESTIS, su gestis-en.itrust.de. URL consultato il 16 ottobre 2014 (archiviato dall'url originale l'11 novembre 2016).
- ^ Sigma Aldrich; rev. del 18.12.2014
- ^ a b Dykstra, R. R. "Hexamethylphosphoric Triamide" Encyclopedia of Reagents for Organic Synthesis, 2001 John Wiley & Sons. DOI: 10.1002/047084289X.rh020
- ^ Beck, A. K.; Seebach, D. "N,N'-Dimethylpropyleneurea" in Encyclopedia of Reagents for Organic Synthesis, 2001 John Wiley & Sons, New York. DOI: 10.1002/047084289X.rd366
- ^ Triptikumar Mukhopadhyay, Dieter Seebach, Substitution of HMPT by the cyclic urea DMPU as a cosolvent for highly reactive nucleophiles and bases, in Helvetica Chimica Acta, vol. 65, n. 1, 1982, pp. 385–391, DOI:10.1002/hlca.19820650141.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Esametilfosforammide
Wikimedia Commons contiene immagini o altri file su Esametilfosforammide
Collegamenti esterni[modifica | modifica wikitesto]
| Controllo di autorità | GND (DE) 4159805-2 |
|---|