Ficoeritrina
| Ficoeritrina | |
|---|---|
| Identificatori | |
| Simbolo | Phycoerythr_ab |
| Pfam | PF02972 |
| SCOP | 1qgw |
La ficoeritrina (a volte abbreviata con la sigla PE) è una proteina cromofora di colore rosso, ovvero un pigmento fotosintetico accessorio, appartenente alla famiglia delle ficobiliproteine aventi lo scopo di intercettare la luce; è presente nelle alghe rosse[1] e nelle criptoficee[2].
Come tutte le ficobiliproteine è composta da una parte proteica legata tramite legame covalente a dei cromofori chiamati ficobiline. Nella famiglia della ficoeritrina le ficobiline più conosciute sono la ficoeritrobilina, il cromoforo tipico accettore della ficoeritrina, e a volte la ficourobilina. Le ficoeritrine sono solitamente composte di monomeri (αβ), organizzati in un trimero a forma di disco (αβ)3 o in un esamero (αβ)6 (il secondo è l'unità funzionale del ficobilisoma). Questi complessi tipici contengono anche un terzo tipo di subunità detta catena γ.[1]
Ficobilisomi[modifica | modifica wikitesto]

Le ficobiliproteine fanno parte di un grande complesso proteico con il compito di intercettare la luce chiamato ficobilisoma. Nelle alghe rosse sono ancorati al lato stromale delle membrane del tilacoide nei cloroplasti, mentre nelle criptoficee sono ridotti e sono densamente raggruppati all'interno del lume del tilacoide, presentando molecole di ficoeritrina PE545.[2][4]
La ficoeritrina è un pigmento accessorio responsabile della fotosintesi. L'energia luminosa è catturata dalla ficoeritrina e successivamente trasferita alla coppia di molecole di clorofilla, che costituisce il centro di reazione, principalmente tramite la ficocianina e l'alloficocianina, altre due ficobiliproteine.
Caratteristiche strutturali[modifica | modifica wikitesto]
Le ficoeritrine, eccetto la PE545, sono composte da monomeri (αβ) assemblati in esameri discoidali (αβ)6 o in trimeri (αβ)3 che racchiudono un canale centrale. Nei ficobilisomi ogni trimero o esamero contiene almeno una proteina di collegamento situata nel canale centrale. La B-ficoeritrina (B-PE) e la R-ficoeritrina (R-PE) delle alghe rosse hanno oltre alle catene α e β una terza subunità γ che combina la proteina di collegamento e le funzioni di intercettazione della luce poiché porta dei cromofori.[1]

La R-ficoeritrina è prodotta prevalentemente dalle alghe rosse. La proteina è costituita da almeno tre differenti subunità e varia a seconda della specie di alga che la produce. La struttura delle subunità della R-ficoeritrina più comune è (αβ)6γ. La subunità α possiede due ficoeritrobiline (PEB), la subunità β invece ne ha due o tre e possiede inoltre una ficourobilina (PUB), mentre le subunità γ presentano tre PEB e due PUB (è il caso della subunità γ1) o una o due PEB e una sola PUB (come nella subunità γ2). Il peso molecolare della R-ficoeritrina è di 250000 Dalton.
Le strutture cristalline disponibili nel Protein Data Bank[8] contengono in una unità asimmetrica (αβ)2 o (αβγ)2 di diverse ficoeritrine:


| Cromoforo o altra molecola non proteica | Ficoeritrina | Catena | |||
|---|---|---|---|---|---|
| PE545 | B-PE | R-PE | altri tipi | ||
| Biline | 8 | 10 | 10 | 10 | α e β |
| Ficoeritrobilina (PEB) | 6 | 10 | 0 o 8 | 8 | β (PE545) o α e β |
| 15,16-diidrobiliverdina (DBV) | 2 | - | - | - | α (-3 e -2) |
| Ficocianobilina (CYC) | - | - | 8 o 7 o 0 | - | α e β |
| Biliverdina IX alpha (BLA) | - | - | 0 o 1 | - | α |
| Ficourobilina (PUB) | - | - | 2 | 2 | β |
| 5-idrossilisina (LYZ) | 1 o 2 | - | - | - | α (-3 o -3 e -2) |
| N-metil asparagina (MEN) | 2 | 2 | 0 o 2 | 2 | β |
| Ione solfato SO42− (SO4) | - | 5 o 1 | 0 o 2 | - | α o α e β |
| Ione cloruro Cl− (CL) | 1 | - | - | - | β |
| Ione magnesio Mg2+ (MG) | 2 | - | - | - | α-3 e β |
| File del PDB controllati | 1XG0 1XF6 1QGW |
3V57 3V58 |
1EYX 1LIA 1B8D |
2VJH | |
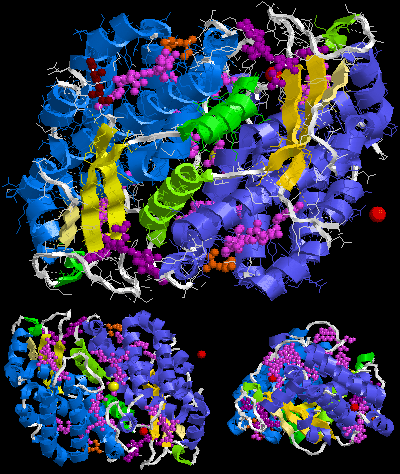
La molecola biologica della ficoeritrina 545 è di tipo (αβ)2 o piuttosto (α3β)(α2β). I numeri 2 e 3 dopo le lettere α nella seconda formula sono in questo caso parte del nome della catena, non il loro computo. Il nome corrispondente delle criptoficee della catena α3 è catena α1.
Il più grande assemblaggio di molecole della B-ficoeritrina (B-PE) è il trimero (αβ)3[5][6]. Tuttavia alcune preparazioni effettuate con alghe rosse danno anche l'esamero (αβ)6[1]. Nel caso della R-ficoeritrina la molecola biologica più grande è (αβγ)6, (αβγ)3(αβ)3 o (αβ)6 a seconda della pubblicazione, per altri tipi di ficoeritrina è invece (αβ)6. Queste catene γ sono molto brevi e consistono solamente di tre o sei aminoacidi riconoscibili[11][12] , mentre la catena γ di collegamento è più lunga (ad esempio la catena γ33 dell'alga rossa Aglaothamnion neglectum misura 277 aminoacidi ed è lunga 33 kDa)[13][1]. Questo perché la densità elettronica del gamma-polipeptide è in gran parte mediata dalla sua triplice simmetria cristallografica e solo pochi aminoacidi possono essere modellati.[11][12][14][15]
Nel caso di (αβγ)6, (αβ)6 o (αβγ)3(αβ)3 i valori della tabella dovrebbero essere moltiplicati per tre, (αβ)3 contiene numeri intermedi di molecole non proteiche.
Nella ficoeritrina PE545 una catena α (-2 or -3) lega una molecola di bilina, in altri casi ne lega due. La catena β si lega sempre a tre molecole. La breve catena γ non si lega a nessuna molecola.
Due molecole di N-metil asparagina sono legate alla catena β, una 5-idrossilisina ad una catena α (-3 o -2), uno ione Mg2+ ad α-3 e β, uno ione Cl− a β, e una o due molecole di ione SO42− ad α o β.


Caratteristiche spettrali[modifica | modifica wikitesto]

I picchi di assorbimento nello spettro della luce visibile sono misurati a 495 e 545/566 nm, a seconda del legame dei cromofori e dell'organismo considerato. Vi è un forte picco di emissione a 575 ± 10 nm (ciò significa che la ficoeritrina assorbe la luce leggermente blu-verde e giallastra ed emette luce di colore giallo-arancio).
| Proprietà | Valore |
|---|---|
| Massimo di assorbimento | 565 nm |
| Picco d'assorbimento addizionale | 498 nm |
| Massimo di emissione | 573 nm |
| Coefficiente di estinzione (ε) | 1.96 x 106 M−1cm−1 |
| Resa quantica (QY) | 0.84 |
| Luminosità (ε x QY) | 1.65 x 106 M−1cm−1 |
Le biline PEB e DBV presenti nella ficoeritrina PE545 assorbono anche la luce della regione spettrale del verde, con massimi rispettivamente a 545 e 569 nm. Il massimo di emissione fluorescente è a 580 nm. [2]
Varianti della R-ficoeritrina[modifica | modifica wikitesto]

La ficoeritrina si trova in una certa varietà di specie algali, pertanto possono esservi variazioni nell'efficienza dell'assorbanza e dell'emissione di luce richiesta per l'agevolazione della fotosintesi. Questo potrebbe essere un risultato della profondità nella colonna d'acqua a cui una specifica alga risiede e di un conseguente bisogno di una maggiore o minore efficienza dei pigmenti accessori.
Con i progressi nell'imaging nella tecnologia di rilevazione che riescono a evitare un fotobleaching troppo rapido i fluorocromi proteici sono diventati un vitale e potente strumento per i ricercatori in campi come la microscopia, l'analisi dei microarray e il Western blot. Alla luce di ciò potrebbe essere benefico per i ricercatori vagliare queste R-ficoeritrine variabili per determinare quale tra esse sia la più appropriata per la loro particolare applicazione. Persino un piccolo incremento nell'efficienza della fluorescenza potrebbe ridurre il rumore di fondo e il tasso di risultati falsi negativi.
Applicazioni pratiche[modifica | modifica wikitesto]
La R-ficoeritrina è utile in laboratorio come indicatore fluorescente per la presenza di cianobatteri e per l'etichettatura degli anticorpi, spesso per la citometria a flusso. Il suo impiego è limitato nella microscopia a immunofluorescenza a causa delle sue caratteristiche di spiccato fotobleaching. Esistono anche altri tipi di ficoeritrine, come la B-ficoeritrina, che hanno proprietà spettrali leggermente differenti. La B-ficoeritrina assorbe fortemente la luce intorno ai 545 nm (regione del verde-giallastro) ed emette fortemente a 572 nm (giallo) e potrebbe essere più adatta per certi strumenti. Tuttavia, la R-ficoeritrina è molto più comunemente disponibile come coniugato degli anticorpi.
La R-ficoeritrina e la B-ficoeritrina sono tra i coloranti fluorescenti più luminosi mai identificati.
Note[modifica | modifica wikitesto]
- ^ a b c d e Ficner R. e Huber R., Refined crystal structure of phycoerythrin from Porphyridium cruentum at 0.23-nm resolution and localization of the γ subunit, in Eur. J. Biochem., vol. 218, n. 1, 1993, pp. 103–106, DOI:10.1111/j.1432-1033.1993.tb18356.x, PMID 8243457. URL consultato il 13 ottobre 2012.
- ^ a b c van der Weij-De Wit C. D., Doust A. B., van Stokkum I. H. M., Dekker J. P., Wilk K. E., Curmi P. M. G., Scholes G. D. e van Grondelle R., How Energy Funnels from the Phycoerythrin Antenna Complex to Photosystem I and Photosystem II in Cryptophyte Rhodomonas CS24 Cells (PDF), in J. Phys. Chem. B., vol. 110, 2006, pp. 25066–25073, DOI:10.1021/jp061546w, PMID 17149931. URL consultato il 13 ottobre 2012 (archiviato dall'url originale il 30 ottobre 2013).
- ^ Christophe Six, Jean-Claude Thomas, Laurence Garczarek, Martin Ostrowski, Alexis Dufresne, Nicolas Blot, David J Scanlan e Frédéric Partensky, Diversity and evolution of phycobilisomes in marine Synechococcus spp.: a comparative genomics study, in Genome Biology, vol. 8, n. 12, 2007, pp. R259, DOI:10.1186/gb-2007-8-12-r259. URL consultato il 16 aprile 2014 (archiviato dall'url originale il 17 aprile 2014).
- ^ Glazer A. N., Light Harvesting by Phycobilisomes, in Annual Review of Biophysics and Biophysical Chemistry, vol. 14, 1985, pp. 47–77, DOI:10.1146/annurev.bb.14.060185.000403, PMID 3924069. URL consultato il 13 ottobre 2012.
- ^ a b Camara-Artigas, A., Crystal Structure of the B-phycoerythrin from the red algae Porphyridium cruentum at pH8, su rcsb.org, RCSB Protein Data Bank (PDB), 16 dicembre 2011, DOI:10.2210/pdb3v57/pdb, PDB ID: 3V57. URL consultato il 12 ottobre 2012.
- ^ a b Camara-Artigas, A., Bacarizo, J., Andujar-Sanchez, M., Ortiz-Salmeron, E., Mesa-Valle, C., Cuadri, C., Martin-Garcia, J.M., Martinez-Rodriguez, S., Mazzuca-Sobczuk, T., Ibanez, M.J. e Allen, J.P., pH-dependent structural conformations of B-phycoerythrin from Porphyridium cruentum, in FEBS J., vol. 279, 2012, pp. 3680–3691, DOI:10.1111/j.1742-4658.2012.08730.x, PMID 22863205, PDB ID: 3V57. URL consultato il 12 ottobre 2012.
- ^ a b c d Image created with RasTop (Molecular Visualization Software).
- ^ Protein Data Bank, su rcsb.org, RCSB Protein Data Bank (PDB). URL consultato il 12 ottobre 2012 (archiviato dall'url originale il 28 agosto 2008).
- ^ Doust, A.B., Marai, C.N.J., Harrop, S.J., Wilk, K.E., Curmi, P.M.G. e Scholes, G.D., High resolution crystal structure of phycoerythrin 545 from the marine cryptophyte rhodomonas CS24, su rcsb.org, RCSB Protein Data Bank (PDB), 16 settembre 2004, DOI:10.2210/pdb1xg0/pdb, PDB ID: 1XG0. URL consultato l'11 ottobre 2012.
- ^ Doust, A.B., Marai, C.N.J., Harrop, S.J., Wilk, K.E., Curmi, P.M.G. e Scholes, G.D., Developing a structure-function model for the cryptophyte phycoerythrin 545 using ultrahigh resolution crystallography and ultrafast laser spectroscopy, in J.Mol.Biol., vol. 344, 2004, pp. 135–153, DOI:10.1016/j.jmb.2004.09.044, PMID 15504407, PDB ID: 1XG0. URL consultato l'11 ottobre 2012.
- ^ a b c d Contreras-Martel, C., Legrand, P., Piras, C., Vernede, X., Martinez-Oyanedel, J., Bunster, M. e Fontecilla-Camps, J.C., Crystal structure of R-phycoerythrin at 2.2 angstroms, su rcsb.org, RCSB Protein Data Bank (PDB), 9 maggio 2000, DOI:10.2210/pdb1eyx/pdb, PDB ID: 1EYX. URL consultato l'11 ottobre 2012.
- ^ a b c d Contreras-Martel, C., Martinez-Oyanedel, J., Bunster, M., Legrand, P., Piras, C., Vernede, X. e Fontecilla-Camps, J.C., Crystallization and 2.2 A resolution structure of R-phycoerythrin from Gracilaria chilensis: a case of perfect hemihedral twinning, in Acta Crystallographica Section D, vol. 57, 2001, pp. 52–60, DOI:10.1107/S0907444900015274, PMID 11134927, PDB ID: 1EYX. URL consultato l'11 ottobre 2012.
- ^ Apt K. E., Hoffman N. E. e Grossman A. R., The γ Subunit of R-phycoerythrin and Its Possible Mode of Transport into the Plastiodf Red Algae, in J Biol Chem., vol. 268, n. 22, 1993, pp. 16208–16215, PMID 8344905. URL consultato il 13 ottobre 2012.
- ^ Ritter, S., Hiller, R.G., Wrench, P.M., Welte, W. e Diederichs, K., Crystal structure of a phycourobilin-containing phycoerythrin, su rcsb.org, RCSB Protein Data Bank (PDB), 29 gennaio 1999, DOI:10.2210/pdb1b8d/pdb, PDB ID: 1B8D. URL consultato il 14 ottobre 2012.
- ^ Ritter, S., Hiller, R.G., Wrench, P.M., Welte, W. e Diederichs, K., Crystal structure of a phycourobilin-containing phycoerythrin at 1.90-A resolution, in J.Struct.Biol., vol. 126, 1999, pp. 86–97, DOI:10.1006/jsbi.1999.4106, PMID 10388620, PDB ID: 1B8D. URL consultato il 14 ottobre 2012.
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) Phycoerythrin, in Medical Subject Headings (MeSH), National Library of Medicine, 2009.