Lipasi pancreatica
| Tracilglicerolo lipasi | |
|---|---|
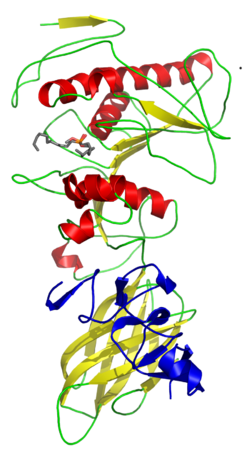 Lipasi pancreatica umana complessata con colipasi suina (in blu) ed un inibitore | |
| Numero EC | 3.1.1.3 |
| Classe | Idrolasi |
| Nome sistematico | |
| triacilglicerolo acilidrolasi | |
| Banche dati | BRENDA, EXPASY, GTD, PDB (RCSB PDB PDBe PDBj PDBsum) |
| Fonte: IUBMB | |
| PNLIP | |
|---|---|
| Gene | |
| HUGO | PNLIP |
| Locus | Chr. 10 q25.3 |
| Proteina | |
| OMIM | 246600 |
| UniProt | P16233 |
| Enzima | |
| Numero EC | 3.1.1.3 |
La lipasi pancreatica è un enzima, appartenente alla famiglia delle lipasi, secreto dal pancreas, e deputato all'idrolisi dei lipidi. È una serina-esterasi che attacca i legami esterei in C1 e in C3 dei triacilgliceroli (o trigliceridi), intervenendo così nella digestione dei grassi secondo la seguente reazione:
- Triacilglicerolo + 2 H2O 2-monoacilglicerolo + 2 acidi grassi
Affinché i triacilgliceroli possano essere assorbiti dalla mucosa intestinale, devono essere convertiti da particelle macroscopiche insolubili in micelle microscopiche finemente disperse. La conversione in piccole particelle avviene grazie all'azione dell'enzima lipasi che trasforma i triacilgliceroli in digliceridi, monogliceridi, acidi grassi liberi e glicerolo.
I prodotti dell'azione della lipasi diffondono nelle cellule epiteliali che rivestono la superficie dell'intestino. Una volta assunti dalla mucosa intestinale, gli acidi grassi e gli altri prodotti vengono riconvertiti in triacilgliceroli, che legandosi a specifiche proteine di trasporto, chiamate apolipoproteine, formano aggregati lipoproteici detti chilomicroni. Queste lipoproteine sono trasferite dalla mucosa al sistema linfatico, entrano nel sangue e vengono trasportati al muscolo e al tessuto adiposo.
Nei capillari di questi tessuti, l'enzima extracellulare lipoproteina lipasi idrolizza i triacilgliceroli ad acidi grassi e glicerolo, che entrano nelle cellule bersaglio. Nelle cellule bersaglio di tipo muscolare, gli acidi grassi vengono ossidati per produrre energia, mentre nelle cellule bersaglio del tessuto adiposo vengono riesterificati a triacilgliceroli per essere conservati come grassi di riserva.
Al contrario di altri enzimi pancreatici che sono attivati da specifiche proteasi, la lipasi pancreatica è secreta già nella forma attiva e non come zimogeno, sebbene diventi effettivamente operativa solo in presenza della colipasi a livello del duodeno.
