Fosfato di monoammonio
| Fosfato di monoammonio | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| diidrogenofosfato di ammonio | |
| Nomi alternativi | |
| diidrogenofosfato di ammonio fosfato di monoammonio | |
| Caratteristiche generali | |
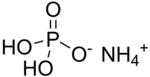
| Formula bruta o molecolare | NH4H2PO4 |
| Peso formula (u) | 115,0257 u |
| Aspetto | solido cristallino incolore |
| Numero CAS | |
| Numero EINECS | 231-764-5 |
| PubChem | 24402 |
| SMILES | N.O=P(O)(O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,80 |
| Indice di rifrazione | 1,525 |
| Solubilità in acqua | 360 g/L (20 °C) |
| Temperatura di fusione | 190 °C (463 K) |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −1445,07 kJ/mol |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | ---[1] |
Il diidrogenofosfato di ammonio (a volte anche fosfato di monoammonio) è un sale acido di ammonio dell'acido fosforico, avente formula NH4H2PO4.[2][3]
Viene sintetizzato per aggiunta di una soluzione di acido fosforico all'ammoniaca fino al punto in cui sono presenti ioni diidrogenofosfato, cioè quando la soluzione è debolmente acida.
Cristallizza in cristalli prismatici tetragonali.
Caratteristiche[modifica | modifica wikitesto]
Il fosfato di monoammonio mostra una pressione di dissociazione dell'ammoniaca di 0,05 mm Hg a 125 °C basata sulla seguente reazione di decomposizione:[4]
- NH4H2PO4(s) ⇄ NH3(g) + H3PO4(l)
I cristalli presentano il fenomeno della birifrangenza, per cui vengono utilizzati in vari campi dell'ottica. A causa della sua struttura cristallina tetragonale, presenta una simmetria ottica monoassiale negativa, con indici di rifrazione no = 1,522 e ne = 1,478 nelle lunghezze d'onda del visibile.[5]
La caratteristica di piezoelettricità dei cristalli viene sfruttata in alcuni trasduttori sonar in alternativa alla magnetostrizione. Negli anni '50 i cristalli venivano usati in alternativa al quarzo e al sale di Rochelle in quanto non igroscopici.[6]
Applicazioni[modifica | modifica wikitesto]
È utilizzato spesso nei fertilizzanti a base di fosfati, in quanto rilascia una grande quantità di azoto e fosforo in forma utilizzabile dalle piante.[7]
Questo composto è anche un componente della polvere ABC in qualche estintore a polvere secca.
Sostituendo uno ione idrogeno con uno ione ammonio, si ottiene il fosfato di diammonio, mentre sostituendo entrambi gli idrogeni con ammonio si trasforma in fosfato di ammonio.
Solubilizzato, abbassa debolmente il pH: una soluzione a 2,5 M di fosfato di monoammonio ha un pH di circa 3,7 a 25 °C.
Note[modifica | modifica wikitesto]
- ^ Sigma Aldrich; rev. del 15.05.2012
- ^ Monoammonium Phosphate (MAP) (PDF), su mosaicco.com. URL consultato il 5 giugno 2015 (archiviato dall'url originale il 17 novembre 2015).
- ^ David R. Lide, Handbook of Chemistry and Physics, 87ª ed., Boca Raton, FL, CRC Press, 1998, pp. 4–40, ISBN 0-8493-0594-2.
- ^ John R Van Wazer, Phosphorus And Its Compounds - Volume I: Chemistry, New York, Interscience Publishers, Inc, 1958, p. 503.
- ^ Amnon Yariv, Pochi Yeh, Optical Waves in Crystals, Wiley, Inc, 1984.
- ^ Willem Hackmann, Seek and Strike: Sonar, Anti-Submarine Warfare and the Royal Navy, 1914–1954, Her Majesty's Stationery Office, 1984, ISBN 0-11-290423-8.
- ^ IPNI, Monoammonium Phosphate (MAP) (PDF), su ipni.net, International Plant Nutrition Institute. URL consultato il 21 luglio 2014.
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) ammonium dihydrogen phosphate, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.

