Utente:Grasso Luigi/sanbox1/Riarrangiamento Demjanov
Il riarrangiamento di Demjanov è la reazione chimica di un'ammina primaria con l'acido nitroso riorganizzandosi per dare un alcool.[1][2][3] Implica la sostituzione con un gruppo idrossile con una possibile espansione di anello.
Viene chiamata dal nome del chimico Russo Nikolai Jakovlevich Demjanov (Dem'anov, Demianov) (1861–1938). [4]
Meccanismo della reazione[modifica | modifica wikitesto]
Il processo della reazione inizia con la diazotazione dell'ammina tramite l'acido nitroso. Il gruppo diazonio è un buon gruppo uscente, con formazione di azoto gassoso quando viene spostato dalla struttura organica. Tale spostamento può effettuarsi tramite un riarrangiamento (percorso A), nella quale uno dei legami sigma adiacenti al gruppo diazo migra. Questa migrazione comporta un'espansione dell'anello. Il carbocatione prodotto viene quindi attaccato da una molecola di acqua. Un percorso alternativo, sposta il gruppo diazo direttamente da una molecola di acqua in una reazione SN2 (percorso B). Entrambi i percorsi conducono alla formazione di un alcool.[4]
| A. | 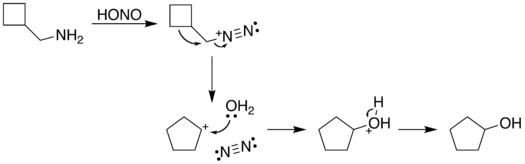 | |
| B. |  |
Applicazioni[modifica | modifica wikitesto]
Il riarrangiamento Demjanov è un metodo per produrre un ingrandimento dell'anello a 1 carbonio in anelli a quattro, cinque o sei membri. Gli anelli risultanti a cinque, sei, sette atomi si possono utilizzare in ulteriori reazioni sintetiche.
Si è dimostrato che la reazione di Demjanov è sensibile a regioselettività. Un esempio di questo fatto è uno studio condotto da D. Fattori che ha osservato la regioselettività del riarrangiamento di Demjanov negli ingrandimenti degli anelli ad un carbonio in certi zuccheri.[5]
Dimostrò che quando una metilammina "exo" subisce la deamminazione dell'acido nitroso secondo Demjanov, non viene prodotto l'ingrandimento dell'anello.
Tuttavia, quando la metilammina endo subisce la reazione nelle stesse condizioni, viene prodotto un mistro di alcool riarrangiati.
Problemi[modifica | modifica wikitesto]
Questo riarrangiamento porta anche a un sottoprodotto sostituito, ma non espanso. Dunque può essere difficoltoso isolare i due prodotti ed ottenere la resa voluta. Inoltre, vengono prodotti stereoisomeri in base alla direzione di addizione della molecola d'acqua e possono essere prodotte altre molecole in base a quali riarrangiamenti avvengono.
Applicazioni future[modifica | modifica wikitesto]
La ricerca attuale esplora le possibilità dell'utilizzo di vari gruppi direttori per influenzare la selettività dei prodotti, come lo stagno o il silicone.[6] Ciò potrebbe portare a un maggiore successo della reazione di Demjanov, potendo consentire un maggiore controllo nella reazione e un aumento nella resa del prodotto desiderata. Tale riarrangiamento è molto utile, ma a volte usarlo può rivelarsi inefficace dalla difficoltà di creare il prodotto preferito. Quindi se vi sono più gruppi direttori possibili, ciò migliorerebbe notevolmente l'applicabilità del processo Demjanov.
Variazioni[modifica | modifica wikitesto]
Riarrangiamento di Tiffeneau-Demjanov[modifica | modifica wikitesto]
The Tiffeneau-Demjanov rearrangement (after Marc Tiffeneau and Nikolai Demjanov) is a variation of the Demjanov rearrangement, which involves both a ring expansion and the production of a ketone by using sodium nitrite and hydrogen cation. Using the Tiffeneau-Demjanov reaction is often advantageous as, while there are rearrangements possible in the products, the reactant always undergoes ring enlargement. As in the Demjanov rearrangement, products illustrate regioselectivity in the reaction. Migratory aptitudes of functional groups dictate rearrangement products.
Uso del diazometano[modifica | modifica wikitesto]
Diazomethane also produces ring enlargement, and its reaction is mechanically similar to the Tiffeneau-Demjanov rearrangement.
Note[modifica | modifica wikitesto]
- ^ (RU) Demjanov, N. J.; Lushnikov, M., Products of the action of nitrous acid on tetramethylenylmethylamine, in J. Russ. Phys. Chem., vol. 35, 1903, pp. 26-42.
- ^ (RU) Demjanov, N. J.; Lushnikov, M., Chem. Zentr., vol. 1, 1903, pp. 828.
- ^ (EN) Smith, P. A. S.; Baer, D. R., Org. React., vol. 11, 1960, pp. 157.
- ^ a b (EN) Jack Li, Jie, Name Reactions, 3ª ed., Berlino, Springer, 2006.
- ^ (EN) Fattori, D.; Henry, S.; Vogel, P., The Demjanov and Tiffeneau-Demjanov one-carbon ring enlargements of 2-aminomethyl-7-oxabicyclo[2.2.1]heptane derivatives. The stereo- and regioselective additions of 8-oxabicyclo[3.2.1]oct-6-en-2-one to soft electrophiles, in Tetrahedron, vol. 49, n. 8, 1993, pp. 1649–1664, DOI:10.1016/S0040-4020(01)80352-5.
- ^ (EN) Chow, L; McClure, M; White, J., Silicon and tin-directed Tiffeneau-Demjanov reaction, in Org. Biomol. Chem., vol. 2, n. 5, 2004, pp. 648–50, DOI:10.1039/b314923d, PMID 14985802.
Bibliografia[modifica | modifica wikitesto]
- ^ Ring expansions. I. Diazomethane and Tiffeneau-Demjanov ring expansions of norcamphor and dehydronorcamphor, in J. Org. Chem., vol. 38, n. 23, 1973, p. 4059, DOI:10.1021/jo00987a023.
- ^ Kotani, R., Demjanov Rearrangement of Methylcyclohexanemethylamine, in J. Org. Chem., vol. 30, n. 2, 1965, p. 350, DOI:10.1021/jo01013a009.
- ^ Hexahydro-1-methyl-4-phenyl-4-acetoxyazepine and the Demjanov Rearrangement of 1-Methyl-4-phenylpiperidine-4-methylamine*, in J. Org. Chem., vol. 30, n. 6, 1965, p. 1840, DOI:10.1021/jo01017a030.
- ^ Unusual consecutive rearrangements in the Demjanov ring-expansion reaction of 2-(aminomethyl)-D2d-dinoradamantane and 9-(aminomethyl)noradamantane, in J. Org. Chem., vol. 48, n. 13, 1985, p. 2289, DOI:10.1021/jo00161a033.
- ^ Steroids and steroidases—XIX: Comparison of diazomethane and tiffeneau-demjanov homologations of 5α-3-oxosteroids. Evidence for predominant equatorial approach of the C-3 carbonyl group by diazomethane, in Tetrahedron, vol. 29, n. 14, 1973, pp. 1941–1947, DOI:10.1016/0040-4020(73)80128-0.
- ^ Synthesis of brexan-2-one and ring-expanded congeners, in J. Org. Chem., vol. 57, n. 20, 1992, p. 5432, DOI:10.1021/jo00046a015.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]


