Siliciuro di platino
| Siliciuro di platino | |
|---|---|
 | |
| Nome IUPAC | |
| Siliciuro di platino | |
| Caratteristiche generali | |
| Formula bruta o molecolare | PtSi |
| Massa molecolare (u) | 223,17 g/mol |
| Numero CAS | |
| PubChem | 9859339 |
| SMILES | [Si].[Pt] |
| Proprietà chimico-fisiche | |
| Densità (g/l, in c.s.) | 12400 g/cm3[1] |
| Temperatura di fusione | 1229[1] |
| Indicazioni di sicurezza | |
| Punto di fiamma | non infiammabile |
Il siliciuro di platino, noto anche come monosiliciuro di platino, è un composto inorganico del platino e del silicio con formula PtSi. È un semiconduttore che si trasforma in un superconduttore quando viene raffreddato a 0,8 K[2].
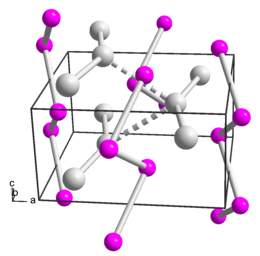
Struttura[modifica | modifica wikitesto]
La struttura cristallina del siliciuro di platino è ortorombica, con ciascun atomo di silicio avente sei atomi di platino vicini. Il suo gruppo spaziale è Pnma (gruppo n°62), il suo simbolo di Pearson è oP8. Le costanti di reticolo sono: , e . Le distanze tra il silicio e i vicini di platino sono le seguenti: uno a una distanza di 2,41 Å, due a una distanza di 2,43 Å, uno a una distanza di 2,52 Å e gli ultimi due a una distanza di 2,64 Å. Ogni atomo di platino ha sei vicini di silicio alle stesse distanze, così come due vicini di platino, a una distanza di 2,87 e 2,90 Å. Tutte le distanze superiori a 2,50 Å sono considerate troppo lontane per essere realmente coinvolte nelle interazioni di legame del composto. Di conseguenza, è stato dimostrato che due serie di legami covalenti compongono i legami che formano il composto. Un insieme è costituito dai tre legami centrali Pt-Si-Pt e l'altro è costituito dai due legami centrali Pt-Si. Il film più sottile di siliciuro di platino sarebbe costituito da due piani alternati di atomi, un unico foglio di strutture ortorombiche; strati più spessi sono formati impilando coppie di fogli alternati. Il meccanismo di legame nel siliciuro di platino è più simile a quello del silicio puro rispetto al platino puro, sebbene la sperimentazione abbia rivelato il carattere di legame metallico nel siliciuro di platino che manca al silicio puro[3].
Sintesi[modifica | modifica wikitesto]
Metodi[modifica | modifica wikitesto]
Il siliciuro di platino può essere sintetizzato in diversi modi. Il metodo standard prevede la deposizione di un sottile film di platino puro su wafer di silicio e il riscaldamento in un forno convenzionale a 450-600 °C per mezz'ora in ambienti inerti. Il processo non può essere eseguito in un ambiente ossigenato, poiché ciò comporterebbe la formazione di uno strato di ossido sul silicio, impedendo la formazione di siliciuro di platino[4]. Una tecnica secondaria per la sintesi richiede un film di platino spruzzato depositato su un substrato di silicio; a causa della facilità con cui il siliciuro di platino può essere contaminato dall'ossigeno, sono state riportate diverse varianti dei metodi. È stato dimostrato che il trattamento termico rapido aumenta la purezza degli strati di siliciuro di platino formati[5]. Anche temperature più basse (200–450 °C) hanno avuto successo[6]; temperature più alte producono strati di siliciuro di platino più spessi, sebbene temperature superiori a 950 °C abbiano formato siliciuro di platino con una maggiore resistività a causa di grappoli di grandi grani di siliciuro di platino[7]
Formazione[modifica | modifica wikitesto]
Indipendentemente dal metodo di sintesi impiegato, il siliciuro di platino si forma allo stesso modo. Quando il platino puro viene prima riscaldato con silicio, si forma inizialmente Pt2Si. Una volta utilizzati tutti gli atomi di platino e di silicio disponibili e le uniche superfici disponibili sono Pt2Si, il siliciuro inizierà la reazione più lenta di conversione in siliciuro di platino. L'energia di attivazione per la reazione Pt2Si è di circa 1,38 eV, mentre è di 1,67 eV per il siliciuro di platino.
L'ossigeno è estremamente dannoso per la reazione, poiché si legherà preferibilmente al platino, limitando i siti disponibili per il legame Pt-Si e prevenendo la formazione di siliciuro. Si è scoperto che una pressione parziale bassa di ossigeno a 10-7 è sufficiente per rallentare la formazione del siliciuro. Per evitare questo problema vengono utilizzati ambienti inerti, nonché piccole camere di ricottura per ridurre al minimo la quantità di potenziali contaminazioni[4]. Anche la pulizia del film metallico è estremamente importante e le condizioni di sporcizia determinano una scarsa sintesi di siliciuro di platino[6].
In alcuni casi uno strato di ossido può essere utile. Quando il siliciuro di platino viene utilizzato come barriera Schottky, uno strato di ossido previene l'usura del siliciuro di platino[4].
Applicazioni[modifica | modifica wikitesto]
Il siliciuro di platino è un semiconduttore e può essere utilizzata una barriera Schottky con elevata stabilità e buona sensibilità nel rilevamento a infrarossi, nelle immagini termiche o nei contatti ohmici e Schottky[8]. Il siliciuro di platino è stato ampiamente studiato e utilizzato negli anni '80 e '90, ma è diventato meno comunemente usato, a causa della sua bassa efficienza quantica. Il siliciuro di platino è ora più comunemente usato nei rivelatori a infrarossi, a causa delle grandi dimensioni delle lunghezze d'onda che può essere utilizzato per rilevatori[9]. È stato utilizzato anche nei rivelatori per l'astronomia a infrarossi. Può funzionare con buona stabilità fino a 0,05 °C. Il basso costo e la stabilità lo rendono adatto per la manutenzione preventiva e l'imaging IR scientifico.
Note[modifica | modifica wikitesto]
- ^ a b (EN) Haynes, William M., CRC Handbook of Chemistry and Physics, 97ª ed., CRC Press, 2016, p. 4.79, ISBN 978-14-98-75429-3.
- ^ (EN) Haynes, William M., CRC Handbook of Chemistry and Physics, 97ª ed., CRC Press, 2016, p. 12.68, ISBN 978-14-98-75429-3.
- ^ (EN) J.E. Kelpeis, O. Beckstein, O. Pankratoc e G.L.W. Hart, Chemical bonding, elasticity, and valence force field models: A case study for α−Pt2Si and Pt'Si, in Physical Review B, vol. 64, n. 15, 2001, DOI:10.1103/PhysRevB.64.155110.
- ^ a b c (EN) A.K. Pant, S.P. Muraka, C. Shepard e W. Lanford, Kinetics of platinum silicide formation during rapid thermal processing, in Journal of Applied Physics, vol. 72, n. 5, 1992, pp. 1833–1836, DOI:10.1063/1.351654.
- ^ (EN) A.A. Naem, Platinum silicide formation using rapid thermal processing, in Journal of Applied Physics, vol. 64, n. 8, 1988, pp. 4161–4167, DOI:10.1063/1.341329.
- ^ a b (EN) C.A. Crider, J.M. Poate, J.E. Rowe e T.T. Sheng, Platinum silicide formation under vacuum and controlled impurity ambients, in Journal of Applied Physics, vol. 52, n. 4, 1981, pp. 2860–2868, DOI:10.1063/1.329018.
- ^ (EN) The properties of this platinum silicide films, in Platinum Metals Review, vol. 20, n. 1, 1976, p. 9.
- ^ (EN) Platinum Silicide (PtSi) Semiconductors, su AZO Materials. URL consultato il 28 aprile 2014 (archiviato dall'url originale il 22 dicembre 2014).
- ^ (EN) H.M. Del Castillo; Gunapala, S.D.; Jones, E.W.; Lin, T., Long wavelength PTSI infrared detectors and method of fabrication therof., US5648297A (15 luglio 1997).


