Implantologia iuxtaossea
Gli impianti iuxtaossei o sottoperiostei, (in inglese subperiosteal implants) sono stati introdotti nel 1941 da Gustav Dahl e rivisitati nel 1946 da Norman Goldberg e Aaron Gerschkoff e sono i dispositivi chirurgici impiegati nell'implantologia iuxtaossea o sottoperiostale (subperiosteal implantology).
Studi scientifici, indicazioni, tecniche alternative[modifica | modifica wikitesto]
In seguito numerosi autori tra cui Linkow LI[1][2][3][4], Cranin AN[5][6][7][8][9], Weiss CM[10][11], Bodine RL, Yanase RT (2), Bodine A[12], Chanavaz M., Maurice James Fagan, Robert A. James[13][14], Marziani[15], E. Belotti[16] hanno contribuito all'evoluzione della tecnica con miglioramenti nel disegno[5][17][18], nello studio dell'interfaccia osso-impianto[11][19], agli aspetti microbiologici[20], all'attacco epiteliale[21][22][23] e agli studi statistici[16][24].

Gli impianti sono stati validati per efficacia, sicurezza e sopravvivenza da numerosi studi longitudinali, prospettici e retrospettivi, long term follow up[25][26][27][28][29][30][31].
Lo studio retrospettivo più rilevante è stato effettuato da Moore e Hansen in un'analisi temporale di 18 anni[32].
Lo studio prospettico più significativo è stato eseguito da Bodine, Yanase, Bodine[33] con un'investigazione di 41 anni[24].
Lo iuxta-osseo, tra le tecniche disponibili e indicate per il trattamento delle atrofie avanzate a carico immediato (Cawood and Howell class VI), è l’impianto che beneficia del più lungo studio prospettico.
-
Analisi di sopravvivenza nello studio di Moore et coll.
-
Analisi di sopravvivenza nello studio di Yanase et coll.
Questi impianti sono indicati per il trattamento con carico immediato delle atrofie gravi e avanzate dell'osso[10] sia totali sia parziali e sono alternativi o prioritari alle procedure di innesti inlay onlay con prelievo dalla teca cranica o dalla cresta iliaca, all'osteotomia di Lefort 1 [34] con innesto interposizionale, agli impianti zigomatici intra-extra sinusali (Quad /Hibrid Zygoma).
Le complicazioni, gli effetti avversi, i rischi, l'invalidità temporanea di alcune metodiche, un’attesa temporale eccessiva per la finalizzazione del lavoro devono far riflettere sull'uso indiscriminato di procedure più invasive e pericolose.
L'osteotomia di Lefort 1 (maxillary downfracture) con innesto interposizionale, anche se predicibile[35], non ha ottenuto un'adeguata accettazione dai pazienti (costi/ospedalizzazione/tempi di guarigione); è indicata nelle gravi atrofie ossee post-oncologiche e post-traumatiche; non ha un rapporto rischio-beneficio favorevole.
Gli innesti ossei (inlay grafting e lateral and vertical onlay grafting) hanno una predicibilità confermata dal maggior numero di studi statistici nei pazienti non fumatori ma limitata a 10 anni[36].
Gli impianti zigomatici (approccio sinusale/extra sinusale) richiedono un'appropriata selezione; condizioni preesistenti di patologia sinusale devono essere preventivamente corrette FESS.
Aparicio et coll. descrive uno studio long term [37] a 10 anni di 41 impianti zigomatici. Sei pazienti hanno sofferto di sinusite nel periodo post-operatorio (14 e 127 mesi); otto pazienti hanno sperimentato un'ostruzione osteomeatale (due bilateralmente); a due pazienti è stata diagnosticata una sinusite.
I due approcci (sinusale ed extra-sinusale) sono indicati nelle emi-maxillectomie, nel trattamento del deficit osseo mascellare esito di resezioni post-oncologiche, nei traumi e nei difetti congeniti non adeguatamente trattati (singolo impianto, Quad e Hibrid Zygoma).
Sono possibili serie complicazioni [38] come l'invasione della fossa infra-temporale o la fossa pterigopalatina, la necrosi asettica dello zigomo, e complicazioni meno gravi: fistola oro-antrale, una sinusite persistente che non si risolve con la sola rimozione dell'impianto, ma richiede un'antrotomia.[39]
L'impianto iuxta-osseo non ha controindicazioni di tipo anatomico e sistemico; la morbilità e la co-morbilità che può causare il fallimento delle attuali tecniche non influisce sulla prognosi e il decorso dell'impianto; la tecnica è di elezione se non si può o non si deve coinvolgere il seno mascellare.
Con questo metodo si possono trattare i fallimenti degli innesti e degli impianti zigomatici; questi impianti sono adatti per pazienti con patologia sinusale causata dagli impianti stessi o dovuta alla mancanza di pervietà osteo-meatale; il fumo, il diabete mellito di primo e secondo tipo, l'osteoporosi, l'osteomalacia non influenzano sensibilmente il decorso.
Il paziente disabile, geriatrico o semplicemente il paziente che ha un'atrofia severa della mascella e della mandibola e che non può compromettere neanche per un giorno la sua vita di relazione, in un solo giorno di trattamento può ripristinare la funzione masticatoria ed estetica.
L'impianto non è inserito nell'osso ma sopra l'osso in stretto contatto e bloccato dalla presenza di sotto-squadri ossei; la stabilità del dispositivo impedisce la formazione di tessuto fibroso.
L’impianto iuxta-osseo non è un impianto standard ma custom–made, ossia progettato e costruito per ogni singolo paziente sulla base del proprio osso basale.
È una tecnica indicata per il trattamento delle severe atrofie parziali o totali (full-arch) della mascella e della mandibola.
L'impianto iuxta-osseo parziale superiore con o senza estensione pterigoidea è alternativo agli impianti zigomatici, pterigoidei, tuberositari, al sinus lifting se la disponibilità ossea è inferiore ai 4 mm e se esistono controindicazioni locali o rischi nella procedura (sinusite/fistola oro-antrale/malattia sinusale/mancanza di pervietà del complesso osteo-meatale, rino-sinusite allergica); la tecnica iuxta-ossea parziale consente un reintervento se le altre procedure sono fallite.
L'impianto iuxta-osseo parziale inferiore è indicato per l'osso basale inferiore e/o in sostituzione degli short-implants (4/6 mm) laddove le tecniche rigenerative non sono predicibili e gravate da rilevanti fallimenti nel breve-medio periodo.
Gli impianti iuxta-ossei parziali sono indicati solo per la sostituzione di un'area edentula riassorbita di almeno 3 elementi dentali.
Se precedentemente la tecnica era adottata solo da operatori molto esperti, la tecnologia digitale ha contribuito a semplificare la procedura e a renderla maggiormente fruibile.
Sulla base di un modello analogico o digitale dell'osso basale, l’esperto programma un disegno (analogico o digitale) rispettando le sedi anatomiche non soggette a ulteriore riassorbimento; la pianificazione del progetto consente la realizzazione del dispositivo in fusione o in printing 3-D (laser-melting).
Il cromo-cobalto-molibdeno (vitallium), il titanio[40] c.p (grado 4) e le leghe beta e alfa/beta in titanio (titanio-niobio/vanadio-alluminio) sono i materiali maggiormente testati per la loro biocompatibilità e per la resistenza ai carichi compressivi e tensili di punta e ciclici.
Il metallo fuso è sottoposto a pulizia, decapaggio e sabbiatura secondo gli standard A.S.T.M o ISO.
Il metallo può essere rivestito da un coating; tra i rivestimenti maggiormente testati sono da segnalare l’idrossiapatite[41][42] e il plasma spray.
Sono stati testati due metodi: metodo in due fasi che prevede l’impronta diretta dell’osso in una sessione chirurgica dedicata; metodo in una singola fase dove la superficie ossea non è ricavata da un'esposizione chirurgica, ma da una ricostruzione in 3d ottenuta dalla TAC multislice.
Metodo in una fase (one phase)[modifica | modifica wikitesto]
Dalla realizzazione di una TAC multistrato, eseguita sulla scorta di specifici parametri, si ottiene un modello virtuale stampabile in 3d (stereolitografia); sul modello anatomico ottenuto dalla stampa si progetta il disegno e le informazioni qualitative e quantitative sono inviate all’odontotecnico per la fusione.
Il processo si adatta alle seguenti fasi:
1) TAC multistrato; 2) modello virtuale in 3d; 3) modello anatomico realizzato in 3d printing; 4) disegno analogico; 5) fusione con controllo radiologico delle micro-porosità[43][44][45][46][7].
Attualmente la TAC volumetrica non consente una segmentazione precisa e affidabile discriminando accuratamente tessuti molli e tessuti duri; gli artefatti metallici, se presente metallo di origine protesica o da innesto artificiale, complicano esponenzialmente il problema.
È in corso la valutazione della realizzazione in totale flusso digitale (modello virtuale; disegno al cad, informazione mediante file stl al processo produttivo in laser melting[47][13][48]).
La prototipazione in laser melting è seguita da un trattamento termico distensivo in forno.
-
Atrofia pre-operatoria
-
Modello litografico ottenuto dalla C.T. multislice ( (Cawood and Howell class VI)
-
Chirurgia in una sola sessione (one phase)
-
Chirurgia in una sola sessione (one phase)
-
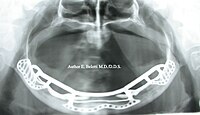
opt post-operatoria a 10 anni
-
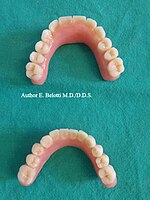
Finalizzazione protesica
Metodo in due fasi (two phase)[modifica | modifica wikitesto]
In un primo intervento, eseguito in anestesia locale o sedo-analgesia, si scheletrizza il mascellare superiore e/o inferiore evitando lesioni al periostio fino all'esposizione delle superfici ossee non riassorbibili; si prende un'impronta con materiale siliconico che consente la realizzazione di un modello anatomico in resina o gesso.
Sul modello si progetta il disegno della struttura e le informazioni qualitative e quantitative vengono inviate all'odontotecnico per la fusione.
In un secondo tempo operatorio (in genere alla terza settimana) è collocato il dispositivo.
Le tecniche hanno entrambe una validità metodologica.
La tecnica one phase, eseguita per l'atrofia della mascella e della mandibola, permette con estrema facilità il raggiungimento di alcune sedi difficilmente esplorabili dall'impronta.
L’impronta dell’osso basale nelle indicazioni del sottoperiosteo parziale è equivalente o superiore in precisione rispetto al modello virtuale ottenuto dalla tac multislice se il processo che conduce al suo ottenimento non è effettuato a regola d'arte.
L’obbiettivo principale del trattamento è la precisione del contatto osseo del dispositivo sulla superficie ossea e la sua stabilità primaria immediata: il disegno deve consentire inoltre che questa stabilità si mantenga nel tempo quando l'impianto verrà caricato e sottoposto alle forze masticatorie.
La stabilità del dispositivo si raggiunge grazie al superamento dei sottosquadri ossei che devono essere pianificati in fase di progettazione; il metallo deve consentire una discreta elasticità e una discreta memoria elastica; in genere non sono necessarie viti di osteosintesi sebbene un loro uso limitato e razionale (se vi sono le condizioni per un adeguato sostegno evitando la penetrazione nei seni paranasali) può contribuire a rendere più stabile il dispositivo.
La precaria stabilità ottenuta dall’uso esclusivo delle viti di osteo-sintesi genera uno sforzo di picco con osteolisi successiva nel punto di applicazione; questa stabilità illusoria impedirebbe anche il microadattamento al letto osseo dell’impianto sotto carico. La congruenza di accoppiamento della superficie osso/metallo è il risultato della corretta investigazione (radiologica/digitale), dell'ottenimento di un modello virtuale e/o fisico di elevata accuratezza a partire dalle immagini tomografiche, dell'applicazione rigorosa delle procedure cliniche e dell'attendibilità del processo costruttivo che riproduce fisicamente il progetto effettuato; la fissazione del dispositivo con l'applicazione delle sole viti di osteosintesi è un cattivo esempio di esecuzione della tecnica.
Nella fase di posizionamento non ci dovrebbero essere spazi morti e l’inserimento di viti ridondanti al fine di compensare il disaccoppiamento potrebbe generare una tensione pericolosa della struttura.
L’impianto iuxta-osseo è caricato immediatamente con un provvisorio fisso che deve rimanere per circa 4 mesi in attesa che il letto periostale (fibre di sharpey) lo ancori definitivamente all'osso.
In seguito sono consentite protesi in acrilico o composito che minimizzano lo stress all’interfaccia osso-impianto.
Una protesi eccessivamente rigida può determinare uno stress-shielding con riassorbimento da ipo-funzione.
Sono consigliare protesi rimovibili (overdenture) con attacchi a clips, a sfera, a chiavistelli e/o meso-strutture in peek (polietereterchetone) ma in taluni casi la protesi (specialmente per i sottoperiostei parziali) può essere fissa cementata o avvitata.
-
iuxta-osseo parziale; il dispositivo è stato realizzato dall'impronta siliconica dell'osso (two phase); si noti il sensibile accoppiamento metallo-osso. La precisione del contato è un criterio di successo della metodica
-
Meso-struttura a clips
-
overdenture
Nel post sono necessari controlli frequenti per la gestione delle forze masticatorie e per la verifica del mantenimento dei contatti e della stabilità occlusale.
La sopravvivenza dell'impianto è legata alla rigorosità nell'applicazione delle procedure investigative, progettuali, cliniche e costruttive, alle conoscenze e all'esperienza dell’operatore; moltissimi casi hanno avuto esito favorevole a distanza di 30/40 anni[49] dall'intervento; per le gravi atrofie [50] dell’osso mandibolare (mandibola a grissino) l’impianto sottoperiostale tripodiale rappresenta la migliore soluzione[51]in termini di sopravvivenza ed efficacia[52][53][54][55].
-
atrofia pre-operatoria
-
impronta in silicone sull'osso; permette la riproduzione fedele del modello anatomico (two phase)
-
Progettazione del dispositivo sul modello in gesso
-
fusione in titanio lega beta
-
Secondo tempo chirurgico (two phase); l'esposizione chirurgica che consente l'inserimento dell'impianto iuxta-osseo
Complicazioni e modalità di trattamento[modifica | modifica wikitesto]
Sono esigue le complicazioni segnalate; le complicazioni statisticamente più rilevanti sono a carico dei tessuti molli.
Un eccessivo spazio morto tra il metallo e l'osso si riempie di tessuto fibroso. Con il passare del tempo il tessuto fibroso può rimanere tale o declinare verso la formazione di tessuto infiammatorio ricco di vasi sanguigni.
Il problema può essere corretto con l'amputazione di una parte della struttura, un debridement e un consensuale graft (innesto osseo omologo, eterologo).
Se per qualche ragione l’impianto si mobilizza significa che al contatto osso-impianto si è interposto un eccesso di tessuto fibroso; in queste condizioni il monitoraggio deve essere intensivo e non si può escludere la rimozione del dispositivo stesso.
Un'esposizione non ha significato clinico se è causata dalla recessione dei tessuti molli; se l'esposizione è invece determinata dal riassorbimento osseo crestale lo spazio morto può infettarsi con progressiva colonizzazione batterica anaerobica del metallo.
Complicazioni inusuali descritte in letteratura o segnalate da report come osteite[56], cellulite, sfondamento nei seni paranasali, comunicazione e fistola oro-antrale sono l'espressione di training inadeguato, inesperienza dell'operatore, inadeguatezza della tecnica o astensione dalla sorveglianza.
L'esatta interpretazione del fallimento può essere individuata solo da operatori esperti e riconosciuti con un lungo training dimostrabile.
La composizione del microbioma a livello della sottomucosa perimplantare potrebbe essere determinante nella sopravvivenza a lungo termine[57].
Non è ancora chiaro se la misura quantitativa del sondaggio peri-monconale o la perdita di attacco possa essere un criterio di orientamento sull'evoluzione non favorevole dell'impianto.
La sopravvivenza e il successo della tecnica sono legate al monitoraggio continuo con cadenza semestrale che si deve estendere al periodo di vita del portatore.
Interfaccia osso-impianto[modifica | modifica wikitesto]
L'impianto iuxta-osseo può giustapporsi all'osso in 4 modalità:
- contatto osseo diretto e trattenuto a esso dalle fibre di sharpey[58]
- contatto fibroso (fibre di collagene senza infiammazione e infezione[58]
- può essere integrato [59] (incluso) nell'osso[19]
- imbustato nel periostio profondo e trattenuto dalle fibre di sharpey[11]
Clinicamente nessuna modalità si è dimostrata superiore ad un'altra; ciò che importa è che l'impianto mantenga la sua stabilità senza segni di sofferenza e infiammazione.
Note[modifica | modifica wikitesto]
- ^ Three year progress report on the pterygoid extension implant for the totally and partially, edentulous maxillae. Linkow LI, Mahler MS. Quintessence Int Dent Dig. 1976 Jan.
- ^ Maxillary pterygoid extension implants: the state of the art. Linkow LI. Dent Clin North Am. 1980.
- ^ Evolutionary design trends in the mandibular subperiosteal implant. Linkow LI. J Oral Implantol. 1984;11(3):402-38..
- ^ linkowlibrary.org, http://www.linkowlibrary.org/books.
- ^ a b The unilateral pterygohamular subperiosteal implant: evolution of a technique. Cranin AN, Satler N, Shpuntoff R. J Am Dent Assoc. 1985 Apr;110(4):496-500.
- ^ Case report using scanning electron microscopy and EDAX (Energy-dispersive Analysis of X-rays) to study the tissue surrounding a subperiosteal implant after repeated surgery. Whittaker JM, Cranin AN, James RA. J Oral Implantol. 1989;15(2).
- ^ a b An in vitro comparison of the computerized tomography/CAD-CAM and direct bone impression techniques for subperiosteal implant model generation. Cranin AN, Klein M, Ley JP, Andrews J, DiGregorio R. J Oral Implantol. 1998;24(2):74-9.
- ^ Atlas of Oral Implantology A. Norman Cranin et coll.
- ^ Posterior region maxilla: a proven implant alternative. Cranin A.N. Dent Implantol Update. 1992.
- ^ a b Severe mandibular atrophy--biological considerations of routine treatment with the complete subperiosteal implant. Weiss CM, Judy KW. Oral Implantol. 1974 Spring;4(4):431-69.
- ^ a b c Principles and Practice of Implant Dentistry Charles Weiss Adam Weiss.
- ^ Forty years of experience with subperiosteal implant dentures in 41 edentulous patients. Bodine RL, Yanase RT, Bodine A J Prosthet Dent. 1996 Jan;75(1):33-44..
- ^ a b CT SCAN CAD/CAM SUBPERIOSTEAL IMPLANT DDS, MS ROBERT A. JAMES First published: February 1994.
- ^ CT scan CAD/CAM subperiosteal implant. James RA. Aust Dent J. 1994 Feb;39(1):56; author reply 56-7.
- ^ Treatise of Implant Dentistry: The Italian Tribute to Modern Implantology. M .Pasqualini et coll.
- ^ a b Enrico Belotti et coll., Impianti endo-ossei a lama e impianti sotto-periostei, in Attualità Dentale, n. 39, 13 dicembre 1992.
- ^ A newly designed partial subperiosteal implant and the classical design: a comparative study. P R Health Sci J. 1994 Sep;13(3):183-90. Whittaker JM, James RA, Lozada J, Cordova C, Freidline.
- ^ Placement of a modified subperiosteal implant: a clinical solution to help those with no bone. Nazarian A. Dent Today. 2014 Jul;33(7):134, 136-7..
- ^ a b The Custom Endosteal Implant: histology and case report of a retrieved maxillary custom osseous-integrated implant nine years in service.Nordquist WD, Krutchkoff DJ. J Oral Implantol. 2014 Apr;40(2):195-2018..
- ^ Microbiological aspects of human mandibular subperiosteal dental implants.Rams TE1, Balkin BE, Roberts TW, Molzan AK.J Oral Implantol. 2013 Dec;39(6):714-22.
- ^ Epithelial attachment and subperiosteal implants Stvrtecky RO, Zarate JO, Borgetti ZARev Asoc Odontol Argent. 1991 Apr-Jun;79(2):110-3. Spanish..
- ^ Clinical study of peri-abutment gingiva in patients with subperiosteal implants Matas Naranjo R, Dreyer Arroyo E, Vicent Vazquez R, Matas Colom J Rev Dent Chile. 1991 Apr;82(1):10-6. Spanish..
- ^ Suspension mechanism of subperiosteal implants in baboons.Whittaker JM, James RA, Lozada J, Cordova C, Freidline C.J Oral Implantol. 1990;16(3):190-7..
- ^ a b Forty years of experience with subperiosteal implant dentures in 41 edentulous patients.Bodine RL, Yanase RT, Bodine A J Prosthet Dent. 1996 Jan;75(1):33-44..
- ^ A twenty-year evaluation of subperiosteal implants. Young L Jr, Michel JD, Moore DJ. J Prosthet Dent. 1983 May;49(5):690-4..
- ^ Subperiosteal implant technology: report from Rumania. J Oral Implantol. 2003;29(4):189-94. Sirbu I1.
- ^ The mandibular subperiosteal implant denture: a prospective survival study. Amet EM. J Prosthet Dent. 1996 Mar;75(3):347-8. No abstract available..
- ^ Subperiosteal implants: success and longevity. Implant Soc. 1992;3(2):5-6. Levi E, Wilder L..
- ^ A collective conference on the utilization of subperiosteal implants in implant dentistry Weiss CM, Reynolds J Oral Implantol. 2000;26(2):127-8..
- ^ Long-term clinical experience and statistical analysis of CAT scan subperiosteal implants at Loma Linda University. Lozada JL. J Oral Implantol. 1996;22(1).
- ^ Long-term retrospective studies on the CT-scan, CAD/CAM, one-stage surgery hydroxyapatite-coated subperiosteal implants, including human functional retrievals. Benjamin LS. Dent Clin North Am. 1992 Jan;36(1):77-93; discussion 94-5..
- ^ A descriptive 18-year retrospective review of subperiosteal implants for patients with severely atrophied edentulous mandibles. Moore DJ, Hansen PA. J Prosthet Dent. 2004 Aug;92(2):145-50., https://www.ncbi.nlm.nih.gov/pubmed/15295323.
- ^ Bodine RL, Yanase RT, Bodine A
- ^ Osteotomia di Lefort 1 (PDF), su pdfs.semanticscholar.org. URL consultato l'11 settembre 2018 (archiviato dall'url originale il 16 settembre 2018).
- ^ Implant Rehabilitation for Extremely Atrophic Maxillae (Cawood Type VI) with Le Fort I Downgrafting and Autogenous Iliac Block Grafts: A 4-year Follow-up Study Varol A, Atali O, Sipahi A, Basa S. Int J Oral Maxillofac Implants. 2016 Nov-Dec;31(6):1415-22. doi: 10.11607/jomi.4740. Varol A, Atali O, Sipahi A, Basa S..
- ^ The rehabilitation of the severely resorbed maxilla by simultaneous placement of autogenous bone grafts and implants: a 10-year evaluation. van Steenberghe D, Naert I, Bossuyt M, De Mars G, Calberson L, Ghyselen J, Branemark PI Clin Oral Investig1997 Sep;1(3):102-8.
- ^ Studio long term
- ^ Complicazioni
- ^ joms.org, https://www.joms.org/article/S0278-2391(16)30446-3/pdf.
- ^ Titanium subperiosteal implants.J Oral Implantol. 1989;15(1):29-3 Krmpotic I, Knezevic G. Related Articles.
- ^ A seven-year clinical evaluation of soft-tissue effects of hydroxylapatite-coated vs.uncoated subperiosteal implants Fettig RH, Kay JF J Oral Implantol. 1994;20(1):42-8.
- ^ Analysis of HA-coated subperiosteal implants.Minichetti JC. J Oral Implantol. 2003;29(3):111-6; discussion 117-9..
- ^ A customised digitally engineered solution for fixed dental rehabilitation in severe bone deficiency: A new innovative line extension in implant dentistry. Gellric h NC1, Zimmerer RM2, Spalthoff S1, Jehn P1, Pott PC3, Rana M1, Rahlf B1. J Craniomaxillofac Surg. 2017 Oct;45(10):1632-1638. doi: 10.1016/j.jcms.2017.07.022. Epub 2017 Aug 3..
- ^ The use of laser technology (Er;Cr:YSGG) and stereolithography to aid in the placement of a subperiosteal implant: case study. Kusek ER. J Oral Implantol. 2009;35(1):5-11. doi: 10.1563/1548-1336-35.1.5..
- ^ Application of stereolithography to subperiosteal implant manufacture. McAllister ML. J Oral Implantol. 1998;24(2):89-92..
- ^ Long-term retrospective studies on the CT-scan, CAD/CAM, one-stage surgery hydroxyapatite-coated subperiosteal implants, including human functional retrievals.Benjamin LS. Dent Clin North Am. 1992 Jan;36(1):77-93; discussion 94-5.
- ^ CAD/CAM subperiosteal implants in Australia. Case report Fischer JE. Aust Dent J. 1993 Aug;38(4):261-4..
- ^ CT scan CAD/CAM subperiosteal implant. James RA..
- ^ Kurtzman GM, Schwartz K The subperiosteal implant as a viable long-term treatment modality in the severely atrophied mandible: a patient's 40-year case history. J Oral Implantol 1995;21(1):35-9.
- ^ [1]
- ^ One-step reconstruction of the severely resorbed mandible with onlay bone grafts and endosteal implants. A 5-year follow-up. Vermeeren JI, Wismeijer D, van Waas MA Department of Oral and Maxillofacial Surgery, Ignatius Teaching Hospital Breda, The Netherlands..
- ^ Hinged tripodal subperiosteal implants for severely atrophied mandibles. Linkow LI Dent Today. 1996 Apr;15(4):70, 72-3.
- ^ Tripodal mandibular subperiosteal implant: basic sciences, operational procedures, and clinical data. Linkow LI, Wagner JR, Chanavaz M. J Oral Implantol. 1998;24(1):16-36..
- ^ Tripodial subperiosteal implants. Linkow LI. J Oral Implantol. 1986;12(2):228-46..
- ^ Ramus hinges for excessive movements of the condyles: a new dimension in mandibular tripodal subperiosteal implants. Linkow LI, Ghalili R. J Oral Implantol. 1999;25(1):11-.
- ^ Nguyen TM1, Caruhel JB2, Khonsari RH A subperiosteal maxillary implant causing severe osteolysis. J Stomatol Oral Maxillofac Surg. 2018 Jun 27.
- ^ Microbiological aspects of human mandibular subperiosteal dental implants. Rams TE1, Balkin BE, Roberts TW, Molzan AK. J Oral Implantol. 2013 Dec;39(6):714-22.
- ^ a b Theories and Techniques of Oral Implantology, su linkowlibrary.org.
- ^ [2]
Bibliografia[modifica | modifica wikitesto]
- Treatise of Implant Dentistry: The Italian Tribute to Modern Implantology. M. Pasqualini et coll
- http://www.linkowlibrary.org/books Leonard Linkow LIBRARY LINKOWLIBRARY.ORG
- Principles and Practice of Implant Dentistry Charles Weiss Adam Weiss
- Evolutionary design trends in the mandibular subperiosteal implant. Linkow LI. J Oral Implantol. 1984;11(3):402-3
- The complete maxillary subperiosteal implant: an overview of its evolution. Demirdjan E. J Oral Implantol. 1998;24(4):196-7.
- Severe mandibular atrophy treated with a subperiosteal implant and simultaneous graft with rhBMP-2 and mineralized allograft: a case report. Loperfido C, Mesquida J, Lozada JL. J Oral Implantol. 2014 De
- Titanium subperiosteal implants. J Oral Implantol. 1989;15(1):29-3 Krmpotic I, Knezevic G.
- The subperiosteal implant. Stevenson AR. Aust Dent J. 1993 Oct;38(5):
- The complete mandibular subperiosteal implant: an overview of its evolution. Sconzo J. J Oral Implantol. 1998;24(1):14-5.
- Posterior region maxilla: a proven implant alternative. Cranin AN. Dent Implantol Update. 1992 Nov;3(11):81-4. N
- Circumferential and bilateral subperiosteal implant technique for the atrophic mandible. Byland JH. Mo Dent J. 1994 May-Jun;74(3):42-7.
- Long-term retrospective studies on the CT-scan, CAD/CAM, one-stage surgery hydroxyapatite-coated subperiosteal implants, including human functional retrievals. Benjamin LS. Dent Clin
- North Am. 1992 Jan;36(1):77-93; discussion 94-5.
- The complete mandibular subperiosteal implant: an overview of its evolution. Sconzo J. J Oral Implantol. 1998;24(1):14-5.
- Long-term clinical experience and statistical analysis of CAT scan subperiosteal implants at Loma Linda University. Lozada JL. J Oral Implantol. 1996;22(1)