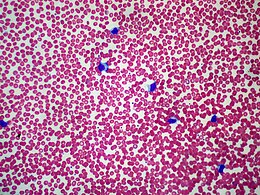
Mononucleosi infettiva
| Mononucleosi infettiva | |
|---|---|
 | |
| Specialità | infettivologia |
| Eziologia | virus di Epstein-Barr e Human betaherpesvirus 5 |
| Classificazione e risorse esterne (EN) | |
| ICD-9-CM | 075075 |
| ICD-10 | B27.027.0 |
| MeSH | D007244 |
| MedlinePlus | 000591 |
| eMedicine | 784513, 222040 e 963894 |
| Sinonimi | |
| Malattia del bacio Angina monocitica Linfomonocitosi adenopatica infettiva Febbre ghiandolare | |
La mononucleosi infettiva (detta anche semplicemente mononucleosi o malattia del bacio, per la sua trasmissibilità attraverso la saliva) è una malattia infettiva virale molto contagiosa causata dal virus di Epstein-Barr (EBV). Le cellule bersaglio del virus sono i linfociti B e il decorso è acuto, solitamente di 4-6 settimane.
La denominazione della malattia è dovuta alla caratteristica presenza nel sangue, in livelli superiori alla norma, di cellule mononucleate normali (linfociti e monociti) e di cellule mononucleate specifiche.
Storia
[modifica | modifica wikitesto]La mononucleosi infettiva fu riconosciuta e descritta per la prima volta in sei pazienti da E. Larey e Douglas H. Sprunt sul Bulletin of the Johns Hopkins Hospital del 1920 con il titolo
«Mononuclear leukocytosis in reaction to acute infection (infectious mononucleosis).»
«Leucocitosi mononucleare in reazione a infezione acuta (mononucleosi infettiva).»
All'epoca il virus di Epstein-Barr (EBV) non era stato ancora isolato e scoperto, ma già dal 1800 la mononucleosi era stata individuata come una sindrome clinica costituita da febbre, faringite e adenopatia. Il termine febbre ghiandolare fu usato nel 1889 da medici tedeschi, tra cui Emil Pfeiffer;[1] mentre l'associazione tra il virus di EBV e la malattia (mononucleosi infettiva) venne riconosciuta nel 1968 da Diehl V, Henle G, Henle W, Kohn G. del Virus and Genetics Laboratories, The Children's Hospital of Philadelphia, School of Medicine, University of Pennsylvania, Philadelphia.[2]
La relazione del virus di EBV con il linfoma di Burkitt fu trovata in quegli anni dallo stesso gruppo di ricerca in collaborazione con ricercatori del Karolinska Institute Medical School.[3]


Eziologia ed epidemiologia
[modifica | modifica wikitesto]La mononucleosi infettiva è causata dal virus di Epstein-Barr, un virus a DNA a doppia elica appartenente alla famiglia degli Herpesviridae, sottofamiglia Gammaherpesvirinae.
Il virus infetta i tessuti epiteliari orofaringei, provocando faringite e talvolta tosse, e i linfociti B con trasmissione orofaringea. Il contagio può avvenire tramite uno scambio di saliva (da cui il termine popolare malattia del bacio), o indirettamente attraverso oggetti entrati in contatto con la saliva di un soggetto infetto (mani, posate, bicchieri, spazzolini, giocattoli).
Oltre il 90% della popolazione adulta risulta essere sieropositivo per il virus e possiede quindi anticorpi diretti verso antigeni virali.[4] I picchi di infezione sono la prima infanzia nei Paesi in via di sviluppo e l'età adolescenziale, dai 15 ai 25 anni, nei Paesi industrializzati.[4] Il decorso è in genere asintomatico o indistinguibile da quello di una faringite o sindrome influenzale e con sintomi spesso trascurabili. Nell'età giovanile nel 75% dei casi si manifesta la forma classica di mononucleosi;[4] in età adulta è tipica una forma lieve, con febbre, malessere e debolezza.[5]
Latenza, oncogenicità e patogenicità, post remissione
[modifica | modifica wikitesto]Il virus rimane latente nell'ospite anche dopo la guarigione. Nei soggetti infettati l'eliminazione del virus con la saliva continua per circa un anno. Passato questo periodo, l'eliminazione del virus continua in maniera saltuaria per tutta la vita; ciò è dimostrabile attraverso la positività per il virus nel gargarizzato in circa il 15-20% dei casi di soggetti esposti e asintomatici.
Alla presenza dell'EBV sono associati alcuni rari tumori come il cancro della rinofaringe, la variante africana del linfoma di Burkitt,[3] alcuni linfomi non-Hodgkin a cellule B[6] (specie in soggetti immunodepressi) e il linfoma di Hodgkin.[7] In Cina, in particolare nella zona meridionale, il linfoma di Burkitt è il più frequente fra i tumori della testa e del collo.[8]
Su base esclusivamente clinica, osservando la sintomatologia, da alcuni autori è stata ipotizzata una correlazione tra mononucleosi infettiva e rischio di lupus eritematoso sistemico; però è stata apparentemente smentita da uno studio prospettico della durata di 30 anni, condotto in Danimarca e terminato nel 2007.[9] Altri studi hanno evidenziato come nei soggetti affetti da malattie autoimmuni, quali sclerosi sistemica, rettocolite ulcerosa, lo stesso lupus eritematoso sistemico e in misura minore in quelli affetti da artrite reumatoide, sindrome di Sjögren, spondilite anchilosante e la malattia di Crohn, la presenza del virus di Epstein-Barr stimola la formazione di un autoanticorpo[10] che potrebbe contribuire al mantenimento dello stato infiammatorio.

Patogenesi
[modifica | modifica wikitesto]Il virus di Epstein-Barr possiede delle glicoproteine di superficie (gp350 e gp220) in grado di legare un recettore (CR2, CD21) per il complemento espresso in diverse cellule dell'organismo, tra cui i linfociti B e le cellule dell'orofaringe.[11][12][13][14]
Una volta entrato in contatto con i tessuti dell'orofaringe, il virus si propaga nei linfonodi delle catene cervicali, sede di contatto con i linfociti B. Da qui, in seguito a intensa replicazione virale, i virus vengono dismessi nel sangue, liberi o associati ai linfociti B. In fase acuta è dimostrabile la presenza del genoma (in forma episomica) in circa il 20% dei linfociti B, con produzione di un pattern di anticorpi tipici, tra cui patognomonici anticorpi eterofili, responsabili di alcune complicanze e fondamentali per fini diagnostici. Terminata la fase acuta, il DNA di EBV è ancora riscontrabile nelle cellule epiteliali dell'orofaringe e nelle memory cell linfonodali.
Di particolare importanza è la reazione cellulo-mediata nei confronti delle cellule B infettate e guidata dai linfociti T; le cellule reattive tendono ad assumere una particolare morfologia e vengono definiti virociti, o cellule di Downey.[15] I virociti hanno dimensioni e forma variabile e si caratterizzano per un citoplasma schiumoso, vacuolizzato e intensamente basofilo, un nucleo ovalare, talora lobulato o reniforme che presenta irregolari depositi di cromatina densa e, talora, nucleoli.
Forme di patologia simili ma rare e differenziabili sono causate da altri Herpesvirus (CMV, HHV-6), da altre forme virali (Adenovirus, HIV, HAV, Rubivirus), dallo Streptococcus pyogenes e dal Toxoplasma gondii.[16]
Anatomia patologica
[modifica | modifica wikitesto]Oltre alle tipiche alterazioni ematologiche, in corso di mononucleosi infettiva sono frequenti diverse alterazioni, soprattutto a carico di milza e fegato. La milza, ingrandita e palpabile, può presentare segni aspecifici, come emorragie sottocapsulari. Nel fegato possono esserci infiltrati diffusi degli spazi portali, con alterazioni in senso regressivo del parenchima epatico e piccoli infarti parcellari. Inoltre i linfociti possono infiltrare le porzioni periarteriolari di intestino e tessuti sottocutanei. I linfonodi risultano ingrossati in tutto il corpo, specialmente sotto le ascelle, nell'inguine e nella regione cervicale posteriore. L'esame istologico rivela la presenza di linfociti T, spesso tanto prolifici da dar luogo a un quadro morfologicamente simile ai linfomi. La mononucleosi può avere ripercussioni anche sul sistema nervoso centrale, che può presentare edema e, raramente, degenerazione mielinica dei fasci nervosi periferici.



Profilo clinico
[modifica | modifica wikitesto]Sintomi e segni aspecifici come febbre, astenia, malessere e cefalea insorgono in circa il 90% dei casi dai 30 ai 60 giorni dopo l'esposizione nei giovani-adulti e in 10-15 giorni nei bambini.[17] La febbre, talora elevata nei giovani, è sovente il sintomo di esordio.
A questa si associa una faringotonsillite di vario grado, a volte modesta e caratterizzata da solo eritema, a volte grave, con un quadro essudativo o pseudomembranoso che può ricordare l'infezione da Streptococcus pyogenes o addirittura da Corynebacterium diphtheriae; è inoltre presente disfagia e odinofagia. In questo contesto, dopo circa una settimana, possono apparire (30% dei casi) piccole lesioni petecchiali a livello della giunzione tra il palato molle e il palato duro, reperto tipico di mononucleosi infettiva.
La linfoadenopatia, quasi sempre presente, è riscontrabile tipicamente a livello cervicale laterale, sia nelle catene anteriori sia in quelle posteriori. I linfonodi affetti, delle dimensioni di una nocciola o poco più grandi, hanno una consistenza duro-elastica, sono mobili nei piani profondi e superficiali, non si associano ad alterazioni della cute sovrastante e sono intensamente dolenti alla palpazione. Benché le zone cervicali siano le più colpite, la linfoadenopatia può essere apprezzabile a livello di tutte le stazioni linfonodali superficiali, come i siti epitrocleari, ascellari, inguinali e poplitei. Anche le stazioni profonde, qualora indagate, possono mostrarsi ingrossate.
La splenomegalia, dimostrabile in più del 50% dei casi, può associarsi variabilmente a epatomegalia; in circa il 9% può inoltre presentarsi ittero. Un esantema, o più correttamente rash aspecifico, talora rubelliforme, altre volte scarlattiniforme, morbilliforme o urticarioide, si presenta nel 10% dei casi ed è spesso associato a terapia empirica della faringite con penicilline semi-sintetiche, come l'ampicillina.[18]
Un'iperemolisi è evidenziabile nel 3% dei casi e si associa alla presenza di IgM anti eritrociti indagabili con il test di Coombs. Questo tipo di anemia immunoemolitica insorge sovente tra la 3ª e la 4ª settimana, con regressione spontanea dopo circa 2 mesi.[19][20] La stessa patogenesi immunologica è causa di piastrinopenia[21] che tuttavia non si associa a fenomeni emorragici. Altri segni e sintomi associabili sono l'angina tonsillare[22] e meno spesso diarrea[23] e dolori addominali.[24]
Complicanze
[modifica | modifica wikitesto]Gravi complicanze insorgono in circa il 5% dei casi di mononucleosi infettiva.[25][26]
La complicazione grave più frequente è la rottura della milza,[27][28][29][30] a rischio nei casi (circa il 50%) in cui questa sia ingrossata (splenomegalia); tale evento può esitare verso emorragie interne che possono provocare lo stato di shock ipovolemico o la morte del paziente.
Un'anemia emolitica può aggravare il quadro ma è autolimitante e può associarsi a porpora dovuta a piastrinopatia e piastrinopenia.[31][32][33]
La sovrainfezione batterica faringo-tonsillare è invece la complicanza locale più frequente e può essere ben gestita da brevi cicli di antibiotici. È tuttavia importante ricordare che devono essere evitate le penicilline per la comparsa di fenomeni esantematici-urticarioidi;[34][35][36][37] in alternativa è possibile utilizzare brevi cicli di macrolidi come eritromicina o azitromicina.
In circa l'1% dei casi si può manifestare una meningite a liquor limpido, con segni neurologici diffusi o con segni di interessamento cerebellare. Ma in assenza di complicanze le forme virali di meningite hanno prognosi benigna e raramente mostrano reliquati. Talora l'infezione da EBV può complicarsi con una sindrome di Guillain-Barré.[38][39][40][41][42]
In casi eccezionali (meno dell'1%), in particolare in immunodepressi, si può manifestare una pericolosa encefalite.[31][43][44][45]
In alcuni individui, probabilmente predisposti per cause congenite o acquisite che alterano la risposta immunitaria contro il virus, l'infezione primaria non è controllata e il virus di Epstein-Barr continua a replicarsi provocando un'infezione cronica attiva (CAEBV)[46][47][48][49] di cui si conoscono forme molto gravi o severe (SCAEBV).[50][51] Questa sindrome ha avuto diverse definizioni, anche perché si sovrappone con altre non ben definite, come la sindrome da stanchezza cronica e la sindrome da emofagocitosi EBV correlata. Contrariamente a quanto asserito negli anni passati, nei pazienti con CAEBV si segnalano sempre più frequentemente neoplasie linfoidi originate dalle cellule T e dalle cellule NK e non dai linfociti B, come generalmente si osserva nelle malattie linfoproliferative post-trapianto EBV positive. L'EBV in particolare, e anche gli altri agenti infettivi che possono dare quadri simil-mononucleosici (CMV, toxoplasma, virus epatitici, HIV) sono tra le cause riconosciute della sindrome da stanchezza cronica,[52][53][54][55] probabilmente a causa degli squilibri che possono apportare al sistema endocrino; un'intensa debolezza durante la fase acuta della mononucleosi conferisce un maggior rischio di sviluppare poi questa complicanza.
Un'epatite fulminante è molto rara e si manifesta soprattutto in soggetti affetti da gravi immunodeficienze.
Altre rare complicanze sono orchite, miocardite, pericardite, ulcere genitali, neutropenia e polmonite interstiziale. Nei soggetti immunodeficienti la mononucleosi può avere un quadro disseminato caratterizzato da grave decorso iperacuto che spesso causa la morte.
I sintomi della mononucleosi infettiva durano circa un mese; segue un periodo di convalescenza caratterizzata da astenia, di durata variabile e che non deve essere confusa con la sindrome da affaticamento cronico.
Alcuni studi hanno concluso che la mononucleosi è un fattore di rischio per la sclerosi multipla.[56]
Profilo diagnostico
[modifica | modifica wikitesto]Il contesto anamnestico e obiettivo è spesso sufficiente per la diagnosi. Le analisi di routine (emocromo con formula) dimostrano leucocitosi (10 000-20 000 leucociti, talora 50 000, per mm3), con inversione della formula leucocitaria verso la linfo-monocitosi (50-60%). Allo striscio periferico è possibile rilevare le cosiddette "cellule linfomonocitoidi" (plasmacellule attivate) e i virociti, che costituiscono il 10-20% dei leucociti. Può esserci una lieve piastrinopenia, mentre una modesta anemia con reticolocitosi e bassi o assenti valori di aptoglobina è indicativa di emolisi.
La diagnosi si fa attraverso la reazione di Paul-Bunnell, in grado di dimostrare gli anticorpi eterofili presenti in corso di mononucleosi infettiva. Questo test è stato sostituito dal più rapido "monotest" che tuttavia risulta nel 25% dei casi falsamente negativo e in un 10% falsamente positivo, in particolar modo in casi di infezione da rosolia, citomegalovirus, HIV o Herpesviridae, e di malattie autoimmuni come lupus eritematoso sistemico e artrite reumatoide[57]. La sierologia dimostra la presenza di IgM anti-VCA e anti-EA in corso di fase acuta. Questi anticorpi scompaiono con la remissione sintomatologica e lasciano il posto alle IgG anti-VCA e anti-EBNA che rimangono positive per tutta la vita. Nei neonati e bambini piccoli, sono necessari altri tipi di test, come la ricerca del DNA virale nei linfociti B del sangue periferico. La bilirubina e la fosfatasi alcalina sono spesso poco elevate.[58] Le transaminasi possono invece raggiungere valori superiori a 200 UI/L.[59][60][61]
Diagnosi differenziale
[modifica | modifica wikitesto]In tutte le forme similari è negativa la sierologia per anticorpi eterofili da cui l'apposito test, reazione di Paul-Bunnell. La diagnosi differenziale si pone con le seguenti manifestazioni:
- Mononucleosi da Citomegalovirus, in cui è raro il coinvolgimento della faringe e negatività sierologica.
- Toxoplasmosi, con quadro simile ma più blando e con negatività sierologica.
- Leucemia acuta, che tuttavia si associa a manifestazioni emorragiche, a grave anemia e leucopenia e uno striscio periferico a cellularità monomorfa.
- Rosolia, a causa della linfoadenopatia cervicale, dell'astenia e dell'esantema; tuttavia la sierologia distingue i due quadri.
- Difterite
- Epatite
- Faringiti batteriche.
Terapia e prognosi
[modifica | modifica wikitesto]Contro la mononucleosi non vi sono cure specifiche; anche gli antivirali di ultima generazione hanno un'efficacia ancora da dimostrare.[62][63] L'agente responsabile della malattia è un virus, per cui è inadeguato ricorrere agli antibiotici; sono indicati solo nel 10-20% dei casi, quando si associa una sovrainfezione faringotonsillare batterica, e alle penicilline si devono preferire i macrolidi. Il trattamento antibiotico può avere effetti nocivi come reazioni simil-allergiche.[64][65][66] La terapia è il riposo a letto fino alla scomparsa della febbre, associata ad analgesici e antipiretici (FANS) per alleviare le manifestazioni della malattia. Non sono previste restrizioni dietetiche.[34]
È fondamentale evitare attività fisica pesante o potenzialmente traumatizzante per circa due mesi, al fine di scongiurare la rottura della milza; in caso di faringite grave con problemi di respirazione, o piastrinopenia o soppressione midollare, rare complicanze, sono indicati corticosteroidi, come il prednisone.[19][67][68]
Nella maggioranza dei casi, comunque, la malattia decorre in non più di quattro settimane senza complicazioni. Invece in presenza di immunodeficienza la mononucleosi può risultare molto grave e con esiti letali. In ogni caso i sintomi possono persistere per mesi dopo la guarigione.
Nel raro caso cui si manifesti sindrome di Guillain-Barré si deve ricorrere alla terapia immunoglobulinica[69][70] e può essere presa in considerazione la terapia con plasmaferesi per un trattamento di lungo periodo delle complicanze di tipo polineuropatico.[71]
Mortalità
[modifica | modifica wikitesto]Escludendo la rottura della milza, facilmente prevenibile, i rischi di mortalità sono legati essenzialmente a pregressi stati di immunodepressione.[72] I casi di decesso possono essere dovuti a epatite fulminante,[73] miocardite virale[73] e infezioni batteriche opportunistiche[74] successive.
Prevenzione
[modifica | modifica wikitesto]Come per tutte le malattie infettive, la prima forma di prevenzione è l'igiene personale e dei luoghi. Specialmente nel caso di contatto con un malato è fondamentale evitare di condividere stoviglie, cibo, occhiali e utensili. È inoltre raccomandato di evitare di baciare i soggetti affetti anche nei giorni successivi al termine delle manifestazioni cliniche[75].
Note
[modifica | modifica wikitesto]- ^ Infectious Mononucleosis: eMedicine Infectious Diseases, su emedicine.medscape.com. URL consultato il 18 settembre 2010.
- ^ Diehl V, Henle G, Henle W, Kohn G, Demonstration of a herpes group virus in cultures of peripheral leukocytes from patients with infectious mononucleosis, in J. Virol., vol. 2, n. 7, luglio 1968, pp. 663–9, PMC 375671, PMID 4881369.
- ^ a b Klein G, Pearson G, Henle G, Henle W, Diehl V, Niederman JC, Relation between Epstein-- Barr viral and cell membrane immunofluorescence in Burkitt tumor cells. II. Comparison of cells and sera from patients with Burkitt's lymphoma and infectious mononucleosis, in J. Exp. Med., vol. 128, n. 5, novembre 1968, pp. 1021–30, PMC 2138569, PMID 4878907.
- ^ a b c Harrison, pp. 1190-1194.
- ^ Infectious Mononucleosis (mono, EBV mononucleosis), su health.state.ny.us. URL consultato il 27 novembre 2009.
- ^ Chan JK, Kwong YL, Common misdiagnoses in lymphomas and avoidance strategies, in Lancet Oncol., vol. 11, n. 6, giugno 2010, pp. 579–88, DOI:10.1016/S1470-2045(09)70351-1, PMID 20227918.
- ^ Hjalgrim H, Rostgaard K, Johnson PC, et al., HLA-A alleles and infectious mononucleosis suggest a critical role for cytotoxic T-cell response in EBV-related Hodgkin lymphoma, in Proc. Natl. Acad. Sci. U.S.A., vol. 107, n. 14, aprile 2010, pp. 6400–5, DOI:10.1073/pnas.0915054107, PMC 2851961, PMID 20308568.
- ^ (EN) Chen Y, Zhao W, Lin L, Xiao X, Zhou X, Ming H, Huang T, Liao J, Li Y, Zeng X, Huang G, Ye W, Zhang Z, Nasopharyngeal Epstein-Barr Virus Load: An Efficient Supplementary Method for Population-Based Nasopharyngeal Carcinoma Screening, in Plos One, vol. 10, n. 7, luglio 2015, pp. e0132669, PMID 26151639. URL consultato il 13 dicembre 2015.
- ^ Ulff-Møller CJ, Nielsen NM, Rostgaard K, Hjalgrim H, Frisch M, Epstein-Barr virus-associated infectious mononucleosis and risk of systemic lupus erythematosus, in Rheumatology (Oxford), vol. 49, n. 9, settembre 2010, pp. 1706–12, DOI:10.1093/rheumatology/keq148, PMID 20488925.
- ^ Vaughan JH, Nguyen MD, Valbracht JR, Patrick K, Rhodes GH, Epstein-Barr virus-induced autoimmune responses. II. Immunoglobulin G autoantibodies to mimicking and nonmimicking epitopes. Presence in autoimmune disease, in J. Clin. Invest., vol. 95, n. 3, marzo 1995, pp. 1316–27, DOI:10.1172/JCI117782, PMC 441471, PMID 7533789.
- ^ C. Busse, R. Feederle; M. Schnölzer; U. Behrends; J. Mautner; HJ. Delecluse, Epstein-Barr viruses that express a CD21 antibody provide evidence that gp350's functions extend beyond B-cell surface binding., in J Virol, vol. 84, n. 2, gennaio 2010, pp. 1139-47, DOI:10.1128/JVI.01953-09, PMID 19889766.
- ^ J. Sashihara, PD. Burbelo; B. Savoldo; TC. Pierson; JI. Cohen, Human antibody titers to Epstein-Barr Virus (EBV) gp350 correlate with neutralization of infectivity better than antibody titers to EBV gp42 using a rapid flow cytometry-based EBV neutralization assay., in Virology, vol. 391, n. 2, settembre 2009, pp. 249-56, DOI:10.1016/j.virol.2009.06.013, PMID 19584018.
- ^ Y. Al Tabaa, E. Tuaillon; K. Bollore; V. Foulongne; G. Petitjean; JM. Seigneurin; C. Duperray; C. Desgranges; JP. Vendrell, Functional Epstein-Barr virus reservoir in plasma cells derived from infected peripheral blood memory B cells., in Blood, vol. 113, n. 3, gennaio 2009, pp. 604-11, DOI:10.1182/blood-2008-02-136903, PMID 18845794.
- ^ KA. Young, AP. Herbert; PN. Barlow; VM. Holers; JP. Hannan, Molecular basis of the interaction between complement receptor type 2 (CR2/CD21) and Epstein-Barr virus glycoprotein gp350., in J Virol, vol. 82, n. 22, novembre 2008, pp. 11217-27, DOI:10.1128/JVI.01673-08, PMID 18786993.
- ^ YF. Tsaparas, ML. Brigden; R. Mathias; E. Thomas; J. Raboud; PW. Doyle, Proportion positive for Epstein-Barr virus, cytomegalovirus, human herpesvirus 6, Toxoplasma, and human immunodeficiency virus types 1 and 2 in heterophile-negative patients with an absolute lymphocytosis or an instrument-generated atypical lymphocyte flag., in Arch Pathol Lab Med, vol. 124, n. 9, settembre 2000, pp. 1324-30, PMID 10975931.
- ^ emedicine: Mononucleosis, su emedicine.medscape.com. URL consultato il 29 aprile 2010.
- ^ Cozad J, Infectious mononucleosis, in The Nurse Practitioner, vol. 21, n. 3, marzo 1996, pp. 14–6, 23, 27–8, DOI:10.1097/00006205-199603000-00002, PMID 8710247. URL consultato il 27 maggio 2009.
- ^ B Kagan, Ampicillin rash, in Western Journal of Medicine, vol. 126, n. 4, 1977, pp. 333–335, PMC 1237570, PMID 855325.
- ^ a b (EN) scholarsresearchlibrary.com (PDF) (archiviato dall'url originale il 22 novembre 2010).
- ^ Rosenfield RE, Schmidt PJ, Calvo RC, McGinniss MH, Anti-i, a frequent cold agglutinin in infectious mononucleosis, in Vox Sanguinis, vol. 10, n. 5, 1965, pp. 631–634, DOI:10.1111/j.1423-0410.1965.tb01418.x, PMID 5864820.
- ^ RL. CARTER, Platelet levels in infectious mononucleosis., in Blood, vol. 25, maggio 1965, pp. 817-21, PMID 14282050.
- ^ K. Yoda, T. Sata, T. Kurata e H. Aramaki, Oropharyngotonsillitis associated with nonprimary Epstein-Barr virus infection., in Arch Otolaryngol Head Neck Surg, vol. 126, n. 2, febbraio 2000, pp. 185-93, PMID 10680870.
- ^ YA. Meunier, Infectious mononucleosis-like syndrome and gastrointestinal disorders in acute acquired cytomegalovirus infection., in Singapore Med J, vol. 46, n. 8, agosto 2005, pp. 421-3, PMID 16049613.
- ^ AL. Chapman, R. Watkin e CJ. Ellis, Abdominal pain in acute infectious mononucleosis., in BMJ, vol. 324, n. 7338, marzo 2002, pp. 660-1, PMID 11895827.
- ^ Jensen, Hal B, Acute complications of Epstein-Barr virus infectious mononucleosis, in Current Opinion in Pediatrics, vol. 12, n. 3, Lippincott Williams & Wilkins, Inc., giugno 2000, pp. 263–268, DOI:10.1097/00008480-200006000-00016, ISSN 1040-8703, PMID 10836164.
- ^ Aghenta A, A Osowo e J Thomas, Symptomatic atrial fibrillation with infectious mononucleosis, in Canadian Family Physician, vol. 54, n. 5, College of Family Physicians of Canada, maggio 2008, pp. 695–696, PMC 2377232, PMID 18474702.
- ^ A. Bonsignore, G. Grillone; M. Soliera; F. Fiumara; M. Pettinato; G. Calarco; LG. Angiò; M. Licursi, [Occult rupture of the spleen in a patient with infectious mononucleosis], in G Chir, vol. 31, n. 3, marzo 2010, pp. 86-90, PMID 20426918.
- ^ DC. Farhi, R. Ashfaq, Splenic pathology after traumatic injury., in Am J Clin Pathol, vol. 105, n. 4, aprile 1996, pp. 474-8, PMID 8604690.
- ^ R. Benz, K. Seiler; M. Vogt, A surprising cause of chest pain., in J Assoc Physicians India, vol. 55, ottobre 2007, pp. 725-6, PMID 18173027.
- ^ B. Knobel, E. Melamud; S. Nofech-Moses; L. Zeidel, [Follicular splenic lymphoid hyperplasia associated with EBV infection], in Harefuah, vol. 137, n. 10, novembre 1999, pp. 449-51, 511, PMID 10959341.
- ^ a b G. Hagemann, HJ. Mentzel; H. Weisser; A. Kunze; C. Terborg, Multiple reversible MR signal changes caused by Epstein-Barr virus encephalitis., in AJNR Am J Neuroradiol, vol. 27, n. 7, agosto 2006, pp. 1447-9, PMID 16908555.
- ^ TM. Mendes, LC. Oliveira; L. Yamamoto; GM. Del Negro; TS. Okay, Epstein-Barr virus nuclear antigen-2 detection and typing in immunocompromised children correlated with lymphoproliferative disorder biopsy findings., in Braz J Infect Dis, vol. 12, n. 3, giugno 2008, pp. 186-91, PMID 18833401.
- ^ R. Likic, D. Kuzmanic, Severe thrombocytopenia as a complication of acute Epstein-Barr virus infection., in Wien Klin Wochenschr, vol. 116, n. 1-2, gennaio 2004, pp. 47-50, PMID 15030124.
- ^ a b Infectious Mononucleosis: Treatment & Medication - eMedicine Infectious Diseases, su emedicine.medscape.com. URL consultato il 18 settembre 2010.
- ^ P. González-Delgado, M. Blanes; V. Soriano; D. Montoro; C. Loeda; E. Niveiro, Erythema multiforme to amoxicillin with concurrent infection by Epstein-Barr virus., in Allergol Immunopathol (Madr), vol. 34, n. 2, pp. 76-8, PMID 16606551.
- ^ L. Mardivirin, L. Valeyrie-Allanore; E. Branlant-Redon; N. Beneton; K. Jidar; A. Barbaud; B. Crickx; S. Ranger-Rogez; V. Descamps, Amoxicillin-induced flare in patients with DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms): report of seven cases and demonstration of a direct effect of amoxicillin on Human Herpesvirus 6 replication in vitro., in Eur J Dermatol, vol. 20, n. 1, pp. 68-73, DOI:10.1684/ejd.2010.0821, PMID 19822481.
- ^ AC. LeClaire, CA. Martin; AD. Hoven, Rash associated with piperacillin/tazobactam administration in infectious mononucleosis., in Ann Pharmacother, vol. 38, n. 6, giugno 2004, pp. 996-8, DOI:10.1345/aph.1D378, PMID 15113982.
- ^ JY. An, B. Yoon; JS. Kim; IU. Song; KS. Lee; YI. Kim, Guillain-Barré syndrome with optic neuritis and a focal lesion in the central white matter following Epstein-Barr virus infection., in Intern Med, vol. 47, n. 17, 2008, pp. 1539-42, PMID 18758131.
- ^ K. Takahashi, M. Kunishige; M. Shinohara; K. Kubo; H. Inoue; H. Yoshino; A. Asano; S. Honda; T. Matsumoto; T. Mitsui, Guillain-Barré syndrome and hemophagocytic lymphohistiocytosis in a patient with severe chronic active Epstein-Barr virus infection syndrome., in Clin Neurol Neurosurg, vol. 108, n. 1, dicembre 2005, pp. 80-3, DOI:10.1016/j.clineuro.2004.11.009, PMID 16311154.
- ^ M. Bitan, R. Or; MY. Shapira; N. Mador; IB. Resnick; N. Saleh; KM. Weinberger; S. Samuel; E. Schechter; S. Slavin; DG. Wolf, Early-onset Guillain-Barré syndrome associated with reactivation of Epstein-Barr virus infection after nonmyeloablative stem cell transplantation., in Clin Infect Dis, vol. 39, n. 7, ottobre 2004, pp. 1076-8, DOI:10.1086/424015, PMID 15472865.
- ^ A. Khalili-Shirazi, N. Gregson; I. Gray; J. Rees; J. Winer; R. Hughes, Antiganglioside antibodies in Guillain-Barré syndrome after a recent cytomegalovirus infection., in J Neurol Neurosurg Psychiatry, vol. 66, n. 3, marzo 1999, pp. 376-9, PMID 10084538.
- ^ Q. Hao, T. Saida; S. Kuroki; M. Nishimura; M. Nukina; H. Obayashi; K. Saida, Antibodies to gangliosides and galactocerebroside in patients with Guillain-Barré syndrome with preceding Campylobacter jejuni and other identified infections., in J Neuroimmunol, vol. 81, n. 1-2, gennaio 1998, pp. 116-26, PMID 9521613.
- ^ L. Drago, A. Lombardi; E. De Vecchi; G. Giuliani; R. Bartolone; MR. Gismondo, Comparison of nested PCR and real time PCR of Herpesvirus infections of central nervous system in HIV patients., in BMC Infect Dis, vol. 4, novembre 2004, p. 55, DOI:10.1186/1471-2334-4-55, PMID 15571633.
- ^ H. Fujimoto, K. Asaoka; T. Imaizumi; M. Ayabe; H. Shoji; M. Kaji, Epstein-Barr virus infections of the central nervous system., in Intern Med, vol. 42, n. 1, gennaio 2003, pp. 33-40, PMID 12583615.
- ^ JA. Schiff, JA. Schaefer; JE. Robinson, Epstein-Barr virus in cerebrospinal fluid during infectious mononucleosis encephalitis., in Yale J Biol Med, vol. 55, n. 1, pp. 59-63, PMID 6287744.
- ^ JI. Cohen, H. Kimura; S. Nakamura; YH. Ko; ES. Jaffe, Epstein-Barr virus-associated lymphoproliferative disease in non-immunocompromised hosts: a status report and summary of an international meeting, 8-9 September 2008., in Ann Oncol, vol. 20, n. 9, settembre 2009, pp. 1472-82, DOI:10.1093/annonc/mdp064, PMID 19515747.
- ^ H. Katano, MA. Ali; AC. Patera; M. Catalfamo; ES. Jaffe; H. Kimura; JK. Dale; SE. Straus; JI. Cohen, Chronic active Epstein-Barr virus infection associated with mutations in perforin that impair its maturation., in Blood, vol. 103, n. 4, febbraio 2004, pp. 1244-52, DOI:10.1182/blood-2003-06-2171, PMID 14576041.
- ^ S. Ohshima, M. Ishii; H. Asada; T. Tatekawa; N. Yamaguchi; H. Kobayashi; T. Ishii; T. Mima; I. Kawase; Y. Saeki, A possible mechanism of NK cell-lineage granular lymphocyte proliferative disorder (NK-GLPD) in a patient with chronic active Epstein-Barr virus infection (CAEBV) and severe hypersensitivity to mosquito bites (SHMB)., in Intern Med, vol. 41, n. 8, agosto 2002, pp. 651-6, PMID 12211536.
- ^ T. Taketani, A. Kikuchi; J. Inatomi; R. Hanada; H. Kawaguchi; K. Ida; T. Oh-Ishi; T. Arai; H. Kishimoto; K. Yamamoto, Chronic active Epstein-Barr virus infection (CAEBV) successfully treated with allogeneic peripheral blood stem cell transplantation., in Bone Marrow Transplant, vol. 29, n. 6, marzo 2002, pp. 531-3, DOI:10.1038/sj.bmt.1703392, PMID 11960276.
- ^ HS. Cho, IS. Kim; HC. Park; MJ. Ahn; YY. Lee; CK. Park, A case of severe chronic active Epstein-Barr virus infection with T-cell lymphoproliferative disorder., in Korean J Intern Med, vol. 19, n. 2, giugno 2004, pp. 124-7, PMID 15366645.
- ^ I. Tsuge, T. Morishima; M. Morita; H. Kimura; K. Kuzushima; H. Matsuoka, Characterization of Epstein-Barr virus (EBV)-infected natural killer (NK) cell proliferation in patients with severe mosquito allergy; establishment of an IL-2-dependent NK-like cell line., in Clin Exp Immunol, vol. 115, n. 3, marzo 1999, pp. 385-92, PMID 10193407.
- ^ SD. Vernon, T. Whistler; B. Cameron; IB. Hickie; WC. Reeves; A. Lloyd, Preliminary evidence of mitochondrial dysfunction associated with post-infective fatigue after acute infection with Epstein Barr virus., in BMC Infect Dis, vol. 6, 2006, p. 15, DOI:10.1186/1471-2334-6-15, PMID 16448567.
- ^ NE. Soto, SE. Straus, Chronic Fatigue Syndrome and Herpesviruses: the Fading Evidence., in Herpes, vol. 7, n. 2, maggio 2000, pp. 46-50, PMID 11867001.
- ^ K. Kawai, A. Kawai, Studies on the relationship between chronic fatigue syndrome and Epstein-Barr virus in Japan., in Intern Med, vol. 31, n. 3, marzo 1992, pp. 313-8, PMID 1319246.
- ^ D. Koo, Chronic fatigue syndrome. A critical appraisal of the role of Epstein-Barr virus., in West J Med, vol. 150, n. 5, maggio 1989, pp. 590-6, PMID 2545048.
- ^ EL. Thacker, F. Mirzaei e A. Ascherio, Infectious mononucleosis and risk for multiple sclerosis: a meta-analysis., in Ann Neurol, vol. 59, n. 3, marzo 2006, pp. 499-503, DOI:10.1002/ana.20820, PMID 16502434.
- ^ Burke A Cunha, Michael Stuart Bronze, Infectious Mononucleosis Workup, su emedicine.medscape.com, Medscape, 11 settembre 2011.
- ^ BA. Cunha, Systemic infections affecting the liver. Some cause jaundice, some do not., in Postgrad Med, vol. 84, n. 5, Ott 1988, pp. 148-58, 161-3, 166-8, PMID 3050927.
- ^ DN. Baron, JL. Bell; WN. Dunnet, Biochemical studies on hepatic involvement in infectious mononucleosis, in J Clin Pathol, vol. 18, marzo 1965, pp. 209-11, PMID 14276157.
- ^ CA. Horwitz, MD. Burke; P. Grimes; J. Tombers, Hepatic function in mononucleosis induced by Epstein-Barr virus and cytomegalovirus., in Clin Chem, vol. 26, n. 2, febbraio 1980, pp. 243-6, PMID 6101548.
- ^ N. Mygind, Serial serum enzyme studies in infectious mononucleosis., in Scand J Infect Dis, vol. 8, n. 3, 1976, pp. 139-42, PMID 968455.
- ^ Torre D, Tambini R, Acyclovir for treatment of infectious mononucleosis: a meta-analysis, in Scand. J. Infect. Dis., vol. 31, n. 6, 1999, pp. 543–7, DOI:10.1080/00365549950164409, PMID 10680982.
- ^ Balfour HH, Hokanson KM, Schacherer RM, A virologic pilot study of valacyclovir in infectious mononucleosis, in J. Clin. Virol., vol. 39, n. 1, 2007, pp. 16–21, DOI:10.1016/j.jcv.2007.02.002, PMID 17369082.
- ^ Mulroy R, Amoxycillin rash in infectious mononucleosis, in Br Med J, vol. 1, n. 5852, marzo 1973, p. 554, DOI:10.1136/bmj.1.5852.554, PMC 1588712, PMID 4266345.
- ^ van der Linden PD, van der Lei J, Vlug AE, Stricker BH, Skin reactions to antibacterial agents in general practice, in J Clin Epidemiol, vol. 51, n. 8, agosto 1998, pp. 703–8, DOI:10.1016/S0895-4356(98)00041-9, PMID 9743319.«infectious mononucleosis increased the risk of rash in amoxicillin users with a factor of 58.»
- ^ Wargo KA, McConnell V, Jennings M, Amoxicillin/telithromycin-induced rash in infectious mononucleosis, in Ann Pharmacother, vol. 39, n. 9, settembre 2005, p. 1577, DOI:10.1345/aph.1G140, PMID 16046485.«Approximately 70-100% of patients who receive a ß-lactam antibiotic while infected with the Epstein-Barr virus will develop a maculopapular rash»
- ^ Candy B, Hotopf M., Steroids for symptom control in infectious mononucleosis, in Cochrane Database Sys Rev, vol. 3, n. 4, 2006, pp. CD004402, DOI:10.1002/14651858.CD004402.pub2, PMID 16856045.
- ^ Infectious Mononucleosis, su webmd.com, WebMD, 24 gennaio 2006. URL consultato il 10 luglio 2006.
- ^ L. Højberg, E. Søndergård e C. Pedersen, A case of Epstein-Barr virus infection complicated with Guillain-Barré syndrome involving several cranial nerves., in Scand J Infect Dis, vol. 37, n. 6-7, 2005, pp. 522-4, DOI:10.1080/00365540510038514, PMID 16012019.
- ^ C. Oncel, A rare clinical presentation of Ebstein-Barr virus., in Braz J Infect Dis, vol. 14, n. 2, aprile 2010, pp. 211-2, PMID 20563455.
- ^ Plasmapheresis in chronic demyelinating polyneuropathy
- ^ Kimura H, Pathogenesis of chronic active Epstein-Barr virus infection: is this an infectious disease, lymphoproliferative disorder, or immunodeficiency?, in Rev. Med. Virol., vol. 16, n. 4, 2006, pp. 251–61, DOI:10.1002/rmv.505, PMID 16791843.
- ^ a b Takano H, Nakagawa K, Ishio N, et al., Active myocarditis in a patient with chronic active Epstein-Barr virus infection, in Int. J. Cardiol., vol. 130, n. 1, ottobre 2008, pp. e11–3, DOI:10.1016/j.ijcard.2007.07.040, PMID 17913266.
- ^ Luzuriaga K, Sullivan JL, Infectious mononucleosis, in N. Engl. J. Med., vol. 362, n. 21, maggio 2010, pp. 1993–2000, DOI:10.1056/NEJMcp1001116, PMID 20505178.
- ^ Mayoclinic - Prevention of mononucleosis
Bibliografia
[modifica | modifica wikitesto]- Anna M. Molina Romanzi, Microbiologia clinica, Torino, UTET, 2002, ISBN 88-7933-251-1.
- Claudio Rugarli, Medicina interna sistematica, 5ª ed., Masson, 2005, ISBN 978-88-214-2792-3.
- Tinsley Randolph Harrison, Principi di medicina interna - Il manuale, 16ª ed., New York-Milano, McGraw-Hill, 2006, ISBN 88-386-2459-3.
- Mauro Moroni, Roberto Esposito, Fausto De Lalla, Malattie infettive, 7ª ed., Milano, Elsevier Masson, 2008, ISBN 978-88-214-2980-4.
- Patrick R. Murray, Ken S. Rosenthal, Michael A. Pfaller, Microbiologia medica, 6ª ed., Milano, Elsevier Masson, 2010, ISBN 978-88-214-3169-2, ..
- Stanley Robbins, Ramzi Cotran, Le basi patologiche delle malattie vol. 1, 8ª ed., Elsevier Masson, 2010, ISBN 978-88-214-3175-3.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikiquote contiene citazioni sulla mononucleosi infettiva
Wikiquote contiene citazioni sulla mononucleosi infettiva Wikizionario contiene il lemma di dizionario «mononucleosi»
Wikizionario contiene il lemma di dizionario «mononucleosi» Wikimedia Commons contiene immagini o altri file sulla mononucleosi infettiva
Wikimedia Commons contiene immagini o altri file sulla mononucleosi infettiva
Collegamenti esterni
[modifica | modifica wikitesto]- Mononucleòsi, su Treccani.it – Enciclopedie on line, Istituto dell'Enciclopedia Italiana.
- Mononucleosi, in Dizionario di medicina, Istituto dell'Enciclopedia Italiana, 2010.
- Mononucleòṡi, su Vocabolario Treccani, Istituto dell'Enciclopedia Italiana.
- mononucleòsi, su sapere.it, De Agostini.
- (EN) mononucleosis, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- (EN) Opere riguardanti Mononucleosis, su Open Library, Internet Archive.
- (EN) CDC Atlanta - Mononucleosi, su cdc.gov. URL consultato il 18 settembre 2010 (archiviato dall'url originale il 27 dicembre 2011).
- (EN) Merck Manual online - Mononucleosi [collegamento interrotto], su merck.com.
- (EN) Medlineplus.gov - Mononucleosi, su vsearch.nlm.nih.gov.
- (EN) Rxlist.com - Mononucleosi, su rxlist.com.
- (EN) University of Leeds Infezioni da EBV, su dentistry.leeds.ac.uk.
| Controllo di autorità | Thesaurus BNCF 36270 · GND (DE) 4161648-0 · J9U (EN, HE) 987007543541305171 · NSK (HR) 005458134 · NDL (EN, JA) 00561419 |
|---|
