Sarcoidosi
| Sarcoidosi | |
|---|---|
 | |
| Specialità | ematologia, dermatologia, pneumologia e oftalmologia |
| Classificazione e risorse esterne (EN) | |
| OMIM | 181000 |
| MeSH | D012507 |
| MedlinePlus | 000076 |
| eMedicine | 301914 |
| Sinonimi | |
| Malattia di Besnier-Boeck-Schaumann | |
| Eponimi | |
| Ernest Henri Besnier Cæsar Peter Møller Boeck Jörgen Nilsen Schaumann | |
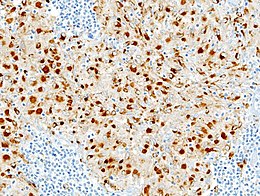
La sarcoidosi (dal greco σαρκωειδής, sarkoeidés, "carnoso"), conosciuta anche come malattia di Besnier-Boeck-Schaumann, è una malattia idiopatica multisistemica che interessa i tessuti connettivi, che insorge di solito tra i 20 e i 40 anni di età; si presenta con caratteristici granulomi non necrotizzanti e non caseosi, composti da un'alta percentuale di tessuto fibrotico indotto dall'azione del fattore di crescita trasformante beta (TGF-β).[1]
Spesso, questi granulomi sono situati nei polmoni o nei linfonodi locali, tuttavia qualsiasi organo può essere colpito.[2] Si suppone che la sarcoidosi sia causata da una reazione immunitaria a un'infezione o dalla presenza di un antigene che persiste anche dopo l'infezione iniziale.[3] Nella maggior parte dei casi la condizione si risolve da sola, senza alcun intervento medico, ma talvolta può colpire un individuo per lungo tempo, diventando pericolosa per la vita e richiedere un trattamento, che il più delle volte si realizza con la somministrazione di farmaci.[2] Il calcitriolo è la principale causa dell'elevata presenza di calcio nel sangue che si verifica nella sarcoidosi ed è sovraprodotta dai granulomi sarcoidosi. L'interferone gamma, prodotto da linfociti e macrofagi attivati, svolge un ruolo importante nella sintesi del calcitriolo.
Il trattamento è generalmente studiato per contribuire ad alleviare i sintomi e quindi non per incidere direttamente nel corso della malattia.[4] Solitamente si ricorre alla somministrazione di farmaci anti-infiammatori, come l'ibuprofene o l'aspirina.[4] Nei casi in cui la condizione si sviluppa fino a diventare progressiva e/o pericolosa per la vita, si ricorre spesso agli steroidi, come prednisone o prednisolone.[4] In alternativa, possono essere utilizzati farmaci comunemente utilizzati per il trattamento dei tumori e per sopprimere il sistema immunitario, come il metotressato, l'azatioprina e il leflunomide.[4][5][6] La mortalità media è inferiore al 5%[7] e varia in funzione dello stadio della malattia e delle sue complicanze, con un maggior mortalità nei casi di complicanze polmonari.[4][8]
Negli Stati Uniti colpisce più comunemente le persone di origine nord europea (soprattutto scandinava o islandese) o afromericani di età compresa tra 20 e i 29 anni, anche se qualsiasi etnia o gruppo di età può essere colpita.[9] In Giappone vi sono meno casi di sarcoidosi rispetto agli Stati Uniti, anche se nei giapponesi la malattia si presenta solitamente in maniera più aggressiva con il cuore che viene spesso coinvolto.[9] Sempre i giapponesi hanno anche un picco di età diversa: tra i 25 e i 40 anni di età.[10] La sarcoidosi si verifica circa due volte più spesso nelle donne e con un decorso solitamente più aggressivo.[9] Nei paesi in via di sviluppo spesso viene confusa con la tubercolosi, avendo sintomi spesso simili.[9]
La sarcoidosi è stata descritta per la prima volta nel 1877, grazie a un medico inglese di nome Jonathan Hutchinson, come una malattia della pelle che causa lesioni rossastre sulle braccia, sul viso e sulle mani.[11]
Storia
[modifica | modifica wikitesto]
La storia delle scoperte scientifiche sulla sarcoidosi è molto legata alla medicina europea, e in particolare a medici scandinavi dell'ottocento e novecento.
L'inglese sir Jonathan Hutchinson (1828-1913) può essere considerato il primo ad avere descritto la sarcoidosi. Nel 1863 presentò il caso di un paziente che soffriva di gotta che aveva lesioni cutanee e che sarebbe morto di insufficienza renale quattro anni più tardi; Hutchinson ne aveva attribuito le cause alla gotta, ma oggi che si ritiene che la vera causa fu l'alterato metabolismo del calcio dato dalla sarcoidosi.
Nel 1889, il dermatologo francese Ernest Henri Besnier (1831-1909) descrisse delle lesioni cutanee simmetriche agli arti; il suo collega norvegese Cæsar Peter Møller Boeck (1845-1917) trattò, nel suo saggio scientifico del 1899 "Multiple benign sarcoid of the skin", lesioni istologiche cutanee e ipotizzò il sospetto che fossero parte di una malattia sistemica. Da allora, le lesioni cutanee sono chiamate "sarcoidosi di Boeck".
L'oculista danese Christian Frederick Heerfordt (1871-1953) descrisse nel 1909 una malattia infiammatoria febbrile con tumefazione della parotide, uveite anteriore e talvolta interessamento del nervo facciale (febbre uveo-parotidea).
Nel 1924 il dermatologo svedese Jörgen Nilsen Schaumann (1879-1953) confermò i risultati di Boeck, descrivendo la sarcoidosi come una malattia sistemica che coinvolge diversi organi, e la chiamò Lymphogranulomatosis benigna per differenziarla dal linfoma di Hodgkin o "Linfogranuloma maligno".
Nel 1941 il medico norvegese Morten A. Kveim inventò il test di Kveim (o di Nickerson-Kveim, o di Kveim-Siltzbach) per la diagnosi della sarcoidosi, diventato ormai fuori uso negli anni novanta.
Lo svedese Sven Halvar Löfgren (1910-1978) descrisse nel 1953 le caratteristiche della forma acuta, basata sulla triade di eritema nodoso, artrite e linfoadenopatia bi-ilare (che interessa i linfonodi degli ili di entrambi i polmoni). Nei giovani questa forma spesso è chiamata sindrome di Löfgren.
Epidemiologia
[modifica | modifica wikitesto]La sarcoidosi colpisce più frequentemente i giovani adulti di entrambi i sessi, anche se alcuni studi hanno riportato una maggiore incidenza nel sesso femminile.[12] Inoltre, si riscontra un'incidenza più elevata negli individui di età inferiore ai 40 anni, con picchi nella fascia di età tra i 20 a 29 anni; un secondo picco si osserva nelle donne con un'età maggiore ai 50 anni.[5][13][14]
La sarcoidosi si presenta in tutto il mondo e in tutte le etnie, con una incidenza media di 16,5 casi su 100.000 negli uomini e 19 casi su 100.000 nelle donne. La malattia è più comune nei paesi del Nord Europa e la più alta incidenza annuale, di 60 casi per 100.000 individui, si riscontra in Svezia e Islanda. Nel Regno Unito la prevalenza è di 16 casi su 100.000.[15] Negli Stati Uniti, la sarcoidosi è più comune nelle persone di discendenza africana rispetto ai caucasoidi, con un'incidenza annuale rispettivamente di 35,5 e 10,9 casi per 100.000 individui.[16] La condizione si riscontra meno frequentemente in Sud America, Spagna, India, Canada e nelle Filippine. Ci può essere una maggiore suscettibilità alla sarcoidosi in coloro che hanno la malattia celiaca. Una possibile correlazione tra le due condizione è stata proposta.[17]
È stato inoltre osservato, negli individui con la condizione, un legame con la stagione.[18] In Grecia circa il 70% delle diagnosi avvengono fra marzo e maggio, in Spagna circa il 50% tra aprile e giugno mentre in Giappone per lo più nei mesi di giugno e luglio.[18]
La diversa incidenza riscontrata nei vari luoghi, può essere almeno in parte attribuibile alla mancanza di programmi di screening in alcune regioni del mondo e la presenza di altre malattie granulomatose, come la tubercolosi, che possono interferire con la diagnosi di sarcoidosi dove esse sono prevalenti.[14] Ci possono essere anche differenze nella gravità della malattia tra le persone di diverse etnie. Diversi studi suggeriscono che i sintomi nelle persone di origine africana possono essere più gravi e diffusi rispetto ai caucasici, che hanno più probabilità di avere una malattia asintomatica.[19] La manifestazione sembra essere leggermente diversa a seconda della razza e del sesso. L'eritema nodoso è molto più comune negli uomini che nelle donne e nei caucasici. Nei giapponesi, il coinvolgimento oftalmologico e cardiaco sono più comuni.[5]
La sarcoidosi si riscontra più comune in alcune professioni, come i vigili del fuoco, gli educatori, il personale militare, le persone che lavorano in settori in cui vengono utilizzati pesticidi, le forze dell'ordine e il personale sanitario.[20]
Eziologia
[modifica | modifica wikitesto]Tra le possibili cause di sarcoidosi potrebbe esserci l'esposizione a silice cristallina, che viene usata come componente di alcune compresse nella forma anidra colloidale (SiO2). Alcuni medici spagnoli, osservando le reazioni dell'organismo di un loro paziente alla somministrazione di antipertensivi, hanno ipotizzato che la silice contenuta nei medicinali possa essere causa di reazioni avverse anche gravi. L'unico elemento comune tra i vari farmaci somministrati al paziente era la silice colloidale anidra nelle compresse. L'associazione tra questa componente e la sarcoidosi è dimostrata dalla comparsa e scomparsa dei sintomi in tre diverse occasioni con tre diversi farmaci.
La reazione probabilmente è dovuta a una risposta immune e infiammatoria alla silice a livello intestinale che ha causato una reazione abnorme in un soggetto evidentemente predisposto alla sarcoidosi. Sono sicuramente dei fattori predisponenti quelli immunologici, dal momento che nel granuloma sarcoidotico vi sono numerose alterazioni immunologiche che suggeriscono una risposta cellulo-mediata di tipo T helper contro antigeni ambientali. I fattori genetici sembrano essere coinvolti dal momento che vi è un raggruppamento di casi all'interno della stessa famiglia e anche una associazione con alcuni genotipo HLA. I fattori ambientali rivestono un ruolo ancora incerto. Di fronte a sintomi di sarcoidosi, è pertanto opportuno valutare sempre la terapia non solo analizzando il tipo di farmaco usato ma anche le eventuali componenti in silice[21].
Segni e sintomi
[modifica | modifica wikitesto]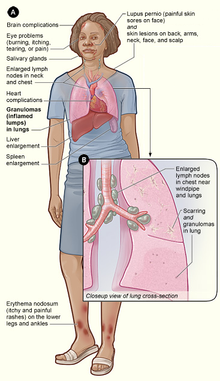
La sarcoidosi è una malattia infiammatoria sistemica che può colpire qualsiasi organo ma i polmoni sono coinvolti nella quasi totalità dei casi (più del 90%). tuttavia può manifestarsi in modo asintomatico, ovvero senza mostrare sintomi, e venire scoperta casualmente in circa il 5% dei casi.[23] I sintomi più comuni, che tendono a essere vaghi, comprendono stanchezza (non alleviata dal sonno, nel 66% dei casi), astenia, perdita di peso, dolori articolari (in circa il 70% dei casi),[24] artrite (14%-38% dei casi), secchezza degli occhi, gonfiore delle ginocchia, visione sfocata, fotofobia, mancanza di respiro, tosse e lesioni cutanee.[1][25][26][27] Meno frequentemente, i pazienti possono presentare emottisi.[1] I sintomi cutanei variano e vanno da eruzioni cutanee e noduli (piccole protuberanze) all'eritema nodoso, al granuloma anulare, al lupus pernio. La sarcoidosi e il cancro possono presentarsi in maniera simile, rendendo difficile la distinzione.[28]
La sarcoidosi polmonare cronica può essere responsabile di insufficienza ventricolare destra. La sarcoidosi del sistema nervoso è una possibile complicanza della sarcoidosi semplice, caratterizzata da infiammazione e depositi anomali di amiloide nel tessuto nervoso, cui può conseguire una paralisi improvvisa e transitoria del VII nervo cranico.
La combinazione di eritema nodoso, linfoadenopatia ilare bilaterale e dolori articolari, prendono il nome di sindrome di Löfgren che ha una prognosi relativamente buona.[1] Questa forma della malattia si verifica molto più comunemente nei pazienti scandinavi rispetto a tutti gli altri.[9]
Tratto respiratorio
[modifica | modifica wikitesto]I polmoni sono di gran lunga l'organo in cui si manifesta più comunemente la sarcoidosi.[29] Almeno il 90% delle persone colpite mostra un coinvolgimento polmonare.[2] In generale, circa il 50% sviluppa alterazioni polmonari permanenti e dal 5% al 15% hanno una fibrosi progressiva al tessuto polmonare. La sarcoidosi del polmone è principalmente una malattia polmonare interstiziale, in cui il processo infiammatorio coinvolge gli alveoli, i piccoli bronchi e i piccoli vasi sanguigni.[30] Nei casi acuti e subacuti, l'esame fisico di solito rivela crepitii secchi.[2] Almeno il 5% di persone soffrono di ipertensione arteriosa polmonare.[2][24] Meno comunemente vi è un coinvolgimento del tratto respiratorio superiore (compresa la laringe, faringe e seni paranasali), che si verifica tra il 5% e il 10% dei casi.[31]
La sarcoidosi polmonare può essere divisa in quattro fasi. Fase 0: nessun coinvolgimento intratoracico. Fase I: adenopatia ilare bilaterale. Fase II: coinvolgimento del parenchima polmonare. Fase III: infiltrati polmonari con fibrosi.[2] Fase 4 - stadio terminale della malattia polmonare con fibrosi polmonare e alveolare.[32]
Cute
[modifica | modifica wikitesto]Tra il 9% e il 37% delle persone con la sarcoidosi sviluppa sintomi cutanei e ciò è più comune negli afro-americani.[2] La cute è il secondo organo più frequentemente colpito dopo i polmoni.[33] Le lesioni più comuni sono l'eritema nodoso, placche, eruzioni maculopapulari, noduli sottocutanei e il lupus pernio.[33] Il trattamento non è tuttavia necessario, dal momento che le lesioni di solito si risolvono spontaneamente entro due-quattro settimane. Anche se può essere deturpante, la sarcoidosi cutanea raramente causa gravi problemi.[2][34][35] La sarcoidosi del cuoio capelluto si presenta con la perdita di capelli a chiazze.[36][37]
Cuore
[modifica | modifica wikitesto]La frequenza del coinvolgimento del cuore varia ed è significativamente influenzata dalla razza; in Giappone oltre il 25% delle persone con sarcoidosi sintomatica sperimenta un coinvolgimento cardiaco, mentre negli Stati Uniti e in Europa questo valore si stima essere di solo il 5%.[2] Gli studi autoptici eseguiti negli Stati Uniti hanno evidenziato una frequenza di coinvolgimento del cuore di circa 20%-30%, mentre gli studi autoptici in Giappone hanno mostrato una frequenza del 60%.[26] I sintomi della sarcoidosi cardiaca possono variare da anomalie asintomatiche della conduzione a un'aritmia ventricolare fatale.[38] Le anomalie della conduzione sono le manifestazioni cardiache più comuni della sarcoidosi e può includere il blocco cardiaco completo.[39] Altre anomalie sono le aritmie ventricolari che si riscontrano in circa il 23% delle persone con sarcoidosi cardiaca.[39] La morte cardiaca improvvisa o il blocco cardiaco è una rara complicazione della sarcoidosi cardiaca.[40][41] La sarcoidosi cardiaca può causare fibrosi, formazione di granuloma o l'accumulo di liquido nell'interstizio del cuore o una combinazione dei primi due.[42]
Occhio
[modifica | modifica wikitesto]Un coinvolgimento oculare si verifica in circa il 10%-90% dei casi.[26] Le manifestazioni negli occhi comprendono uveite, uveoparotite e l'infiammazione della retina che può causare la perdita dell'acuità visiva o la cecità.[43] La manifestazione oftalmologico più comune di sarcoidosi è l'uveite.[26][44] La combinazione di uveite anteriore, parotite, paralisi del VII nervo cranico e febbre, prende nome di "sindrome di Heerford". Sono stati anche osservati noduli alla sclera associati alla sarcoidosi.[45]
Sistema nervoso
[modifica | modifica wikitesto]Uno qualsiasi dei componenti del sistema nervoso può risultare coinvolto nella condizione.[46] La sarcoidosi che colpisce il sistema nervoso è nota come "neurosarcoidosi".[46] I nervi cranici sono più comunemente colpiti, in circa il 5%-30% dei casi di neurosarcoidosi, mentre la paralisi del nervo faciale, spesso bilaterale, è la manifestazione neurologica più comune.[46][47][48] La condizione si verifica improvvisamente ed è solitamente transitoria. Il coinvolgimento del sistema nervoso centrale è presente nel 10%-25% dei casi di sarcoidosi.[31] Altre manifestazioni comuni della neurosarcoidosi comprendono disfunzioni del nervo ottico, papilledema, disfunzione del palato, alterazioni del sistema neuroendocrino, alterazioni dell'udito, anomalie dell'ipotalamo e dell'ipofisi, meningite cronica e neuropatia periferica.[2] La mielopatia, cioè il coinvolgimento del midollo spinale, si verifica in circa il 16%-43% dei casi di neurosarcoidosi ed è spesso associata con una prognosi meno favorevole.[46] Il coinvolgimento del sistema neuroendocrino nella neurosarcoidosi si verifica in circa il 5%-10% dei casi e può comportare il diabete insipido, cambiamenti nel ciclo mestruale e disfunzione ipotalamica.[46][48] Quest'ultima può portare a cambiamenti nella temperatura corporea, nell'umore e e nella produzione di prolattina.[46]
Funzione endocrina e esocrina
[modifica | modifica wikitesto]Spesso si riscontra, nei casi di sarcoidosi, un aumento della prolattina; si stima che tra il 3% e il 32% dei casi presentino iperprolattinemia[49] e ciò porta spesso, nelle donne, a amenorrea, galattorrea o alla mastite non puerperale. Inoltre, vi è frequentemente un aumento della 1,25-diidrossi-vitamina D, il metabolita attivo della vitamina D, solitamente idrossilato nel rene, ma che nei pazienti con sarcoidosi può essere idrossilata al di fuori di essi, ovvero all'interno delle cellule immunitarie che si trovano nei granulomi. L'1 alfa, 25(OH)2D3 è la causa principale dell'ipercalcemia riscontrabile nei casi di sarcoidosi. La produzione di interferone gamma prodotto da linfociti e macrofagi attivati, svolge un ruolo importante nella sintesi di calcitriolo.[50] L'ipercalciuria (eccessiva secrezione di calcio nelle urine) e l'ipercalcemia (una quantità troppo elevata di calcio nel sangue) si riscontrano in meno del 10% dei casi. Una disfunzione tiroidea è presente nel 4,2%-4,6% dei casi.[51][52]
L'allargamento della parotide si verifica in circa il 5%-10% delle persone[5] e vi è, di regola, un coinvolgimento bilaterale. La ghiandola di solito non appare tenera, ma dura e liscia. Può riscontrarsi una bocca asciutta; le altre ghiandole esocrine raramente sono coinvolte.[2] Gli occhi, le ghiandole o le parotidi, vengono interessate nel 20%-50% dei casi.[53]
Apparato gastrointestinale e genito-urinario
[modifica | modifica wikitesto]Un coinvolgimento sintomatico dell'apparato gastrointestinale, con l'esclusione del fegato, si verifica in meno dell'1% di persone e lo stomaco è l'organo più frequentemente colpito, anche se l'intestino può essere interessato in alcuni rari casi.[5][54] Studi autoptici hanno riscontrato un coinvolgimento gastrointestinale in meno del 10% dei pazienti con sarcoidosi.[48] Questi casi si presentano in modo simile alla malattia di Crohn che è una frequente patologia granulomatosa dell'intestino.[5] Le autopsie hanno rivelato anche un coinvolgimento del pancreas nell'1%-3% dei pazienti.[48] Sintomi al rene si verificano solo nello 0,7% dei casi, anche se all'autopsia è stato dimostrato tale organo viene colpito nel 22% dei pazienti ed esclusivamente nei casi di malattia cronica.[5][26][48] I sintomi renali solitamente consistono in una nefrocalcinosi, anche se può essere riscontrata una nefrite granulomatosa interstiziale che si manifesta con una ridotta clearance della creatinina.[5][48] Meno comunemente possono essere colpiti l'epididimo, i testicoli, la prostata, le ovaie, le tube di Falloppio, l'utero o la vulva.[26][55][56] Un coinvolgimento testicolare è stato riscontrato, in sede autoptica, in circa il 5% dei pazienti.[48][56] Nei maschi, la sarcoidosi può portare alla sterilità.[57]
Circa il 70% dei pazienti presentano granulomi nel fegato, anche se solo nel circa il 20%-30% dei casi si riscontrano anomalie nei test di funzionalità epatica.[1][2] In circa il 5%-15% vi è anche epatomegalia, cioè l'ingrossamento del fegato.[26] Solo il 5%-30% dei casi di coinvolgimento epatico sono sintomatici.[58] L'ittero si verifica raramente.[2][5]
Ematologia e immunologia
[modifica | modifica wikitesto]Anomalie negli esami del sangue sono frequenti, riscontrabili in oltre il 50% dei casi, tuttavia ciò non è sufficiente per formulare una diagnosi.[2][31] La linfopenia è l'anomalia ematologica più comune nella sarcoidosi.[2] L'anemia si verifica in circa il 20% delle persone con sarcoidosi.[2] La leucopenia è meno comune e si verifica ancora meno frequentemente ma raramente è grave.[2] Anche la trombocitopenia e l'anemia emolitica sono piuttosto rare.[5] In assenza di splenomegalia, leucopenia può riflettere coinvolgimento del midollo osseo, ma la presentazione più comune è una ridistribuzione delle cellule T del sangue ai siti della malattia.[19] Altri reperti non specifici includono monocitosi, che si riscontra nella maggior parte dei casi di sarcoidosi,[59] aumento degli enzimi epatici o della fosfatasi alcalina. Gli individui con sarcoidosi hanno spesso anomalie immunologiche come le allergie.[53] L'ipergammaglobulinemia policlonale è anch'essa un'anomalia immunologica piuttosto comune riscontrabile nella sarcoidosi.[53]
La linfoadenopatia (ingrossamento dei linfonodi) è frequente nella sarcoidosi e si riscontra nel 15% dei casi.[27] I linfonodi intratoracici appaiono ingranditi nel 75%-90% di tutti i pazienti; solitamente si tratta di linfonodi ilari, ma anche quelli paratracheali vengono comunemente coinvolti. La linfoadenopatia periferica è molto comune, con coinvolgimento soprattutto dei linfonodi cervicali, ascellari, epitrocleari e inguinali.[60] Circa il 75% dei casi mostrano un coinvolgimento della milza visibile al microscopio, anche se solo in circa il 5-10% dei casi si arriva alla splenomegalia.[5][53]
Diagnosi
[modifica | modifica wikitesto]
La diagnosi richiede una valutazione combinata dei dati clinici, radiologici e istologici, e va confermata con esame istologico (di norma eseguito nelle sedi più accessibili, come può essere una biopsia transbronchiale in corso di broncoscopia, o una biopsia linfonodale).[61]
La sarcoidosi può essere diagnosticata inaspettatamente su radiografie del torace di routine sotto forma di adenopatia ilare bilaterale o presentarsi con linfoadenopatia periferica. Anche la PET mostra un'elevata sensibilità diagnostica.
L'esame radiologico dimostra che:
- Nel 10% circa delle persone coinvolte risulta avere una radiografia normale,
- Nel 15% si riscontra infiltrati polmonari senza presenza di linfoadenopatia,
- Nel 40% mostra la linfoadenopatia dell'ilo,
- Nel 30-50% dei casi si ha la combinazione di linfoadenopatia e infiltrati, la più grave.
In caso di evidenti segni clinici di Sindrome di Löfgren, si può evitare la conferma istologica qualora il lavaggio broncoalveolare abbia evidenziato la tipica linfocitosi CD4+.[61]
Complessivamente, la diagnosi è di esclusione, in quanto non ci sono ancora test sufficiente specifici per questa patologia.[61]
Dal punto di vista laboratoristico in corso di sarcoidosi sono elevati la beta2-microglobulina, prodotta dai linfociti, e l'ACE (Enzima Convertitore dell'Angiotensina) prodotto dalle cellule del granuloma sarcoide e indice di attività della malattia.
Trattamento
[modifica | modifica wikitesto]
Il trattamento della malattia non è strettamente necessario[12]. La somministrazione di corticosteroidi, in particolar modo di prednisone, con lo scopo di ridurre la risposta infiammatoria rappresenta l'approccio terapeutico d'elezione. Il ricorso a farmaci diversi, quali il metotrexate, l'azatioprina, melatonina, l'idrossiclorochina e la ciclosporina, è giustificato nei pazienti con sarcoidosi sistemica che non rispondono alla terapia steroidea o che necessitano di dosi di mantenimento troppo elevate. In alcuni casi si ricorre all'associazione dell'immunosoppressore e dello steroide per migliorare il controllo della malattia. Scopo della terapia con corticosteroidi e farmaci citotossici è la riduzione del processo infiammatorio e della formazione di granulomi.
L'uso dell'ACE vale solo come test orientativo, ma non è in alcun modo specifico.
Recentemente è stato individuato un probabile marker indicatore dell'attività macrofagica, cioè quei macrofagi alveolari attivati ed esponenti l'antigene, secondo l'MHC classe II, ai linfociti: la chitotriosidasi, una chitinasi utile secondo i ricercatori a formare un quadro globale e indicativo sulla gravità della malattia.
Prognosi
[modifica | modifica wikitesto]
La sarcoidosi può guarire spontaneamente o diventare cronica, con esacerbazioni e remissioni. In alcune persone, tale condizione può progredire fino alla fibrosi polmonare e, quindi, alla morte. Circa la metà dei casi si risolvono senza un trattamento o entro 12-36 mesi dall'inizio della cura, mentre la quasi totalità guarisce entro i cinque anni. Alcuni casi, tuttavia, possono persistere per diversi decenni.[5] Due terzi delle persone con la sarcoidosi, raggiungono una remissione dei sintomi entro 10 anni dalla diagnosi.[62] Quando vi è un coinvolgimento cardiaco, la prognosi è generalmente meno favorevole, anche se un trattamento a base di corticosteroidi appare efficace nel migliorare la conduzione atrio-ventricolare.[14][63] La prognosi tende a essere meno favorevole nella popolazione afro-americana, rispetto a quella caucasica.[9]
Sembra che gli individui con sarcoidosi vedano aumentata significativamente la probabilità di sviluppare un tumore, in particolare il tumore del polmone, i linfomi[64] e negli altri organi noti per essere coinvolti nella sarcoidosi.[65][66] Nella sindrome sarcoidosi-linfoma, la sarcoidosi è seguita dallo sviluppo di una sindrome linfoproliferativa come il linfoma non-Hodgkin.[67] Ciò può essere attribuito alle anomalie immunologiche sottostanti che si verificano durante il processo della sarcoidosi.[68]
La sarcoidosi può anche essere una conseguenza di un tumore[69] o verificarsi in concomitanza con esso.[70][71] Sono stati riportati casi di leucemia a cellule capellute[72], leucemia mieloide acuta[73] e leucemia mieloblastica acuta[74], associati alla sarcoidosi.
Note
[modifica | modifica wikitesto]- ^ a b c d e King, TE, Jr., Sarcoidosis: Interstitial Lung Diseases: Merck Manual Home Edition, su The Merck Manual Home Edition, Merck Sharp & Dohme Corp, marzo 2008. URL consultato il 19 febbraio 2014.
- ^ a b c d e f g h i j k l m n o p q A. Fauci, D. Kasper, S. Hauser, J. Jameson e J. Loscalzo, Harrison's Principles of Internal Medicine, 18ª ed., New York, McGraw-Hill Professional, 2011, ISBN 978-0-07-174889-6.
- ^ Baughman RP, Culver DA, Judson MA, Culver e Judson, A concise review of pulmonary sarcoidosis, in American Journal of Respiratory and Critical Care Medicine, vol. 183, n. 5, marzo 2011, pp. 573-81, DOI:10.1164/rccm.201006-0865CI, PMC 3081278, PMID 21037016.
- ^ a b c d e Kamangar, N; Rohani, P; Shorr, AF, Sarcoidosis Treatment & Management, su Peters, SP; Talavera, F; Rice, TD; Mosenifar, Z (a cura di), Medscape Reference, WebMD, 6 febbraio 2014. URL consultato il 19 febbraio 2014.
- ^ a b c d e f g h i j k l Nunes H, Bouvry D, Soler P, Valeyre D, Bouvry, Soler e Valeyre, Sarcoidosis, in Orphanet J Rare Dis, vol. 2, 2007, p. 46, DOI:10.1186/1750-1172-2-46, PMC 2169207, PMID 18021432.
- ^ King CS, Kelly W e Kelly, Treatment of sarcoidosis, in Disease-a-month, vol. 55, n. 11, novembre 2009, pp. 704-18, DOI:10.1016/j.disamonth.2009.06.002, PMID 19857644.
- ^ Alicia K. Gerke, Morbidity and Mortality in Sarcoidosis, in Current opinion in pulmonary medicine, vol. 20, n. 5, 2014-9, pp. 472-478, DOI:10.1097/MCP.0000000000000080. URL consultato il 13 ottobre 2018.
- ^ Sarcoidosis: Practice Essentials, Background, Pathophysiology, 17 settembre 2018. URL consultato il 13 ottobre 2018.
- ^ a b c d e f Kamangar, N; Rohani, P; Shorr, AF, Sarcoidosis, su Peters, SP; Talavera, F; Rice, TD; Mosenifar, Z (a cura di), Medscape Reference, WebMD, 6 febbraio 2014. URL consultato il 19 febbraio 2014.
- ^ Sarcoidosis (PDF), su State of Lung Disease in Diverse Communities, American Lung Association, 2010. URL consultato il 21 febbraio 2014 (archiviato dall'url originale il 21 dicembre 2014).
- ^ James DG, Sharma OP e Sharma, From Hutchinson to now: a historical glimpse (PDF), in Current Opinion in Pulmonary Medicine, vol. 8, n. 5, settembre 2002, pp. 416-23, PMID 12172446.
- ^ a b Judson MA, Boan AD, Lackland DT, The clinical course of sarcoidosis: presentation, diagnosis, and treatment in a large white and black cohort in the United States, in Sarcoidosis Vasc Diffuse Lung Dis, vol. 29, n. 2, ottobre 2012, pp. 119–27, PMID 23461074.
- ^ Baughman RP, Lower EE, du Bois RM, Sarcoidosis, in Lancet, vol. 361, n. 9363, marzo 2003, pp. 1111–8, DOI:10.1016/S0140-6736(03)12888-7, PMID 12672326.
- ^ a b c Syed J, Myers R e Myers, Sarcoid heart disease, in Can J Cardiol, vol. 20, n. 1, gennaio 2004, pp. 89-93, PMID 14968147.
- ^ Amir H. Sam e James T.H. Teo, Rapid Medicine, Wiley-Blackwell, 2010, ISBN 1-4051-8323-3.
- ^ Henke CE, Henke G, Elveback LR, Beard CM, Ballard DJ, Kurland LT, Henke, Elveback, Beard, Ballard e Kurland, The epidemiology of sarcoidosis in Rochester, Minnesota: a population-based study of incidence and survival (PDF), in Am. J. Epidemiol., vol. 123, n. 5, 1986, pp. 840-5, PMID 3962966.
- ^ Rutherford RM, Brutsche MH, Kearns M, Bourke M, Stevens F, Gilmartin JJ, Brutsche, Kearns, Bourke, Stevens e Gilmartin, Prevalence of coeliac disease in patients with sarcoidosis, in Eur J Gastroenterol Hepatol, vol. 16, n. 9, settembre 2004, pp. 911-5, DOI:10.1097/00042737-200409000-00016, PMID 15316417. URL consultato il 18 dicembre 2015 (archiviato dall'url originale il 10 giugno 2012).
- ^ a b Baughman RP, Lower EE, du Bois RM, Lower e Du Bois, Sarcoidosis, in Lancet, vol. 361, n. 9363, 29 marzo 2003, pp. 1111-8, DOI:10.1016/S0140-6736(03)12888-7, PMID 12672326.
- ^ a b Statement on Sarcoidosis (PDF), in American Journal of Respiratory and Critical Care Medicine, vol. 160, n. 2, agosto 1999, pp. 736-755, DOI:10.1164/ajrccm.160.2.ats4-99, PMID 10430755.
- ^ A Lazarus, Sarcoidosis: epidemiology, etiology, pathogenesis, and genetics., in Disease-a-month, vol. 55, n. 11, novembre 2009, pp. 649-60, DOI:10.1016/j.disamonth.2009.04.008, PMID 19857640.
- ^ (Xagena2009) - Solà R, Montserrat B, et al. Silica in oral drugs as a possible sarcoidosis-inducing agent, Lancet 2009; 373: 1943 - Fonte: Reazioni – AIFA, 2009.
- ^ Lung Diseases: Sarcoidosis: Signs & Symptoms, su nhlbi.nih.gov, National Heart, Lung, and Blood Institute. URL consultato il 9 maggio 2009.
- ^ Kamangar, N; Rohani, P; Shorr, AF, Sarcoidosis Clinical Presentation, su Peters, SP; Talavera, F; Rice, TD; Mosenifar, Z (a cura di), Medscape Reference, WebMD, 6 febbraio 2014. URL consultato il 19 febbraio 2014.
- ^ a b Nunes H, Uzunhan Y, Freynet O, Humbert M, Brillet PY, Kambouchner M, Valeyre D, Uzunhan, Freynet, Humbert, Brillet, Kambouchner e Valeyre, Pulmonary hypertension complicating sarcoidosis, in Presse medicale, vol. 41, 6 Pt 2, giugno 2012, pp. e303–16, DOI:10.1016/j.lpm.2012.04.003, PMID 22608948.
- ^ Sweiss NJ, Patterson K, Sawaqed R, Jabbar U, Korsten P, Hogarth K, Wollman R, Garcia JG, Niewold TB, Baughman RP, Patterson, Sawaqed, Jabbar, Korsten, Hogarth, Wollman, Garcia, Niewold e Baughman, Rheumatologic manifestations of sarcoidosis, in Seminars in Respiratory and Critical Care Medicine, vol. 31, n. 4, agosto 2010, pp. 463-73, DOI:10.1055/s-0030-1262214, PMC 3314339, PMID 20665396.
- ^ a b c d e f g Holmes J, Lazarus A e Lazarus, Sarcoidosis: extrathoracic manifestations, in Disease-a-month, vol. 55, n. 11, novembre 2009, pp. 675-92, DOI:10.1016/j.disamonth.2009.05.002, PMID 19857642.
- ^ a b Dempsey OJ, Paterson EW, Kerr KM, Denison AR, Paterson, Kerr e Denison, Sarcoidosis, in BMJ, vol. 339, 28 agosto 2009, pp. b3206, DOI:10.1136/bmj.b3206, PMID 19717499.
- ^ Tolaney SM, Colson YL, Gill RR e and others, Sarcoidosis mimicking metastatic breast cancer, in Clin. Breast Cancer, vol. 7, n. 10, ottobre 2007, pp. 804-10, DOI:10.3816/CBC.2007.n.044, PMID 18021484.
- ^ Baughman RP, Lower EE, Gibson K, Lower e Gibson, Pulmonary manifestations of sarcoidosis, in Presse medicale, vol. 41, 6 Pt 2, giugno 2012, pp. e289–302, DOI:10.1016/j.lpm.2012.03.019, PMID 22579234.
- ^ Fuhrer G, Myers JN e Myers, Intrathoracic sarcoidosis, in Disease-a-month, vol. 55, n. 11, novembre 2009, pp. 661-74, DOI:10.1016/j.disamonth.2009.04.009, PMID 19857641.
- ^ a b c Chen ES, Moller DR e Moller, Sarcoidosis—scientific progress and clinical challenges, in Nature reviews. Rheumatology, vol. 7, n. 8, 12 luglio 2011, pp. 457-67, DOI:10.1038/nrrheum.2011.93, PMID 21750528.
- ^ Wasfi YS, Fontenot AP. Chapter 12. Sarcoidosis. In: Hanley ME, Welsh CH, eds. CURRENT Diagnosis & Treatment in Pulmonary Medicine. New York: McGraw-Hill; 2003.
- ^ a b Mañá J, Marcoval J e Marcoval, Skin manifestations of sarcoidosis, in Presse medicale, vol. 41, 6 Pt 2, giugno 2012, pp. e355–74, DOI:10.1016/j.lpm.2012.02.046, PMID 22579238.
- ^ Heath CR, David J, Taylor SC, David e Taylor, Sarcoidosis: Are there differences in your skin of color patients?, in Journal of the American Academy of Dermatology, vol. 66, n. 1, gennaio 2012, pp. 121.e1–14, DOI:10.1016/j.jaad.2010.06.068, PMID 22000704.
- ^ Lodha S, Sanchez M, Prystowsky S, Sanchez e Prystowsky, Sarcoidosis of the skin: a review for the pulmonologist (PDF), in Chest, vol. 136, n. 2, agosto 2009, pp. 583-96, DOI:10.1378/chest.08-1527, PMID 19666758.
- ^ WD; Berger, T; Dirk, M James, Andrew's diseases of the skin: clinical dermatology, 10th, Philadelphia, Saunders Elsevier, 2006, pp. 708-711, ISBN 978-0-8089-2351-0.
- ^ House NS, Welsh JP, English JC, Welsh e English Jc, Sarcoidosis-induced alopecia, in Dermatology Online Journal, vol. 18, n. 8, 15 agosto 2012, p. 4, PMID 22948054.
- ^ Doughan AR, Williams BR e Williams, Cardiac sarcoidosis, in Heart, vol. 92, n. 2, 2006, pp. 282-8, DOI:10.1136/hrt.2005.080481, PMC 1860791, PMID 16415205.
- ^ a b Youssef G, Beanlands RS, Birnie DH, Nery PB, Beanlands, Birnie e Nery, Cardiac sarcoidosis: applications of imaging in diagnosis and directing treatment, in Heart, vol. 97, n. 24, dicembre 2011, pp. 2078-87, DOI:10.1136/hrt.2011.226076, PMID 22116891.
- ^ Reuhl J, Schneider M, Sievert H, Lutz FU, Zieger G, Schneider, Sievert, Lutz e Zieger, Myocardial sarcoidosis as a rare cause of sudden cardiac death, in Forensic Sci. Int., vol. 89, n. 3, ottobre 1997, pp. 145-53, DOI:10.1016/S0379-0738(97)00106-0, PMID 9363623.
- ^ Rajasenan V, Cooper ES e Cooper, Myocardial sarcoidosis, bouts of ventricular tachycardia, psychiatric manifestations and sudden death. A case report, in J Natl Med Assoc, vol. 61, n. 4, 1969, pp. 306-9, PMC 2611747, PMID 5796402.
- ^ Chapelon-Abric C, Cardiac sarcoidosis, in Presse Med, vol. 41, 6 Pt 2, 2012, pp. e317–30, DOI:10.1016/j.lpm.2012.04.002, PMID 22608949.
- ^ Bodaghi B, Touitou V, Fardeau C, Chapelon C, LeHoang P, Touitou, Fardeau, Chapelon e Lehoang, Ocular sarcoidosis, in Presse medicale, vol. 41, 6 Pt 2, giugno 2012, pp. e349–54, DOI:10.1016/j.lpm.2012.04.004, PMID 22595776.
- ^ Papadia M, Herbort CP, Mochizuki M, Herbort e Mochizuki, Diagnosis of ocular sarcoidosis, in Ocular Immunology and Inflammation, vol. 18, n. 6, dicembre 2010, pp. 432-41, DOI:10.3109/09273948.2010.524344, PMID 21091056.
- ^ Qazi FA, Thorne JE, Jabs DA, Thorne e Jabs, Scleral nodule associated with sarcoidosis, in American Journal of Ophthalmology, vol. 136, n. 4, ottobre 2003, pp. 752-4, DOI:10.1016/S0002-9394(03)00454-9, PMID 14516826.
- ^ a b c d e f Nozaki K, Judson MA e Judson, Neurosarcoidosis: Clinical manifestations, diagnosis and treatment, in Presse medicale, vol. 41, 6 Pt 2, giugno 2012, pp. e331–48, DOI:10.1016/j.lpm.2011.12.017, PMID 22595777.
- ^ Said G, Lacroix C, Plante-Bordeneuve V, Lacroix, Planté-Bordeneuve, Le Page, Pico, Presles, Senant, Remy, Rondepierre e Mallecourt, Nerve granulomas and vasculitis in sarcoid peripheral neuropathy, in Brain, vol. 125, Pt 2, 2002, pp. 264-75, DOI:10.1093/brain/awf027, PMID 11844727.
- ^ a b c d e f g Vardhanabhuti V, Venkatanarasimha N, Bhatnagar G, Maviki M, Iyengar S, Adams WM, Suresh P, Venkatanarasimha, Bhatnagar, Maviki, Iyengar, Adams e Suresh, Extra-pulmonary manifestations of sarcoidosis (PDF), in Clinical Radiology, vol. 67, n. 3, marzo 2012, pp. 263-76, DOI:10.1016/j.crad.2011.04.018, PMID 22094184.
- ^ Porter N, Beynon HL, Randeva HS, Beynon e Randeva, Endocrine and reproductive manifestations of sarcoidosis, in QJM, vol. 96, n. 8, 2003, pp. 553-61, DOI:10.1093/qjmed/hcg103, PMID 12897340.
- ^ Rheumatology Diagnosis & Therapies, 2nd, Philadelphia, Lippincott Williams & Wilkins, 2005, p. 342.
- ^ Antonelli A, Fazzi P, Fallahi P, Ferrari SM, Ferrannini E, Fazzi, Fallahi, Ferrari e Ferrannini, Prevalence of hypothyroidism and Graves disease in sarcoidosis, in Chest, vol. 130, n. 2, agosto 2006, pp. 526-32, DOI:10.1378/chest.130.2.526, PMID 16899854.
- ^ Manchanda A, Patel S, Jiang JJ, Babu AR, Patel, Jiang e Babu, Thyroid: an unusual hideout for sarcoidosis (PDF), in Endocrine practice, vol. 19, n. 2, marzo–April 2013, pp. e40–3, DOI:10.4158/EP12131.CR, PMID 23337134.
- ^ a b c d Fausto N, Abbas A, Robbins and Cotran Pathologic Basis of disease., 7th, Philadelphia, PA, Elsevier/Saunders, 2004, pp. 737-9, ISBN 978-0-7216-0187-8.
- ^ Hemasri Tokala, Karthik Polsani e Jagadeesh K. Kalavakunta, Gastric sarcoidosis: a rare clinical presentation, in Case Reports in Gastrointestinal Medicine, vol. 2013, 1º gennaio 2013, p. 260704, DOI:10.1155/2013/260704, ISSN 2090-6528, PMC 3867894, PMID 24368949.
- ^ Vera C, Funaro D, Bouffard D, Funaro e Bouffard, Vulvar sarcoidosis: case report and review of the literature, in Journal of Cutaneous Medicine and Surgery, vol. 17, n. 4, luglio–August 2013, pp. 287-90, PMID 23815963.
- ^ a b Paknejad O, Gilani MA, Khoshchehreh M, Gilani e Khoshchehreh, Testicular masses in a man with a plausible sarcoidosis, in Indian J Urol, vol. 27, n. 2, April–June 2011, pp. 269-27, DOI:10.4103/0970-1591.82848, PMC 3142840, PMID 21814320.
- ^ Paknejad O, Gilani MA, Khoshchehreh M, Gilani e Khoshchehreh, Testicular masses in a man with a plausible sarcoidosis, in Indian Journal of Urology, vol. 27, n. 2, April–June 2011, pp. 269-27, DOI:10.4103/0970-1591.82848, PMC 3142840, PMID 21814320.
- ^ Cremers JP, Drent M, Baughman RP, Wijnen PA, Koek GH, Drent, Baughman, Wijnen e Koek, Therapeutic approach of hepatic sarcoidosis, in Curr Opin Pulm Med, vol. 18, n. 5, settembre 2012, pp. 472-82, DOI:10.1097/MCP.0b013e3283541626, PMID 22617809.
- ^ Wurm K, Löhr G e Löhr, Immuno-cytological blood tests in cases of sarcoidosis, in Sarcoidosis, vol. 3, n. 1, 1986, pp. 52-9, PMID 3033787.
- ^ Chen HC, Kang BH, Lai CT, Lin YS, Kang, Lai e Lin, Sarcoidal granuloma in cervical lymph nodes, in Journal of the Chinese Medical Association, vol. 68, n. 7, luglio 2005, pp. 339-42, DOI:10.1016/S1726-4901(09)70172-8, PMID 16038376.
- ^ a b c Core Curriculum Ematologia, McGraw-Hill, p. 164.
- ^ What Is Sarcoidosis?, su National Heart, Lung and Blood Institute, National Institutes of Health, 14 giugno 2013. URL consultato il 21 febbraio 2014.
- ^ Sadek MM, Yung D, Birnie DH, Beanlands RS, Nery PB, Yung, Birnie, Beanlands e Nery, Corticosteroid therapy for cardiac sarcoidosis: a systematic review, in Can J Cardiol, vol. 29, n. 9, settembre 2013, pp. 1034-41, DOI:10.1016/j.cjca.2013.02.004, PMID 23623644.
- ^ Karakantza M, Matutes E, MacLennan K, O'Connor NT, Srivastava PC, Catovsky D, Matutes, MacLennan, O'Connor, Srivastava e Catovsky, Association between sarcoidosis and lymphoma revisited, in J. Clin. Pathol., vol. 49, n. 3, 1996, pp. 208-12, DOI:10.1136/jcp.49.3.208, PMC 500399, PMID 8675730.
- ^ Askling J, Grunewald J, Eklund A, Hillerdal G, Ekbom A, Grunewald, Eklund, Hillerdal e Ekbom, Increased risk for cancer following sarcoidosis, in Am. J. Respir. Crit. Care Med., vol. 160, 5 Pt 1, novembre 1999, pp. 1668-72, DOI:10.1164/ajrccm.160.5.9904045, PMID 10556138.
- ^ Tana C, Giamberardino MA, Di Gioacchino M, Mezzetti A, Schiavone C, Giamberardino, Di Gioacchino, Mezzetti e Schiavone, Immunopathogenesis of sarcoidosis and risk of malignancy: a lost truth?, in International Journal of Immunopathology and Pharmacology, vol. 26, n. 2, April–June 2013, pp. 305-13, PMID 23755746.
- ^ Kornacker M, Kraemer A, Leo E, Ho AD, Kraemer, Leo e Ho, Occurrence of sarcoidosis subsequent to chemotherapy for non-Hodgkin's lymphoma: report of two cases, in Ann. Hematol., vol. 81, n. 2, 2002, pp. 103-5, DOI:10.1007/s00277-001-0415-6, PMID 11907791.
- ^ Suvajdzic N, Milenkovic B, Perunicic M, Stojsic J, Jankovic S, Milenkovic, Perunicic, Stojsic e Jankovic, Two cases of sarcoidosis-lymphoma syndrome, in Med. Oncol., vol. 24, n. 4, 2007, pp. 469-71, DOI:10.1007/s12032-007-0026-8, PMID 17917102.
- ^ Yao M, Funk GF, Goldstein DP, DeYoung BR, Graham MM, Funk, Goldstein, Deyoung e Graham, Benign lesions in cancer patients: Case 1. Sarcoidosis after chemoradiation for head and neck cancer, in J. Clin. Oncol., vol. 23, n. 3, 2005, pp. 640-1, DOI:10.1200/JCO.2005.02.089, PMID 15659510.
- ^ Yamasawa H, Ishii Y, Kitamura S, Ishii e Kitamura, Concurrence of sarcoidosis and lung cancer. A report of four cases, in Respiration, vol. 67, n. 1, 2000, pp. 90-3, DOI:10.1159/000029470, PMID 10705270.
- ^ Zambrana F, Antúnez A, García-Mata J, Mellado JM, Villar JL, Antúnez, García-Mata, Mellado e Villar, Sarcoidosis as a diagnostic pitfall of pancreatic cancer, in Clin Transl Oncol, vol. 11, n. 6, 2009, pp. 396-8, DOI:10.1007/s12094-009-0375-1, PMID 19531456.
- ^ Schiller G, Said J, Pal S, Said e Pal, Hairy cell leukemia and sarcoidosis: a case report and review of the literature, in Leukemia, vol. 17, n. 10, 2003, pp. 2057-9, DOI:10.1038/sj.leu.2403074, PMID 14513061.
- ^ Maloisel F, Oberling F e Oberling, Acute myeloid leukemia complicating sarcoidosis, in J R Soc Med, vol. 85, n. 1, 1992, pp. 58-9, PMC 1293471, PMID 1548666.
- ^ Reich JM, <366::AID-CNCR2820550212>3.0.CO;2-1 Acute myeloblastic leukemia and sarcoidosis. Implications for pathogenesis, in Cancer, vol. 55, n. 2, 1985, pp. 366-9, DOI:10.1002/1097-0142(19850115)55:2<366::AID-CNCR2820550212>3.0.CO;2-1, PMID 3855267.
Bibliografia
[modifica | modifica wikitesto]- Joseph C. Segen, Concise Dictionary of Modern Medicine, New York, McGraw-Hill, 2006, ISBN 978-88-386-3917-3.
Voci correlate
[modifica | modifica wikitesto]Altri progetti
[modifica | modifica wikitesto] Wikizionario contiene il lemma di dizionario «sarcoidosi»
Wikizionario contiene il lemma di dizionario «sarcoidosi» Wikimedia Commons contiene immagini o altri file su sarcoidosi
Wikimedia Commons contiene immagini o altri file su sarcoidosi
Collegamenti esterni
[modifica | modifica wikitesto]- (EN) sarcoidosis, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- Associazione Amici Contro la Sarcoidosi Italia, su sarcoidosi.org.
- (EN) The Foundation for Sarcoidosis Research, su stopsarcoidosis.org.
- (EN) Pathology Images of Sarcoidosis and Other Granulomatous Diseases, su granuloma.homestead.com.
- (EN) WASOG World Association for Sarcoidosis and Other Granulomatous Disorders, su wasog.org.
| Controllo di autorità | Thesaurus BNCF 24187 · J9U (EN, HE) 987007556071105171 · NDL (EN, JA) 00574579 |
|---|