Carbonati: differenze tra le versioni
Vai alla navigazione
Vai alla ricerca
Contenuto cancellato Contenuto aggiunto
Nessun oggetto della modifica |
Nessun oggetto della modifica |
||
| Riga 2: | Riga 2: | ||
[[File:Carbonate-3D-balls.png|thumb|Struttura tridimensionale dello ione carbonato, che evidenzia anche la [[risonanza (chimica)|risonanza]] con ciascun atomo di [[ossigeno]] (sfere rosse) che condivide un [[legame covalente|doppio legame]] e con carica negativa delocalizzata sui tre atomi.]] |
[[File:Carbonate-3D-balls.png|thumb|Struttura tridimensionale dello ione carbonato, che evidenzia anche la [[risonanza (chimica)|risonanza]] con ciascun atomo di [[ossigeno]] (sfere rosse) che condivide un [[legame covalente|doppio legame]] e con carica negativa delocalizzata sui tre atomi.]] |
||
I '''carbonati''' sono [[sale|sali]] derivati dall'[[acido carbonico]]. |
I '''carbonati''' sono [[sale|sali]] derivati dall'[[acido carbonico]]. |
||
valduga gay |
|||
Il carbonato è un [[anione]] di formula CO{{apici e pedici|b=3|p=2−}} caratterizzato da una discreta [[Teoria acido-base di Brønsted-Lowry|basicità di Brønsted-Lowry]], possedendo costante basica {{Exp|2,27|−4}}. Il carbonato può reagire con gli [[acido|acidi]] divenendo dapprima [[idrogenocarbonato]], HCO{{apici e pedici|b=3|p=−}}, e per neutralizzazione totale formando [[anidride carbonica]] e [[acqua]]. |
Il carbonato è un [[anione]] di formula CO{{apici e pedici|b=3|p=2−}} caratterizzato da una discreta [[Teoria acido-base di Brønsted-Lowry|basicità di Brønsted-Lowry]], possedendo costante basica {{Exp|2,27|−4}}. Il carbonato può reagire con gli [[acido|acidi]] divenendo dapprima [[idrogenocarbonato]], HCO{{apici e pedici|b=3|p=−}}, e per neutralizzazione totale formando [[anidride carbonica]] e [[acqua]]. |
||
Versione delle 09:41, 20 feb 2018
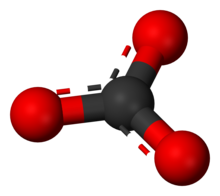
I carbonati sono sali derivati dall'acido carbonico. valduga gay Il carbonato è un anione di formula CO2−3 caratterizzato da una discreta basicità di Brønsted-Lowry, possedendo costante basica 2,27×10−4. Il carbonato può reagire con gli acidi divenendo dapprima idrogenocarbonato, HCO−3, e per neutralizzazione totale formando anidride carbonica e acqua.
Generalmente solo i carbonati dei metalli alcalini e di ammonio sono solubili in acqua, mentre i bicarbonati insolubili sono generalmente quelli dei metalli alcalino-terrosi.
Un acido più un acido basico reagiscono e formano sale, acqua, e anidride carbonica.
I carbonati
- Carbonato d'ammonio
- Carbonato di bario
- Carbonato di cadmio
- Carbonato di calcio
- Carbonato di cesio
- Carbonato di litio
- Carbonato di magnesio
- Carbonato di manganese idrato
- Carbonato di piombo
- Carbonato di potassio
- Carbonato di sodio
- Carbonato di stronzio
Voci correlate
Altri progetti
 Wikimedia Commons contiene immagini o altri file su carbonati
Wikimedia Commons contiene immagini o altri file su carbonati
Collegamenti esterni
| Controllo di autorità | Thesaurus BNCF 21829 · LCCN (EN) sh85020136 · GND (DE) 4147300-0 · BNF (FR) cb12000900x (data) · J9U (EN, HE) 987007283484005171 · NDL (EN, JA) 00572680 |
|---|