Silicato di sodio: differenze tra le versioni
m Bot: accenti |
m Bot: Aggiungo: sr:Natrijum silikat Modifico: ru:Жидкое стекло |
||
| Riga 122: | Riga 122: | ||
[[pl:Szkło wodne]] |
[[pl:Szkło wodne]] |
||
[[pt:Silicato de sódio]] |
[[pt:Silicato de sódio]] |
||
[[ru: |
[[ru:Жидкое стекло]] |
||
[[sr:Natrijum silikat]] |
|||
[[sv:Vattenglas]] |
[[sv:Vattenglas]] |
||
[[uk:Рідке скло]] |
[[uk:Рідке скло]] |
||
Versione delle 11:18, 25 set 2010
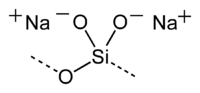
| Silicato di sodio | |
|---|---|
 | |
 | |
| Nomi alternativi | |
| E550 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | Na2SiO3 |
| Massa molecolare (u) | 122,06 |
| Numero CAS | |
| Numero EINECS | 229-912-9 |
| PubChem | 23266 |
| SMILES | [O-][Si](=O)[O-].[Na+].[Na+] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,4 g/cm3 |
| Temperatura di fusione | 1361 K |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
| Frasi R | R34, R37 |
| Frasi S | S1/2, S13, S24/25, S36/37/39, S45 |
Il silicato di sodio è un composto chimico di formula Na2SiO3. A temperatura ambiente è allo stato solido.
Utilizzi
Il silicato di sodio trova i seguenti impieghi:
- come insetticida, acaricida e fungicida;
- assieme ad altri materiali nella composizione del vetro solubile (in inglese "waterglass");
- in edilizia, come ignifugo e come accelerante per il calcestruzzo proiettato (ad esempio nella costruzione di gallerie);[1]
- nell'industria tessile, per il candeggio o la tintura del cotone;
- mescolato ad altre sostanze, come adesivo;[2]
- nell'arte viene utilizzato dal 1825 come agente protettivo per le pitture murali.[3]
Sintesi
Una piccola quantità di silicato di sodio può essere prodotta mettendo della silice (un cristallo di quarzo oppure se non si dispone di nessuno di questi due, un vetro abbastanza puro) nell'idrossido di sodio liquido, la cui temperatura di fusione è di 323 °C (vicina a quella del piombo). Se non si dispone di un'apparecchiatura adeguata, si può usare una soluzione molto concentrata di idrossido di sodio (25 M) ed un contenitore in plastica abbastanza spesso. Il contenitore per la reazione non dovrà essere né di vetro (in quanto lo bucherebbe), né di alluminio (altrimenti l'idrossido di sodio reagendo con l'alluminio produrrebbe alluminato di sodio (NaAlO2) ed idrogeno (H2), portando tutto a rischio di esplosione. La reazione avviene e si forma il silicato di sodio secondo la reazione:
- SiO2 + 2NaOH --> Na2SiO3 + H2O
Note
- ^ http://www.ingessil.com/IMG/BT10.pdf
- ^ Antonio Turco, "Nuovissimo ricettario chimico", Hoepli editore, 1990, p.82. ISBN 88-203-1837-7
- ^ http://sullarte.it/dizionario_arte/s/silicato_di_sodio_pittura_al.php
