Solvatazione: differenze tra le versioni
m Bot: Aggiungo: nl:Solvatatie |
|||
| Riga 28: | Riga 28: | ||
[[hu:Szolvatáció]] |
[[hu:Szolvatáció]] |
||
[[ja:溶媒和]] |
[[ja:溶媒和]] |
||
[[nl:Solvatatie]] |
|||
[[nn:Solvatisering]] |
[[nn:Solvatisering]] |
||
[[pl:Solwatacja]] |
[[pl:Solwatacja]] |
||
Versione delle 08:42, 23 apr 2009
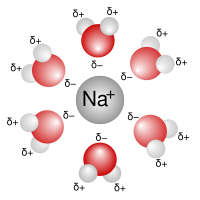
Per solvatazione in chimica si intende l'interazione tra soluto e solvente che porta le singole molecole di soluto disciolto a circondarsi di molecole di solvente. Una soluzione si differenzia infatti da una generica dispersione perché il soluto è disperso nel solvente a livello delle singole molecole o ioni e quindi non si hanno due fasi.
Interazioni intramolecolari soluto-solvente
I solventi polari sono quelli i cui atomi portano delle cariche parziali, vi è cioè un dipolo. L'acqua è il più comune solvente polare, altri solventi polari sono il DMSO, l'acetonitrile o gli alcoli. Sciogliendo un sale o una molecola polare in questi solventi, le molecole di solvente circondano il soluto in modo da orientare la carica dell'uno verso la carica opposta dell'altro e da stabilizzare il sistema.
La interazioni che si possono stabilire tra soluto e solvente sono legame idrogeno, interazioni ione-dipolo o dipolo-dipolo, o forze di Van der Waals.
Esempio
NaCl+H2O: l'ossigeno interagisce con lo ione sodio; quest'ultimo, reagendo con più molecole di acqua, si stacca dal cloro. Il cloro a sua volta interagisce anch'esso con l'acqua (la parte positiva), facendo avvenire il processo di solvatazione.