Galangina
| Galangina | |
|---|---|
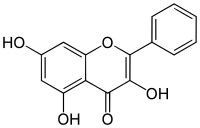 | |
| Nome IUPAC | |
| 3,5,7-triidrossi-2-fenilcromen-4-one | |
| Nomi alternativi | |
| galangina 3,5,7-triidrossiflavone | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C15H10O5 |
| Massa molecolare (u) | 270,24 |
| Numero CAS | |
| Numero EINECS | 208-960-4 |
| PubChem | 5281616 |
| SMILES | C1=CC=C(C=C1)C2=C(C(=O)C3=C(C=C(C=C3O2)O)O)O |
| Proprietà chimico-fisiche | |
| Temperatura di fusione | 214,5 °C (487,5 K) |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | 1500 (topo, per os) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 315 - 319 - 335 |
| Consigli P | 261 - 305+351+338 [1] |
La galangina è un flavonoide isolato dai rizomi di Alpinia officinarum e Alpinia galanga (famiglia Zingiberaceae), specie erbacee originarie del Sud-Est asiatico. La pianta si sviluppa da un rizoma simile a quello dello zenzero, con foglie grandi e frutti rossi. La varietà minore raggiunge il metro di altezza e produce piccoli fiori striati di rosso, mentre la varietà maggiore raggiunge anche i due metri d'altezza.
La galangina è anche uno dei componenti della propoli utilizzata come rimedio tradizionale potenzialmente utile come antibatterico, antimicotico, antivirale, cicatrizzante e immunostimolante. La propoli in commercio deve contenere non meno del 2% di flavonoidi, espressi come galangina.
Manifesta attività antiossidante.[2] È efficace contro la perossidazione, inibisce l'attività della xantina ossidasi e la lipoperossidasi.[3]
Proprietà chimico-fisiche[modifica | modifica wikitesto]
La galangina (3,5,7-tridrossiflavone, PM 270,24) è un flavone che presenta un punto di ebollizione di 518.6 °C (a 760 mmHg) e una densità pari a 1,579 g/cm3. Si presenta come una polvere aghiforme di colore giallo tenue, solubile in cloroformio e benzene, moderatamente solubile in etanolo ed etere. È dotata di quattro legami a rotazione libera, cinque accettori e tre donatori di atomi di idrogeno.[4]
Studi relativi alle proprietà biologiche della galangina[modifica | modifica wikitesto]
Attività antiproliferative[modifica | modifica wikitesto]
Il carcinoma epatocellulare (hepatocellular carcinoma, HCC) è uno dei tumori più diffusi con elevato tasso di mortalità in vari Paesi come ad esempio la Cina.
In letteratura studi in vitro indicano che la galangina potrebbe previene l'HCC attraverso molteplici meccanismi inibendo l'azione di agenti cancerogeni ambientali e dietetici e con l'inversione dell'effetto Warburg[5]. Questo flavonoide, inoltre, favorisce l’arresto del ciclo cellulare nella fase G0/G1, l’induzione dell'apoptosi tramite stimolazione delle specie reattive dell'ossigeno, l'induzione dell'autofagia e l’inibizione dell’angiogenesi, delle metastasi e della multiresistenza (MDR) ai farmaci chemioterapici. Inoltre, sono stati dimostrati effetti sinergici con altri farmaci chemioterapici.[5]
Attività sul gliobastoma multiforme umano[modifica | modifica wikitesto]
Alcuni studi in letteratura hanno valutato l'efficacia della galangina nel trattamento del glioblastoma multiforme umano (GBM) studiando le basi molecolari dei suoi effetti inibitori nella malattia. Infatti, si è osservato che la galangina inibisce la proliferazione delle cellule GBM (U251, U87MG e A172) in modo dose-dipendente e il numero di colonie formate è significativamente ridotto. I risultati hanno dimostrato che la galangina è in grado di indurre simultaneamente apoptosi e autofagia protettiva nelle cellule GBM, indicando che il trattamento combinato di galangina con inibitori dell'autofagia può essere una strategia terapeutica efficace.[6]
Attività sulla neuroinfiammazione[modifica | modifica wikitesto]
La neuroinfiammazione associata alla microglia ha un ruolo fondamentale nella progressione delle malattie neurodegenerative quindi il controllo dell'attivazione della microglia è stato studiato come potenziale strategia terapeutica. Diversi studi hanno dimostrato gli effetti antinfiammatori della galangina sulla microglia e analizzato i meccanismi molecolari sottostanti. La galangina inibisce l'espressione dell'ossido nitrico sintasi inducibile e delle citochine pro-infiammatorie e migliora l'espressione dell'interleuchina antinfiammatoria IL-10 nella microglia BV2 stimolata dal lipopolisaccaride. I dati suggeriscono che il PPAR-γ gioca un ruolo chiave nel mediare gli effetti antinfiammatori della galangina modulando le vie di segnalazione NF-κB e Nrf2/CREB.[7]
Attività antiossidante[modifica | modifica wikitesto]
La galangina ha mostrato proprietà antiossidanti sopprimendo l'espressione delle subunità NADPH ossidasi p47phox e gp91phox e migliorando l'emeossigenasi-1. Dagli studi emerge che anche PPAR-γ è coinvolto nella funzione antinfiammatoria della galangina.[7]
Studi sulla associazione galangina e quercetina[modifica | modifica wikitesto]

I flavonoidi sono composti che hanno dimostrato di possedere potenti effetti antinfiammatori in modelli cellulari e animali di infiammazione. Nello studio di Hae Nim Lee et al., 2018[8]sono stati valutati gli effetti e i meccanismi antinfiammatori di due flavonoidi naturali, quercetina e galangina, nei macrofagi RAW264.7 stimolati da lipopolisaccaridie (LPS). È stato evidenziato che la quercetina e la galangina riducono la produzione di ossido nitrico (NO), NO sintasi inducibile e interleuchina-6 e la traslocazione nucleare del fattore nucleare-B (NF-κB).
Inoltre, l'attivazione indotta da LPS della chinasi extracellulare regolata dal segnale 1/2 (Erk1/2) e della chinasi N-terminale c-Jun (JNK) è stata soppressa dalla quercetina e dalla galangina. Complessivamente, i dati hanno indicato che NF‑κB, Erk1/2 e JNK potrebbero essere potenziali bersagli molecolari di quercetina e galangina in una risposta infiammatoria indotta da LPS.
Successivamente, sono stati studiati gli effetti della somministrazione orale di quercetina o galangina, da sole o in combinazione, in un modello murino di dermatite atopica indotta da 2,4‑dinitroclorobenzene. Si è osservato che i due flavonoidi erano in grado di diminuire l'infiammazione e in combinazione risultavano ancora più efficaci.[8]
La galangina nella propoli[modifica | modifica wikitesto]
La propoli viene raccolta sia in zone temperate che tropicali. Chimicamente la propoli è composta da più di 180 diversi tipi di sostanze chimiche.[9] In generale, la propoli contiene polifenoli (flavonoidi, acidi fenolici ed esteri), aldeidi e chetoni fenolici, ecc. La percentuale di queste sostanze è la seguente: resine e balsami vegetali 50%, cera d'api 30%, polline 5%, oli essenziali e aromatici 10% e alcune altre sostanze che includono anche composti organici. La percentuale dei diversi composti è variabile perché tale percentuale è influenzata dal momento della sua raccolta e anche dall'origine geografica, quindi anche la percentuale di galangina può variare all'interno della propoli. Tuttavia, la propoli in commercio deve contenere non meno del 2% di flavonoidi, espressi come galangina.[10]
Proprietà collegate alla propoli[modifica | modifica wikitesto]

La galangina è anche uno dei componenti principali della propoli insieme a crisina, apigenina, kaempferolo, quercetina, pinocembrina e naringenina.
Grazie a questi composti, la propoli ha numerose proprietà biologiche: attività antimicrobiche, protettive nei confronti dei raggi UV, analgesiche, antiossidanti e rigenerative.[11]
In letteratura sono presenti alcuni studi che riportano le proprietà della propoli nella cura del diabete mellito. È stato indagato l'effetto di pinobanksina, galangina, crisina e pinocembrina isolate dalla propoli sulla resistenza all'insulina. Gli studi dimostrano che galangina e pinocembrina possono migliorare la resistenza all'insulina; al contrario, la pinobanksina e la crisina sono risultate inefficaci. I trattamenti con galangina e pinocembrina aumentano sostanzialmente il consumo di glucosio e il contenuto di glicogeno potenziando le attività di esochinasi e piruvato chinasi. Inoltre, dalle analisi si deduce che galangina e pinocembrina possono avere un effetto sinergico sul miglioramento della resistenza all'insulina tramite la via di segnalazione Akt/mTOR, attraverso una aumentata regolazione della fosforilazione di IR, Akt e GSK3β e una diminuita regolazione della fosforilazione dell'IRS.[12]
Galangina e COVID-19[modifica | modifica wikitesto]
Sulla base degli effetti antivirali e dei componenti fitochimici del miele, in un articolo review è stato esaminato il ruolo del miele come prodotto naturale potenzialmente utile nella cura del COVID-19. Alcuni composti bioattivi del miele hanno evidenziato potenziali effetti antivirali (ad es., metilgliossale, crisina, acido caffeico, galangina ed esperidinina) anche potenziando le risposte immunitarie antivirali. Tuttavia, i meccanismi d'azione e l'effettiva utilità di questi composti rimangono ambigue.[13]
Preparazioni[modifica | modifica wikitesto]
La propoli in commercio viene titolata almeno a 30 mg/mL in galangina mentre l'estratto secco è titolato in galangina min. 8%. Si utilizzano la soluzione idroalcolica in gocce o l'estratto secco in capsule. Rari effetti indesiderati possono essere secchezza della bocca, dolori allo stomaco talora associati a diarrea e anche reazioni allergiche a livello della pelle. Gli effetti indesiderati generalmente scompaiono con la sospensione del trattamento. Non si utilizza usata in gravidanza e durante l’allattamento.[14]
Note[modifica | modifica wikitesto]
- ^ Sigma Aldrich; rev. del 02.01.2013
- ^ T. Miyake, Shibamoto, T., Antioxidative Activities of Natural Compounds Found in Plants, in J. Agric. Food Chem., vol. 45, 1997, pp. 1819-1922.
- ^ A. Russo, Longoo, R., Vanella, A., Antioxidant activity of propolis: role of caffeic acid phenethyl ester and galangin, in Fitoterapia, 2002, pp. S21-S29.
- ^ Pubchem, su pubchem.ncbi.nlm.nih.gov.
- ^ a b Dengyang Fang et al., Chemopreventive mechanisms of galangin against hepatocellular carcinoma: A review.
- ^ Yang Kong et al., The Natural Flavonoid Galangin Elicits Apoptosis, Pyroptosis, and Autophagy in Glioblastoma, in Front Oncol. 2019.
- ^ a b Min-Ji Choi et al., Anti-inflammatory mechanism of galangin in lipopolysaccharide-stimulated microglia: Critical role of PPAR-γ signaling pathway, in Biochem Pharmacol. 2017 Nov.
- ^ a b Hae Nim Lee et al., Anti‑inflammatory effect of quercetin and galangin in LPS‑stimulated RAW264.7 macrophages and DNCB‑induced atopic dermatitis animal models.
- ^ Kuropatnicki A.K., Szliszka E., Krol W., Historical aspects of propolis research in modern times., in Evidence-Based Complement. Alternat. Med. 2013.
- ^ Syed Ishtiaq Anjum et al., Composition and functional properties of propolis (bee glue): A review.
- ^ Anna Kurek-Górecka et al., Bee Products in Dermatology and Skin Care, in Molecules 2020.
- ^ Yinkang Liu et al., Galangin and Pinocembrin from Propolis Ameliorate Insulin Resistance in HepG2 Cells via Regulating Akt/mTOR Signaling, in Evid Based Complement Alternat Med. 2018.
- ^ Mohammad A. I. et al., Antiviral and Immunomodulatory Effects of Phytochemicals from Honey against COVID-19, in Potential Mechanisms of Action and Future Directions.
- ^ Propoli, su simn.org.
Bibliografia[modifica | modifica wikitesto]
B.A. Baviskar, L. Deore e S. Khadabadi, Pharmacognosy and Phytochemistry, ISBN 9789386584588.
Guida alle piante fitoterapiche, Edra, 2019, ISBN 9788821452390.
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su galangina
Wikimedia Commons contiene immagini o altri file su galangina
Collegamenti esterni[modifica | modifica wikitesto]
- Galangin in Good Scents Company[1]