Influenza aviaria
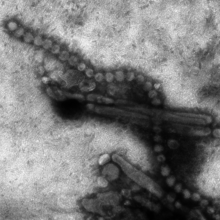
L'Influenza aviaria (nota anche come peste aviaria, dal latino avis "uccello") è una malattia infettiva contagiosa altamente diffusiva, dovuta a un virus influenzale di ceppo A (orthomyxovirus), che colpisce diverse specie di uccelli selvatici e domestici, con sintomi che possono essere inapparenti o lievi (virus a bassa patogenicità), oppure gravi e sistemici con interessamento degli apparati respiratorio, digerente e nervoso e alta mortalità (virus ad alta patogenicità). Il virus può trasmettersi agli umani, come è stato definitivamente dimostrato a partire dal 1997.
Epidemiologia e storia[modifica | modifica wikitesto]
L'influenza aviaria venne descritta per la prima volta in Piemonte nel 1878[1]. Nel 1901 se ne attribuì la causa a un virus, che nel 1955 è stato ascritto al "tipo A influenzale".
Nel 1923 un ricercatore portò clandestinamente il virus in un suo laboratorio negli U.S.A., da cui nel 1924 si diffuse colpendo il mercato dei polli di New York e in seguito tutti i territori dell'Est; tuttavia l'epidemia venne comunque sradicata nel giro di un anno.
Nel 1961 in Sudafrica è stato descritto il primo focolaio di malattia da virus HPAI in uccelli selvatici (1300 sterne).
La malattia è stata segnalata in tutto il mondo, ma i focolai da virus HPAI (peste aviaria propriamente detta) erano considerati di rara insorgenza.
Dal 1996, invece, è iniziata una serie di epidemie da virus H7 e H5 che ha coinvolto un po' tutti i continenti: Hong Kong (1997, 2001, 2002, 2003); Australia (1997); Cile (2002); centro-America (2000, 2001, 2003); Paesi Bassi, Belgio, Germania (2003); Canada (2004); U.S.A.(2004); Sudafrica (2004); sud-est asiatico (2004, 2005); Asia, Europa (2005, 2006).
L'epidemia da virus H5N1, iniziata alla fine del 2003 nel sud-est asiatico, ha coinvolto sinora più di 150 milioni di volatili. Oltre che in Vietnam, Thailandia, Cambogia, Laos, Indonesia, la malattia è stata individuata in Corea, Giappone, Cina, Russia, Kazakistan, Mongolia. Dall'ottobre 2005 il virus è entrato in Europa, in Turchia, e da qui nel resto del continente, variamente segnalato soprattutto nei volatili selvatici, nonché in Italia.
Diffusione in Europa (2022)[modifica | modifica wikitesto]
Nel corso del 2022, focolai di influenza aviaria ad alta patogenicità (HPAI) sono stati segnalati nel pollame o in volatili in cattività in Ungheria, nei Paesi Bassi, in Slovacchia, in Germania, in Croazia (contea di Osjecko-Baranjska), in Bulgaria (provincia di Dobrich) e in Francia. Sono state istituite zone di protezione e di sorveglianza attorno a tali focolai.[2]
Eziologia[modifica | modifica wikitesto]
Il virus appartiene al genere Orthomyxovirus (famiglia Orthomyxoviridae), tipo "A". Si tratta di virus a RNA, pleomorfi (cioè di forma variabile) più o meno tondeggianti del diametro di circa 100-120 nm.
Presentano un rivestimento esterno lipidico (envelope) da cui sporgono delle proteine di superficie (H=emagglutinina; N=neuraminidasi), fondamentali per il legame con le cellule e l'immunità (vedi oltre). All'interno è presente un nucleocapside (RNA+proteine) elicoidale contenente 8 segmenti di RNA che codifica per 10 tipi di proteine.
Le H e N possono differire antigenicamente dando luogo a varianti fenotipiche virali. Negli uccelli sono presenti tutte quelle conosciute: 16 per l'H e 9 per la N che, combinandosi, determinano un grandissimo numero di "sottotipi"diversi,denominati ognuno con la sigla H(n) N(n).
I vari sottotipi sono stati classificati in due gruppi, a seconda della capacità di dar luogo a sindromi più o meno gravi:
- virus HPAI (high pathogenic avian influenza, virus ad alta patogenicità),
- virus LPAI (low pathogenic avian influenza, virus a bassa patogenicità).
Dato che questa caratteristica dipende dalla struttura virale e può variare nel tempo a causa di mutazioni o ricombinazioni genetiche, ceppi poco patogeni possono diventare altamente patogeni.
Il virus è particolarmente resistente alle basse temperature e, in tali condizioni, rimane vitale a lungo nelle feci (7 giorni, oltre 30 giorni a 0 °C), tessuti, acqua (sino a un mese a 4 °C). Viene distrutto a 60 gradi in 30 minuti, per bollitura in 2 minuti, per luce solare diretta in 1÷2 giorni ed è inattivato immediatamente dai raggi UV e dai comuni disinfettanti.
Variabilità virale[modifica | modifica wikitesto]
Come tutti i virus influenzali, quello aviario possiede un elevato tasso di mutazione che procede secondo due meccanismi:
- deriva antigenica (drift);
- sostituzione antigenica (shift) o ricombinazione.
Nel primo caso (drift) si tratta di mutazioni puntiformi dell'RNA che possono essere silenti (cioè non modificano gli aminoacidi codificati), oppure possono determinare cambiamenti nella sequenza proteica. L'accumulo di mutazioni in un sito antigenico determina periodicamente la comparsa di nuovi ceppi dello stesso sottotipo o nuovi sottotipi (il tasso medio di mutazione dei geni che codificano per l'emagglutinina è circa 1000 volte superiore a quello che si ha nel corso, per esempio, della sintesi normale delle cellule dei mammiferi).
Nello shift, si ha la sostituzione completa di una proteina virale (per esempio una emoagglutinina, o una neuraminidasi). Ciò è reso possibile dal fatto che il genoma è segmentato, cioè formato da otto segmenti indipendenti di RNA che possono essere scambiati con altri virus, quando replicano assieme in una stessa cellula, con la formazione risultante di veri e propri ibridi virali. Questi ultimi possono esibire nuove combinazioni di H e N assieme ad altre proteine esterne o interne. Gli eventi di ricombinazione si verificano ordinariamente in individui di specie ricettive a più sottotipi contemporaneamente (suini e diverse specie di uccelli tra cui gli acquatici migratori).
Quando compare un virus di un sottotipo nuovo, per superare il processo selettivo esso deve adattarsi al nuovo ospite e potersi trasmettere. Ciò richiede numerosi cicli virali e quindi numerosi passaggi da soggetto a soggetto. La diffusibilità peraltro non è necessariamente accompagnata da patogenicità, che dipende sia dal virus (mutazioni patogeniche) che dall'ospite (bersagli cellulari coinvolti). Per esempio l'H5N1/HongKong/97 (frutto di ricombinazioni avvenute in oche, anatre e quaglie: H5N1+H6N1+H9N2= H5N1 altamente patogeno), pur essendo particolarmente aggressivo per la mutazione di una proteina interna (NS1), fino ad oggi non si è radicato negli umani (umanizzato), cioè non è in grado di replicarsi efficientemente né ritrasmettersi. Questa proprietà però potrebbe essere acquisita da un ibrido dell'H5N1 con un virus influenzale umano (vedi i paragrafi successivi).
H5N1[modifica | modifica wikitesto]
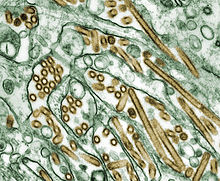
Definito nasty beast (una brutta bestia) in un articolo su “Nature”, è il virus altamente patogeno ad ampio spettro d'ospite di cui si è già accennato precedentemente: nel dicembre 1997 ha per la prima volta infettato 18 persone a Hong Kong, uccidendone 6.
Da allora sino a settembre 2007 sono state contagiate circa 300 persone con oltre duecento morti, soprattutto nel sud est asiatico, ma anche in Cina, Azerbaigian, Iraq, Egitto, Turchia.
Considerato il numero delle persone esposte l'incidenza è stata molto bassa.
L'infezione ha interessato soggetti a stretto rapporto con il pollame vivo e in scarsissime condizioni igieniche. In qualche caso c'è stato contagio interumano che però non si è esteso oltre una prima generazione di contatti.
Seppure sporadica la malattia si è presentata con una mortalità elevata (più del 50%) come mai si era verificato per alcun virus aviario noto. Per tali motivi l'OMS e i maggiori virologi ed epidemiologi mondiali ritengono H5N1, nel caso dovesse acquisire la capacità di replicarsi efficacemente negli umani, i migliori candidati per una eventuale nuova pandemia influenzale entro i prossimi 3-5 anni.
A livello globale, gli aumenti esponenziali dei focolai di influenza aviaria non sono solo una questione di mutazioni casuali nei virus influenzali, ma anche il risultato di fattori sociali e ambientali antecedenti. Come mostra il caso di studio dello scioglimento del permafrost dello Qinghai nell'altopiano del Tibet, esso fornisce un chiaro esempio di come sia nata una epidemia di influenza (H5N1) correlata ai persistenti focolai di ceppi di influenza aviaria del Qinghai negli ultimi dodici anni.[3] Infatti, il governo cinese istituì allevamenti di oche, allevate in cattività ,come fonte di cibo ad alto contenuto proteico per gli operai impegnati nella costruzione di una ferrovia. A partire dal 2005 e proseguendo negli anni successivi, il lago Qinghai è stato teatro della comparsa senza precedenti dell'influenza aviaria tra le oche migratrici.[3] Questo è stato un momento chiave nella diffusione globale dell'H5N1 al pollame in tre continenti.[3]
Patogenesi[modifica | modifica wikitesto]
Verosimilmente tutte le specie aviarie sono suscettibili di infezione e tutti gli studiosi sono concordi nel ritenere gli uccelli il crogiolo evolutivo di origine di tutti i virus influenzali che si sarebbero adattati nel corso di milioni di anni. Gli uccelli selvatici sono i serbatoi naturali (reservoir) del virus, in particolare le specie acquatiche, nei quali circolano tutti i sottotipi conosciuti di Orthomyxovirus di tipo A. In queste specie appartenenti a vari ordini:
- anseriformi: anatre, oche, cigni, germani
- ciconiformi: cicogne, ibis, fenicotteri, aironi, nitticore, garzette
- steganopodi: cormorani, pellicani, marangoni, sule
- procellariformi: albatri
- laridi: gabbiani
- limicoli: pavoncella, cavaliere d'Italia, ...
Il virus è presente nell'intestino dove normalmente persiste in modo inapparente (virus LPAI). Molti di questi uccelli sono migratori e trasportano il virus in tutte le parti del mondo. Durante le soste in prossimità di zone umide (stagni, foci dei fiumi) incontrano altre specie di uccelli migratori o stanziali o domestici creando una situazione ideale per il contagio interspecifico favorito dal fatto che la maggior parte degli stormi è formata da soggetti giovani più ricettivi. Altri gruppi, come i columbiformi (piccioni, colombe, tortore), i turdidi (merli, cesene), irundinidi (rondini), sturnidi (storni e passeri), sembrano poco ricettivi o addirittura resistenti. I rapaci sono sensibili ma non costituiscono un serbatoio importante.
Gli uccelli domestici sono l'anello intermedio tra gli uccelli selvatici e gli altri animali domestici. Tutte le specie sono colpite (polli, faraone, oche, ecc.). Particolarmente sensibili risultano essere i tacchini.
Fra le specie domestiche, il maiale ha un ruolo fondamentale in quanto possiede recettori sia per i virus aviari che umani (tra i quali è particolarmente sensibile ai virus H1N1, H3N2 e H1N2) e può svolgere un ruolo di incubatore evolutivo e di anello di trasmissione interspecifica.
Nei felidi il primo caso di infezione è stato segnalato a dicembre 2003, in due tigri e due leopardi di uno zoo tailandese morti per aver mangiato carcasse intere di polli freschi infetti. Nell'ottobre del 2004 c'è stata un'epidemia in un altro zoo tailandese con la morte/abbattimento di 147 tigri su 441. In questi casi è da notare che nelle carcasse dei polli ingeriti era presente una notevole carica virale dovuta agli intestini. Sono stati segnalati casi nei gatti (anche in Europa) e negli zibetti e recentemente nel cane. In tutte queste specie considerate comunque la malattia è risultata sporadica e non epidemiologicamente rilevante, anche se testimonianza della particolare aggressività del ceppo in causa (H5N1).
Materiali infettanti sono le feci e le secrezioni oro-nasali. La trasmissione può essere diretta (più frequente) da soggetto a soggetto, o indiretta (soprattutto d'inverno o nei climi freddi, per la maggiore persistenza del virus nell'ambiente) con acqua, oggetti e attrezzi contaminati soprattutto dalle feci. Le vie di penetrazione sono quella oro-nasale e congiuntivale.
Sebbene il virus influenzale umano derivi, filogeneticamente dal virus influenzale aviario, cioè ne sia una forma modificata abile all'infezione umana, per quanto riguarda il virus aviario, fino al 1997 non erano mai stati descritti e dimostrati casi di trasmissione diretta da uccelli a umani. In realtà il virus aviario può passare agli umani per cause principalmente professionali.
In letteratura erano noti solo quattro casi di isolamento del virus da soggetti che avevano manifestato, al massimo, delle congiuntiviti transitorie: tutti del sottotipo H7N7 a bassa patogenicità. Il primo nel 1959, da un paziente con epatite. Il secondo (1977) in un tecnico di laboratorio australiano (esposizione accidentale). Il terzo (1981) trasmesso da una foca a un guardiano. Il quarto (1996) nelle secrezioni oculari di una allevatrice di anatre in Inghilterra.
Dal 1997 in poi la prospettiva è drasticamente cambiata con le segnalazioni di diversi casi di influenza trasmessi direttamente dal pollame in occasione delle gravi epidemie che, come si è visto, hanno interessato varie parti del mondo ma soprattutto l'Estremo Oriente. Sinora solo i sottotipi H5, H7 e H9 sono stati capaci di compiere il “salto di specie”. Oltre a H5N1, sono stati riscontrati i seguenti sottotipi: H7N7, H9N2, H7N2 e H7N3.
H7N7 ad alta patogenicità, nei Paesi Bassi nel 2003, è stato responsabile di una delle più gravi epidemie di IA mai verificatasi (più di 30 milioni di volatili abbattuti). Sono state contagiate 86 persone che hanno manifestato congiuntiviti associate o meno a sintomi influenzali. C'è stata una vittima: un veterinario impegnato nelle operazioni di polizia sanitaria in allevamento.
H9N2, a Hong Kong nel 1999 è stato isolato in due bambine ricoverate con sintomi simil-influenzali. In seguito le autorità cinesi segnalarono altri 5 casi relativi al 1998.
H7N3, H7N2 sono stati isolati in nord America, associati a congiuntiviti nel 2002/2004.
Aumento della virulenza[modifica | modifica wikitesto]
Nel luglio 2004 un gruppo di ricercatori guidati da H. Deng del Harbin Veterinary Research Institute, e dal Professor Robert Webster del St Jude Children's Research Hospital, Memphis, riportarono i risultati di esperimenti in cui i topi sono stati esposti al virus. Essi riscontrarono un progressivo aumento della patogenicità nell'arco di tre anni.[4]
Nell'agosto 2005, l'Organizzazione Mondiale della Sanità pubblicò il seguente notiziario.[5]:
Si riassumono i punti della comunicazione:
- Il rischio di pandemia è grande.
- Il rischio persisterà.
- L'evoluzione del virus non può essere predetta.
- Il sistema di primo allarme è debole.
- L'intervento preventivo (con vaccini) è possibile ma non ancora testato.
- La riduzione della morbosità e della mortalità durante una pandemia sarà impedita da inadeguati rifornimenti medici.
Clinica[modifica | modifica wikitesto]
Negli esseri umani, è stato trovato che l'influenza aviaria causa sintomi simili ad altri tipi di influenza[6]:
- febbre
- tosse
- odinofagia
- dolori muscolari
- congiuntivite
- in alcuni casi, può causare problemi respiratori e polmonite, e può essere fatale.
In un caso, un bambino di quattro anni affetto da H5N1 si presentò in ospedale con diarrea seguita rapidamente da coma e conseguente decesso, senza sviluppare altri sintomi influenzali[7]
Si distinguono due forme cliniche principali della malattia:
- influenza aviaria a bassa patogenicità (LPAI)
- influenza aviaria ad alta patogenicità (HPAI)
Le due forme, che possono coesistere, dipendono, oltre che dal ceppo virale (come già detto) anche dalla sensibilità dell'ospite per cui lo stesso virus può dare forme diverse in specie diverse. La morbilità è sempre elevata.
LPAI (Low Pathogenic Avian Influenza)[modifica | modifica wikitesto]
È la forma benigna.
Negli uccelli selvatici è prevalente e i sintomi sono in genere inapparenti (portatori sani) o molto lievi.
Nelle specie domestiche dopo una incubazione di 3-5 giorni, si possono manifestare: riduzione delle performance zootecniche (scarso accrescimento, calo deposizione); inappetenza; depressione; congiuntivite; sintomi respiratori (scolo nasale, sinusite, tosse); diarrea. Normalmente, a meno di complicazioni batteriche, si ha guarigione dopo 7-10 giorni. I sintomi sono più o meno evidenti e variamente presenti, più intensi nei tacchini.
HPAI (High Pathogenic Avian Influenza)[modifica | modifica wikitesto]
È la forma maligna o peste aviaria classica. In tutti i focolai sinora descritti sono stati isolati sempre sottotipi H5 e H7.
Negli uccelli selvatici è molto rara e il primo caso è stato descritto nel 1961 in Sudafrica dove ha coinvolto 1300 sterne, trovate morte, dalle quali è stato isolato il sottotipo H5N3. Più recentemente sono stati descritti molti casi letali nei paesi asiatici coinvolti nell'epidemia da H5N1. Il più grande è stato registrato a maggio 2005 nel lago Qinghai (Cina occidentale) con la morte di oltre 6000 uccelli acquatici di diverse specie.
Negli uccelli domestici, nei casi acuti, dopo una breve incubazione (1-5 giorni), si registrano gli stessi sintomi delle forme LPAI ma in maniera decisamente più grave e con la presenza possibile di edema facciale e dei bargigli, emorragie cutanee, sintomi nervosi (tremori, atassia, paresi). Il decorso è di 3-4 giorni con mortalità/letalità elevatissime (sino al 100%) specialmente nei tacchini, che sono i più suscettibili, dove si sono spesso osservate forme iperacute (morti improvvise).
Le lesioni anatomopatologiche, in entrambe le forme sono più o meno evidenti secondo il decorso della malattia. Possono essere macroscopicamente assenti nei casi iperacuti. Nei casi acuti interessano gli apparati digerente, respiratorio, nervoso. Nelle forme HPAI è caratteristico un quadro di diatesi emorragica generalizzata.
Diagnosi[modifica | modifica wikitesto]
Diagnosi differenziale[modifica | modifica wikitesto]
Con colera aviario acuto, malattia di Newcastle, laringotracheite infettiva.
Esami di laboratorio[modifica | modifica wikitesto]
L'influenza aviaria negli uomini può essere individuata attraverso i medesimi strumenti usati per la normale influenza. Tuttavia, questi test non sempre sono affidabili.
Nel marzo 2005, l'Organizzazione Mondiale della Sanità annunciò che tre pazienti vietnamiti, inizialmente negativi, sono stati poi riscontrati fra i casi di influenza aviaria. Tutti e tre sono stati ricoverati.
Al momento, il test più affidabile (microneutralizzazione) richiede l'uso di virus vivi che interagiscano con gli anticorpi nel corpo del paziente; poiché è necessaria la presenza di virus vivi, questi test vengono effettuati solo in strutture isolate appositamente[8].
Diretta (isolamento del virus) da tamponi tracheali o cloacali (feci) di uccelli vivi oppure da organi di uccelli morti
- Inoculazione in uova di pollo embrionate di 9-11 giorni e quindi dimostrazione del virus con
- emagglutinazione sul liquido allantoideo;
- immunodiffusione (AGID);
- sierotipizzazione (individuazione del sottotipo H);
- valutazione della patogenicità (inoculazione in pulcini di 6 settimane);
- RT-PCR (ricerca dell'RNA virale).
- Indiretta (ricerca degli anticorpi) in campioni di sangue o siero.
Terapia[modifica | modifica wikitesto]
Data la rilevanza economica e sanitaria della malattia non si attua alcuna terapia ma si interviene con misure di eradicazione. Farmaci antivirali sono talvolta efficaci sia per prevenire che per curare la malattia. In futuro, tuttavia, i farmaci antivirali potrebbero risultare inefficienti: in Cina molti di questi farmaci venivano somministrati ai polli già nei primi anni novanta e il virus potrebbe avere sviluppato una sorta di resistenza a questi tipi di farmaci[9].
Diversi nuovi medicinali sono stati sviluppati negli ultimi anni. Si sta lavorando alla preparazione di tali medicinali ma il lavoro è complicato a causa della mutazione del virus, che può diventare in alcuni casi resistente alle medicine e rendere tali medicinali meno efficaci. Uno degli antivirali, il Tamiflu, è sospettato in vari siti di indurre depressione e suicidio. Alcuni smentiscono il legame con la spagnola e l'efficacia del vaccino (Blog di Beppe Grillo: Comment on Influenza aviaria: tutto sotto controllo). Il costo di questo normale antivirale in Svizzera si aggira intorno ai 60 euro, ma in varie capitali europee è salito oltre i 400 euro. Ogni farmaco, nell'ultima fase di sperimentazione per essere autorizzato e dichiarato efficace deve essere testato su esseri umani e guarire qualche malato; per l'aviaria ciò non è stato ancora possibile, essendosi il virus manifestato in pochi casi mortali e non studiati. Inoltre non sono stati studiati la tossicità e gli effetti collaterali del vaccino.
Prevenzione[modifica | modifica wikitesto]
- Distanza sociale. Viaggiando meno, lavorando da casa e chiudendo le scuole ci sono minori opportunità di diffusione del virus.
- Precauzioni Respiratorie. Mettendo una mano davanti alla bocca tossendo o starnutendo si può limitare il diffondersi del virus. Tuttavia, non è efficace al 100% poiché il virus rimane sulle mani e potrebbe diffondersi attraverso altri mezzi, come le maniglie della porta e altro. Pertanto sarebbe preferibile tossire o starnutire su un braccio.
- Maschere chirurgiche. Nessuna maschera può evitare il diffondersi del virus, ma la NIOSH N95 standard raccomandata dall'OMS dà una buona protezione. Altre maschere possono aiutare, ma risultare meno efficaci. La maschera può essere usata per ricordare al portatore di non portare le mani in faccia. Questo può ridurre l'infezione dopo il contatto con superfici toccate da soggetti infetti in luoghi affollati dove la gente, dopo aver tossito o starnutito, non si è lavata le mani.
- Igiene. Lavarsi frequentemente le mani, specialmente quando c'è stato contatto con altra gente o superfici potenzialmente contaminate può essere d'aiuto.
Vaccini[modifica | modifica wikitesto]

Un vaccino non sarà pronto nei primi momenti della pandemia.[10] Una volta che il virus viene identificato, ci sarà bisogno di diversi mesi prima che il vaccino diventi ampiamente accessibile, poiché deve essere sviluppato, testato e autorizzato. La capacità di produrre i vaccini varia ampiamente da Stato a Stato; in effetti solo 15 Paesi sono elencati come Produttori di vaccini influenzali secondo l'Organizzazione Mondiale della Sanità.[11] Si stima che, al meglio, si potranno produrre 750 milioni di dosi all'anno, laddove occorrono due dosi di vaccino per l'immunizzazione. La distribuzione sarà probabilmente problematica.[12] Alcuni stati, comunque, hanno ben sviluppato piani per la produzione di grandi quantità di vaccino. Per esempio, le autorità canadesi dicono che potranno produrre circa 32 milioni di dosi di vaccino a quadrimestre, abbastanza vaccino per ogni persona in Canada.[13] Anche gli Stati Uniti hanno fatto passi in avanti per produrre vaccini, che potrebbe essere pronto per la produzione di massa nel 2005.[14]
Le condizioni igieniche degli animali nel sud-est asiatico sono notoriamente tra le peggiori; alcuni veterinari fanno notare come le stalle nell'UE non vengano più pulite, e la fonte principale di diffusione del virus non sia la vicinanza tra animali ed esseri umani, quanto la vicinanza tra gli animali e i loro escrementi nelle stalle, e la promiscuità fra i polli stivati in 20 in un metro quadro e dunque molto vicini a quelli malati di aviaria.
Il vaccino è prodotto e brevettato da alcune case farmaceutiche, nonostante il fatto che la competizione dei laboratori e la non condivisione dei risultati e la limitazione dello sforzo di ricerca a questi soli anziché a tutte le strutture disponibili, potrebbe creare notevoli ritardi alla scoperta di cure efficaci. Inoltre non impegnare tutte le strutture disponibili nella produzione di vaccini, potrebbe rallentarne la produzione (oltre i tempi minimi inevitabili imposti dalla meiosi delle cellule).
L'attività di sorveglianza sull'influenza aviaria in Italia è coordinata dal Dipartimento per le sanità pubblica veterinaria, la nutrizione e la sicurezza degli alimenti - Direzione Genereale della sanità animale e del farmaco veterinario - Ufficio III - del Ministero della Salute, che si avvale del supporto del Centro di referenza Nazionale per l'influenza aviaria presso l'Istituto Zooprofilattico Sperimentale delle Venezie.
In Italia[modifica | modifica wikitesto]
La variante del virus isolata è però diversa da quella che ha decimato gli allevamenti di polli asiatici. Lo ha reso noto il Ministero della Salute che ha diffuso gli esiti delle verifiche condotte presso il Centro di Referenza Nazionale per le influenze aviarie. Stando a questi risultati, l'H5N1 trovato a Mirandola è un virus a bassa patogenicità (LPAI), appartenente ai ceppi H5 comunemente rinvenuti del bacino del Mediterraneo. "L'isolato italiano – conferma il dott. Mauro Delogu dell'Università di Bologna – è caratterizzato da bassa patogenicità per gli animali e patogenicità nulla per l'uomo".
Soprattutto in Veneto, Lombardia ed Emilia, dal 1997 in poi si sono verificati diversi focolai da virus LPAI e HPAI dei sottotipi: H5N2 (1997, HPAI); H5N9 (1998, LPAI); H7N1 (1999-2001, HPAI con più di 15 milioni di capi coinvolti); H7N3 (2002-2003, LPAI con 388 focolai per 8 milioni di capi); H5N3, H7N3, H7N7 (2004,LPAI); H5N2 (2005, LPAI con 25 focolai in Veneto e 15 in Lombardia).
Se l'influenza aviaria permane fra gli animali solamente con limitati casi di contagio tra umani, essa non sarà una pandemia, anche se il rischio continuerà a porsi.
Per prevenire che la situazione progredisca in una pandemia, sono state prese le seguenti contromisure:
- Raccolta e vaccinazione del pollame
- Viaggi limitati nelle aree dove si è riscontrato il virus
Le strategie a lungo termine proposte per le regioni colpite dall'influenza aviaria in forma endemica nei gallinacei selvatici includono:
- cambiare le tecniche di allevamento per aumentare l'igiene e ridurre il contatto tra gallinacei domestici e selvatici.
- mutare le tecniche di allevamento nelle regioni dove gli animali vivono in quartieri chiusi e insani e cambiare le tecniche di mercato del pollo all'aria aperta, dove gli uccelli vengono macellati in condizioni non sane vicino a frutta e vegetali. I combattimenti fra galli giocano un ruolo importante nella diffusione della malattia, ponendo gli esseri umani a contatto con possibili gallinacei infetti
- cambiare le pratiche per la vendita, passando da polli venduti vivi a polli venduti macellati e preconfezionati.
- migliorare i costi e l'accessibilità dei vaccini
Il Senato approva un decreto-legge con il quale:
- dà la facoltà al ministro della salute di sospendere la caccia;
- dispone la creazione del Centro nazionale di lotta ed emergenza contro le malattie animali;
- autorizza ad assumere dirigenti veterinari e carabinieri dei NAS;
- autorizza il governo ad attingere al Fondo spese impreviste per l'acquisto di farmaci e di materiale profilattico;
- assegna a Baxter, Sanofi-Aventis, Chiron, Berna, commesse per la produzione del vaccino.
Profilassi diretta[modifica | modifica wikitesto]
La peste aviaria era già contemplata all'art.150-151-152-153 del regolamento di polizia veterinaria nº320/54.
L'OM 19 07 91 ha introdotto l'obbligo di denuncia per i casi di influenza da virus altamente virulenti, con misure di censimento, sequestro e isolamento, disinfezioni, eventualmente vaccinazione obbligatoria, l'istituzione di ZI (zona infetta) e ZP (zona di protezione) con restrizione delle movimentazioni sino a 15 giorni dall'ultimo esito. Il sindaco poteva ordinare l'abbattimento totale.
Il DPR nº 656 del 15 11 96 ha attuato la direttiva 92/40CE che ha istituito misure comunitarie di lotta contro l'influenza aviaria (quest'ultima è stata abrogata e sostituita dalla direttiva 2005/94 CE, del 20 12 2005 ma non è stata ancora recepita in Italia; dovrebbe esserlo entro il 1º luglio 2007). Le misure prevedono in caso di focolai da H5 e H7 (o altri ceppi altamente patogeni) l'abbattimento e distruzione di tutti i volatili del focolaio (ed eventualmente di volatili di allevamenti epidemiologicamente contigui), distruzione o trattamento di tutti i materiali contaminati, nonché procedure di disinfezione, blocco/limitazione della movimentazione di persone, animali o cose, istituzione di zona di restrizione e sorveglianza rispettivamente di uno e dieci km. Misure da tenere sino a 21 giorni dopo l'estinzione dell'ultimo focolaio. La vaccinazione è vietata ma può essere autorizzata dal Ministero della salute.
In seguito, la nuova emergenza da virus H5N1, con le implicazioni zoonosiche relative, hanno condotto l'Italia, come il resto del mondo, a un inasprimento drastico delle misure sanitarie. A partire dall'Ordinanza MDS 26 08 2005 (misure di polizia veterinaria in materia di malattie infettive e diffusive nei volatili da cortile) che detta norme per assicurare la tracciabilità dei volatili e loro prodotti, soprattutto di importazione, sono state emanate tutta una serie di disposizioni riguardanti la sorveglianza sui volatili domestici e selvatici nonché piani di emergenza per garantire la vigilanza e il controllo sulla eventuale insorgenza della malattia e soprattutto tutelare al massimo i cittadini riguardo ai prodotti della filiera avicola. Tutta la legislazione è visionabile sul sito dell'IZS delle Venezie(vedi link nei Collegamenti esterni).
Profilassi indiretta (vaccini)[modifica | modifica wikitesto]
Il Ministero della salute prevede un piano di vaccinazione d'emergenza nelle ovaiole, tacchini da carne e capponi che è stato già attuato in Lombardia e Veneto, e che prevede per il 2006 l'uso di ceppi inattivati: H5N9 (capponi e tacchini); H5N9+H7N1 (ovaiole).
Note[modifica | modifica wikitesto]
- ^ (EN) D. J. Alexander e I. H. Brown, History of high pathogenic avian influenza, in Rev. Sci. Tech., vol. 28, n. 1, 2009, pp. 19–38, DOI:10.20506/rst.28.1.1856, PMID 19618616.
- ^ Decisione di esecuzione (UE) 2022/963 della Commissione del 17 giugno 2022 che modifica l’allegato della decisione di esecuzione (UE) 2021/641 relativa a misure di emergenza in relazione a focolai di influenza aviaria ad alta patogenicità in alcuni Stati membri [notificata con il numero C(2022) 4286] (Testo rilevante ai fini del SEE), su eur-lex.europa.eu.
- ^ The evolution of H5N1 influenza viruses in ducks in southern China
- ^ Responding to the avian influenza pandemic threat (PDF), su who.int.
- ^ Health in the news | Bupa UK, su bupa.co.uk. URL consultato il 12 settembre 2005 (archiviato dall'url originale il 26 ottobre 2005).
- ^ MMS: Error
- ^ canada.com - Health, su canada.com. URL consultato il 12 settembre 2005 (archiviato dall'url originale il 14 dicembre 2005).
- ^ Bird Flu Drug Rendered Useless - washingtonpost.com
- ^ Information on Avian Influenza | Avian Influenza (Flu)
- ^ Copia archiviata, su who.int. URL consultato il 13 settembre 2006 (archiviato dall'url originale il 22 agosto 2006).
- ^ Copia archiviata, su phacilitate.co.uk. URL consultato il 13 settembre 2006 (archiviato dall'url originale il 17 luglio 2006).
- ^ Canada to launch avian flu vaccine trial | CTV News Archiviato il 27 marzo 2007 in Internet Archive.
- ^ Error - washingtonpost.com
Bibliografia[modifica | modifica wikitesto]
- Kuiken T et alii (2004), Avian H5N1 Influenza in Cats, Science 2004 306: 241
Altri progetti[modifica | modifica wikitesto]
 Wikinotizie contiene notizie di attualità su influenza aviaria
Wikinotizie contiene notizie di attualità su influenza aviaria Wikimedia Commons contiene immagini o altri file su influenza aviaria
Wikimedia Commons contiene immagini o altri file su influenza aviaria
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) bird flu, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
- (EN, FR) Influenza aviaria, su Enciclopedia canadese.
- (EN) FAQ dell'OMS riguardo l'influenza aviaria, su who.int. URL consultato il 12 settembre 2005 (archiviato dall'url originale il 24 novembre 2004).
- (EN) Informazioni riguardo l'influenza aviaria, su cdc.gov.
- Notizie sull'influenza aviaria, Istituto superiore di sanità, su epicentro.iss.it.
- Piano nazionale in preparazione della pandemia, Ministero della Salute, PDF 9/2/2006 (PDF), su ministerosalute.it. URL consultato il 25 febbraio 2006 (archiviato dall'url originale il 22 febbraio 2006).
| Controllo di autorità | Thesaurus BNCF 14158 · LCCN (EN) sh85010531 · GND (DE) 4998967-4 · BNF (FR) cb131794563 (data) · J9U (EN, HE) 987007282449805171 |
|---|