Tricloruro di cromo
Il tricloruro di cromo o cloruro di cromo(III) è il composto chimico di formula CrCl3. Esiste in forme diverse a seconda del grado di idratazione. Anidro, è un solido cristallino viola inodore, insolubile in acqua. Esiste inoltre il tricloruro di cromo esaidrato, che si può isolare in tre isomeri differenti.
Tricloruro di cromo anidro, CrCl3[modifica | modifica wikitesto]
| Tricloruro di cromo | |
|---|---|
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | CrCl3 (anidro) |
| Massa molecolare (u) | 158,36 g/mol |
| Aspetto | solido viola |
| Numero CAS | |
| Numero EINECS | 233-038-3 |
| PubChem | 24808 |
| DrugBank | DB09129 |
| SMILES | Cl[Cr](Cl)Cl |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 2,87 (25 °C) |
| Solubilità in acqua | insolubile (1,4 mg/l a 25°C in acqua deionizzata) |
| Temperatura di fusione | 1150 °C (1423 K) |
| Temperatura di ebollizione | 1300 °C (1573 K) decomposizione |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 302 |
| Consigli P | 262 [1] |
Struttura[modifica | modifica wikitesto]
Il CrCl3 anidro ha una struttura cristallina tipo YCl3, con un impacchettamento pseudo cubico compatto degli ioni cloruro, mentre gli ioni Cr3+ riempiono due terzi delle cavità ottaedriche disponendosi uno strato sì e uno no. L'assenza di cationi su strati alternati rende debole il legame tra strati adiacenti, e quindi i cristalli di CrCl3 si sfaldano facilmente lungo questi piani, e il solido ha un aspetto a scaglie.
-
Modello space-filling dell'impacchettamento cubico compatto degli ioni cloruro nella struttura cristallina di CrCl3
-
Modello ball-and-stick di parte di uno strato
-
Impilamento di strati
-
Coordinazione ottaedrica attorno al cromo
Sintesi[modifica | modifica wikitesto]
Il CrCl3 anidro si può ottenere per alogenazione diretta del cromo metallico con cloro, o indirettamente trattando l'ossido di cromo(III) con cloro in presenza di carbonio a 800 °C; in questo caso si forma monossido di carbonio come prodotto secondario:[2]
- Cr2O3 + 3C + 3Cl2 → 2CrCl3 + 3CO
Lo si può preparare anche trattando l'esaidrato con cloruro di tionile.
Reattività[modifica | modifica wikitesto]
Il CrCl3 anidro è un composto stabile e idrofobico, con un'evidente facilità a caricarsi di elettricità statica, per cui è molto più pratico pesarlo in contenitori di vetro.
In acqua ultrapura, senza aggiunta di acido, una soluzione ottenuta facendo vorticare costantemente a 25 °C per 12 h 1 L di acqua lasciato a contatto con circa 50 mg di CrCl3 anidro (che sono già un largo eccesso rispetto alla capacità di dissoluzione del sale) presenta un pH di circa 4,7, per via dell'idrolisi acida causata dai pochi cationi tripositivi Cr3+ passati in soluzione. Questa soluzione, filtrata subito dopo la preparazione, analizzata in spettroscopia ottica di emissione risulta avere una concentrazione di cromo totale intorno a 460 µg/l, corrispondente a 1,41 mg/l di CrCl3 disciolti, pari a una concentrazione molare di ~8,9 µmol/l di CrCl3 (o di cromo).
Come la maggior parte dei composti di Cr(III), è chimicamente piuttosto inerte, mentre nello stato di ossidazione vicino il Cr(II) è più reattivo. Ad esempio, CrCl3 solido è insolubile in acqua, ma si scioglie facilmente in presenza di un riducente che permetta la formazione di quantità catalitiche di Cr(II). Una volta sciolto in acqua si formano inizialmente i cationi complessi [Cr(H2O)4Cl2]+.
CrCl3 è un acido di Lewis, classificato duro secondo la teoria HSAB. Forma un gran numero di addotti del tipo [CrCl3L3]z, dove L è una base di Lewis. Ad esempio, reagisce con la piridina, C5H5N, per formare un addotto:
- CrCl3 + 3C5H5N → CrCl3(C5H5N)3
Fuso con cloruri dei metalli alcalini come il cloruro di potassio, CrCl3 forma complessi ottaedrici come K3CrCl6 e K3Cr2Cl9 (in questa ultima specie il cromo è ancora ottaedrico, ma ci sono tre ponti cloro che uniscono i due atomi di cromo).
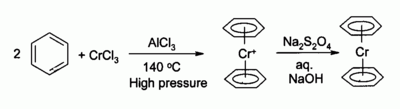
CrCl3 è usato come precursore di molti composti inorganici e complessi del cromo. Un esempio particolare è quello del dibenzenecromo, composto di struttura simile al ferrocene:
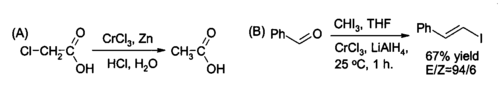
In sintesi organica il CrCl3 è usato per preparare in situ il cloruro di cromo(II), reagente molto usato per ridurre alogenuri alchilici e per la sintesi di alogenuri (E)-alchenilici. Di solito la reazione è condotta usando due moli di CrCl3 per ogni mole di litio alluminio idruro, ma se è possibile operare in ambiente acido acquoso possono bastare zinco e acido cloridrico:
CrCl3 è stato usato in reazioni organiche anche come acido di Lewis, ad esempio per catalizzare reazioni di Diels-Alder.[3]
Tricloruro di cromo esaidrato, CrCl3•6H2O[modifica | modifica wikitesto]
| Tricloruro di cromo | |
|---|---|
 | |
| Nome IUPAC | |
| Tricloruro di cromo esaidrato | |
| Nomi alternativi | |
| Cloruro di cromo(III) esaidrato | |
| Caratteristiche generali | |
| Formula bruta o molecolare | CrCl3•6H2O |
| Massa molecolare (u) | 266,45 g/mol |
| Aspetto | solido verde scuro |
| Numero CAS | |
| Numero EINECS | 233-038-3 |
| PubChem | 24808 |
| DrugBank | DB09129 |
| SMILES | Cl[Cr](Cl)Cl |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,76 (20 °C) |
| Solubilità in acqua | 58 g/100ml (20 °C) |
| Temperatura di fusione | 356 (83 °C) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| attenzione | |
| Frasi H | 302 |
| Consigli P | 262 [1] |
Le forme idrate si possono preparare sciogliendo il metallo in acido cloridrico. Alla formula CrCl3•6H2O corrispondono tre diversi composti, che costituiscono un caratteristico caso di isomeria detta "di idratazione", per via della diversa posizione dell'acqua dentro o fuori la sfera di coordinazione. Le formule di struttura sono:
- [Cr(H2O)4Cl2]Cl•2H2O di colore verde scuro, è la forma più comune, reperibile in commercio. I dati riportati nel riquadro a fianco si riferiscono a questo isomero.
- [Cr(H2O)5Cl]Cl2•H2O di colore verde chiaro;
- [Cr(H2O)6]Cl3 di colore violetto.
Dal punto di vista chimico le tre situazioni si possono distinguere per titolazione in soluzione acquosa con AgNO3, che provoca la precipitazione di 1, 2 o 3 ioni cloruro, rispettivamente.
L'isomero verde scuro è solubile in acqua e in alcool, insolubile in etere dietilico. Si usa come materiale di partenza per la sintesi di altri composti di cromo (anche coloranti). Viene inoltre usato come mordente nell'industria tessile. Sciolto in acqua, il catione complesso [Cr(H2O)4Cl2]+ reagisce lentamente: i leganti cloruro vengono sostituiti progressivamente dal solvente:
- [Cr(H2O)4Cl2]+ → [Cr(H2O)5Cl]2+ → [Cr(H2O)6]3+
Sicurezza[modifica | modifica wikitesto]
I composti di Cr(III) sono molto meno tossici di quelli di Cr(VI), tuttavia le varie forme di CrCl3 sono pericolose in caso di contatto con la pelle, ingestione o inalazione.[4][5]
Note[modifica | modifica wikitesto]
- ^ a b scheda del cloruro di cromo su IFA-GESTIS Archiviato il 16 ottobre 2019 in Internet Archive.
- ^ D. Nicholls, Complexes and first-row transition elements, London, Macmillan Press, 1975, ISBN 0-333-17088-1.
- ^ G. Calvet, M. Dussaussois, N. Blanchard e C. Kouklovsky, Lewis acid-promoted hetero Diels-Alder cycloaddition of α-acetoxynitroso dienophiles, in Org. Lett., vol. 6, n. 14, 2004, pp. 2449–2451, DOI:10.1021/ol0491336.
- ^ Scheda di sicurezza del CrCl3 anidro, su sciencelab.com. URL consultato il 29 gennaio 2011 (archiviato dall'url originale il 18 settembre 2012).
- ^ Scheda di sicurezza del CrCl3 esaidrato, su sciencelab.com. URL consultato il 29 gennaio 2011 (archiviato dall'url originale il 9 ottobre 2012).
Bibliografia[modifica | modifica wikitesto]
- N. N. Greenwood, A. Earnshaw, Chemistry of the elements, 2ª ed., Oxford, Butterworth-Heinemann, 1997, ISBN 0-7506-3365-4.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Tricloruro di cromo
Wikimedia Commons contiene immagini o altri file su Tricloruro di cromo