Metallocarbonile

Un metallocarbonile è un complesso formato da un metallo di transizione e da molecole di monossido di carbonio (CO) che, in questo contesto, si chiamano "carbonili", da cui anche il nome di questi complessi. I metallocarbonili omolettici, che cioè contengono solo ligandi CO, sono genericamente indicati come M(CO)n, mentre quelli che contengono anche altri ligandi sono indicati come LmM(CO)n-m, dove L dona formalmente al metallo due elettroni, come fa CO. Questo per i metallocarbonili mononucleari che contengono un solo centro metallico e sono i più semplici, ma sono noti anche molti complessi polinucleari, contenenti più centri metallici legati fra loro e/o tramite uno o più carbonili a ponte.
Si tratta generalmente di composti volatili e tossici, tossicità dovuta in parte alla formazione di carbossiemoglobina che non è in grado di legare l'ossigeno.[1] Tendono ad avere carattere apolare e ad essere incolori, ad eccezione dei metallocarbonili polinucleari che possono assumere colorazione variabile.
Tra i principali utilizzi spicca quello come catalizzatori in sintesi industriali.
Storia[modifica | modifica wikitesto]
Il primo metallocarbonile fu sintetizzato da Ludwig Mond, Carl Langer e Friedrich Quincke nel 1890.[2] I tre chimici scoprirono il tetracarbonilnichel durante le loro ricerche riguardanti la corrosione subita dalle valvole di nichel in contatto con gas contenenti CO.
Struttura[modifica | modifica wikitesto]

La formazione dei metallocarbonili rispetta generalmente la regola dei 18 elettroni, che corrisponde tipicamente alla condizione di massima stabilità dovuta al riempimento degli orbitali. Ad esempio, il cromo possiede 6 elettroni di valenza e necessita quindi di altri 12 elettroni: legandosi con 6 molecole di CO, ciascuna delle quali porta un contributo di 2 elettroni di valenza, forma il composto Cr(CO)6 con 18 elettroni sistemati negli orbitali a maggior carattere legante. Gli elementi dei gruppi 9 e 10 della tavola periodica tendono frequentemente a formare metallocarbonili con 18 elettroni di valenza, come nel caso di Ni(CO)4.
Il CO si lega all'atomo metallico tramite un legame σ e una retrodonazione π.
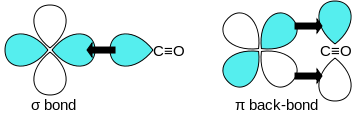
Il ligando dona elettroni utilizzando i suoi orbitali HOMO con simmetria σ. Il legame del complesso viene rafforzato dalla sovrapposizione degli orbitali d del metallo con il LUMO π* del CO. Quest'ultimo legame ha l'effetto di delocalizzare la densità elettronica dal metallo verso il ligando CO, il che spiega la prevalenza di numeri di ossidazione del metallo nulli o negativi. Il popolamento degli orbitali antileganti π* indebolisce il legame all'interno del monossido di carbonio.
Generalmente i metallocarbonili possiedono una struttura simmetrica in accordo con la teoria VSEPR. I complessi polinucleari, che cioè contengono più centri metallici, come nel caso di Mn2(CO)10, formano dei cluster[1][3] che vengono descritti indicando il numero di centri legati a ponte (utilizzando la lettera μ con a pedice il numero di atomi metallici) e l'apticità del monossido di carbonio (ovvero il numero di atomi utilizzati per il legame, si specifica con η2 quando è implicato anche l'atomo di ossigeno).
Metodi di indagine[modifica | modifica wikitesto]
I principali metodi di indagine sulla struttura dei metallocarbonili si basano sulla spettroscopia IR e sulla spettroscopia NMR C13. La maggioranza delle bande di stiramento del CO cade tra i 2100–1700 cm−1. Al crescere della carica diminuisce la frequenza di stiramento. A titolo illustrativo, si osservi la tabella riportata sotto.[4][5]
| Metallocarbonile | νCO (cm−1) |
|---|---|
| CO(g) | 2143 |
| [Mn(CO)6]+ | 2090 |
| Cr(CO)6 | 2000 |
| [V(CO)6]- | 1860 |
| [Ti(CO)6]2- | 1750 |
Nei cluster all'aumentare del numero di atomi metallici si osserva una diminuzione della frequenza di stiramento, corrispondendo anche l'aumento dei centri metallici a un ulteriore indebolimento del legame nel CO. Ciò è utile a distinguere il legame -C≡O terminale. Oltre alla frequenza a cui si registrano i picchi è utile anche osservare il numero di bande rilevabili dallo spettro IR, essendo tale numero legato al grado di simmetria del complesso.
Utile alla determinazione della struttura dei metallocarbonili è anche la spettroscopia NMR 13C, in quanto dal relativo spettro è possibile differenziare i ligandi CO non equivalenti. Il nucleo 13C del CO terminale risulta più schermato.
Sintesi[modifica | modifica wikitesto]
I principali metodi di sintesi dei metallocarbonili binari consistono nella combinazione diretta tra monossido di carbonio e metallo e nella carbonilazione riduttiva.
Combinazione diretta[modifica | modifica wikitesto]
Il tetracarbonilnichel, NI(CO)4, è il metallocarbonile più facilmente sintetizzabile per reazione diretta tra il metallo finemente suddiviso e il monossido di carbonio. Altri carbonili si formano più lentamente e richiedono condizioni elevate di temperatura e pressione:[6]
- Fe + 5 CO → Fe(CO)5 (a T=200 °C e P=200 atm)
- 2 Co + 8 CO → Co2(CO)8 (a T= 150 °C e P=35 atm)
Carbonilazione riduttiva[modifica | modifica wikitesto]
Per la sintesi dei carbonili della maggior parte dei metalli di transizione risulta più agevole ricorrere alla carbonilazione riduttiva. Si tratta di una reazione in cui il sale o un altro composto contenente il metallo viene fatto reagire con il CO in presenza di un agente riducente, rappresentato solitamente da sodio metallico, alluminio, LiAlH4, composti alluminioalchilici, o anche dallo stesso CO. In questo tipo di reazioni il metallo viene ridotto allo stato di ossidazione 0. Esempi di carbonilazioni riduttive sono:
- CrCl3 + Al + 6 CO → AlCl3 + Cr(CO)6
- Re2O7 + 17 CO → Re2(CO)10 + 7 CO2
Reazioni[modifica | modifica wikitesto]
Le reazioni più importanti dei metallocarbonili sono le sostituzioni, la migrazione alchilica, le ossidoriduzioni e le reazioni del ligando CO.
Sostituzioni[modifica | modifica wikitesto]
Il ligando CO è suscettibile alla sostituzione da parte di un nucleofilo attraverso un meccanismo dissociativo. Ad esempio, facendo reagire Cr(CO)6 con una trialchilfosfina (PR3) in solvente tetraidrofurano (THF), è possibile ottenere Cr(CO)5PR3 attraverso il seguente meccanismo che implica l'esistenza di un intermedio solvatato:
- Cr(CO)6 + THF Cr(CO)5(THF) + CO
- Cr(CO)5(THF) + PR3 → Cr(CO)5PR3 + THF
Un meccanismo alternativo è l'interscambio, un processo concertato:
- Cr(CO)6 + PR3 → [Cr(CO)6PR3]‡ → Cr(CO)5PR3 + CO
Questo genere di reazioni sono spesso promosse per via termica o fotochimica.
Migrazione alchilica[modifica | modifica wikitesto]
Nella migrazione alchilica un metallocarbonile che comprende come ligando un gruppo alchilico addiziona una molecola di CO generando un derivato acilico. Ad esempio:
- Mn(CO)5CH3 + CO → Mn(CO)4(COCH3)
Il meccanismo suggerito prevede la formazione di un intermedio in cui il gruppo alchilico si lega al carbonio del CO, con una molecola di solvente che prende il suo posto nella sfera di coordinazione del metallo.[7] Successivamente il solvente legato viene sostituito dal CO che si addiziona.
Ossidoriduzioni[modifica | modifica wikitesto]
La riduzione con sodio metallico permette di ottenere gli anioni altamente reattivi dei metallocarbonili:
- Fe(CO)5 + 2 Na → [Fe(CO)4]2- + CO + 2 Na+
Nella reazione appena descritta il ferro passa dallo stato di ossidazione 0 a quello -2. I carbonili polinucleari riducendosi tendono a scindersi:
- Os3(CO)12 + 6 Na → 3 [Os(CO)4]2- + 6 Na+
In presenza di una buona base di Lewis o di un forte nucleofilo è possibile che avvenga anche una dismutazione:
- 3 Fe(CO)5 + 4 OH- → [Fe3(CO)11]2- + CO32- + 2 H2O + 3 CO
Questi anioni protonandosi possono dare legami M-H, come nel caso di HMn(CO)5. Possono reagire anche con alogenuri alchilici o acilici, mentre con alogenuri organometallici si ha la formazione di un legame M-M:
- [Mn(CO)5]- + ReBr(CO)5 → (OC)5Mn-Re(CO)5 + Br-
L'ossidazione all'aria dei metallocarbonili produce l'ossido metallico e CO o CO2. L'ossidazione con un alogeno può essere invece sfruttata per produrre alogenuri organometallici:
- Mn2(CO)10 + Br2 → 2 MnBr(CO)5
Reazioni del ligando CO[modifica | modifica wikitesto]
In base al livello di polarizzazione del legame del ligando CO, l'atomo di carbonio di quest'ultimo è suscettibile di attacco da parte di nucleofili forti quali il litiometile:
- LiCH3 + Mo(CO)6 → (CO)5Mo=C(CH3)(O-Li+)
Il prodotto ottenuto dalla precedente reazione, noto anche come carbene di Fischer, può essere trasformato in un composto neutro ad esempio facendolo reagire con ioduro di metile:
- (CO)5Mo=C(CH3)(O-Li+) + CH3I → (CO)5Mo=C(CH3)(OCH3) + LiI
L'attacco nucleofilo di OH- produce invece la dismutazione già descritta in precedenza quando si è parlato delle ossidoriduzioni.
Il ligando CO può reagire anche tramite un attacco elettrofilo all'atomo di ossigeno, quando vi è apprezzabile densità elettronica localizzata su questo atomo:
- Cl(PR3)4ReCO + Al(CH3)3 → Cl(PR3)4ReCO + Al(CH3)3 · Al(CH3)3
Metallocarbonili come catalizzatori[modifica | modifica wikitesto]
I metallocarbonili sono un'importante classe di catalizzatori omogenei e precursori catalitici utilizzati in vari processi industriali. La tabella che segue elenca alcuni catalizzatori e il loro utilizzo specifico.[8]
| Catalizzatore | Applicazione catalitica |
|---|---|
| RhCl(PPh3)3 | Idrogenazione degli alcheni |
| cis-[Rh(CO)2I2]- | Processo Monsanto |
| HCo(CO)4 | Idroformilazione, isomerizzazione degli alcheni |
| HRh(CO)4 | Idroformilazione (solo per alcuni alcheni ramificati) |
| HRh(CO)(PPh3)3 | Idroformilazione |
| [Ru(CO)2I3]- | Omologazione degli acidi carbossilici |
| [HFe(CO)4]- | Reazione di spostamento del gas d'acqua |
| (η5-C5H5)2Ti(CH3)2 | Polimerizzazione degli alcheni |
| (η5-C5H5)2ZrH2 | Idrogenazione di alcheni e alchini |
| Pd(PPh3)4 | Molte applicazioni di laboratorio inclusa la reazione di Heck |
Note[modifica | modifica wikitesto]
- ^ a b Elschenbroich, C. ”Organometallics” (2006) Wiley-VCH: Weinheim. ISBN 978-3-527-29390-2
- ^ Shriver, p. 501.
- ^ P. J. Dyson, J. S. McIndoe, Transition Metal Carbonyl Cluster Chemistry, Gordon & Breach: Amsterdam (2000). ISBN 90-5699-289-9.
- ^ Nakamoto, Infrared and Raman spectra of inorganic and coordination compounds, Wiley, New York (1986)
- ^ Frerichs, S.R.; Stein, B.K.; Ellis, J.E.; J. Amer. chem. Soc., 109, 5558 (1987)
- ^ Shriver, p. 510.
- ^ Housecroft, Sharpe, p.720.
- ^ Tratta da Housecroft, Sharpe, p.722
Bibliografia[modifica | modifica wikitesto]
- D.F. Shriver, P.W Atkins; C.H. Langford, Chimica inorganica, Zanichelli, 1993, ISBN 978-88-08-12624-5.
- Catherine E. Housecroft, Alan G. Sharpe, Inorganic chemistry, 2ª ed., Pearson Education Limited, 2005, ISBN 0-13-039913-2.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Metallocarbonile
Wikimedia Commons contiene immagini o altri file su Metallocarbonile
Collegamenti esterni[modifica | modifica wikitesto]
- (EN) metal carbonyl, su Enciclopedia Britannica, Encyclopædia Britannica, Inc.
| Controllo di autorità | J9U (EN, HE) 987007556522605171 |
|---|
