Inositolo: differenze tra le versioni
Ho modificato il nome dell'inositolo da vitamina B8 a B7 |
Revisione della voce |
||
| Riga 77: | Riga 77: | ||
}} |
}} |
||
L''''inositolo''' (chiamato a volte anche vitamina B7) è un composto di origine biologica, strutturalmente simile al glucosio (anche se chimicamente non è uno zucchero) coinvolto in numero processi biologici tra cui quelli di signalling cellulare e come elemento strutturale. Può essere sia assunto con dieta che sintetizzato dal corpo umano, dove può presentare un grado più. In particolare, il mio-inositlo è la forma che non presenta gruppi fosforici legati. |
|||
L''''inositolo''' è un [[poliolo]] carbociclico la cui forma più importante in natura è il ''myo''-inositolo (''cis''-1,2,3,5-''trans''-4,6-cicloesanesolo). Altri [[isomeria|isomeri]] presenti occasionalmente in natura sono il ''scyllo''-, ''chiro''-, ''muco''-, ''neo''-inositolo. Altri isomeri possibili sono il ''allo''-, ''epi''-, ''cis''-inositolo. Non è uno zucchero, essendo i monosaccaridi, nella loro forma ciclica, [[emiacetale|emiacetali]] o [[emichetale|emichetali]] (struttura eterociclica contenente ossigeno). |
|||
== Chimica == |
|||
Con inositolo ci si riferisce ad una famiglia di molecole dalla struttura simile che differiscono per essere stereoisomeri. Chimicamente gli inositoli sono dei [[poliolo|polioli]] carbociclici, non sono uno zucchero essendo i monosaccaridi, nella loro forma ciclica, [[emiacetale|emiacetali]] o [[emichetale|emichetali]] (struttura eterociclica contenente ossigeno). La forma più importante in natura è il ''myo''-inositolo (''cis''-1,2,3,5-''trans''-4,6-cicloesanesolo) ma occasionalmnete si rilevano altri [[isomeria|isomeri]] confermazionali che differiscono solamente per il differente orientamento dei gruppi -OH, come ''scyllo''-, ''chiro''-, ''muco''-, ''neo''-inositolo. Altri isomeri possibili sono il ''allo''-, ''epi''-, ''cis''-inositolo. Quando ci si riferisce agli integratori alimentari, generalmente si intende il mio-inositolo. |
|||
Nella sua conformazione più stabile il mio-inositolo assume la conformazione a sedia, in cui 5 idrossili sono posti in conformazione equaotoriale ed 1 in conformazione assiale (quello in C2) che si presenta come una polvere di bassa palpabilità, di colore bianco niveo, inodore, dal sapore lievemente dolce. |
|||
== Presenza in natura e sintesi == |
== Presenza in natura e sintesi == |
||
L'inositolo si trova in molti alimenti, in particolare nei cereali, nelle noci, nella frutta specialmente in meloni ed arance. L'inositolo non è |
L'inositolo si trova in molti alimenti, in particolare nei cereali, nelle noci, nella frutta specialmente in meloni ed arance dove si ritrova molto spesso essi insolubili di difficile assorbimento, per questo motivo l'inositolo contentuto negli alimenti è spesso scarsamente asssorbibile. L'inositolo non è in realtà una vitamina (anche se è spesso conosciuto come Vitamina B7), perchè a differenza di queste, l'organismo è in grado di sintetizzarlo in quantità sufficiente per cui ricade nella classe delle pseudovitamine nel [[Vitamina B|complesso B]]. |
||
Il ''mio''-Inositolo è sintetizzato a partire dal glucosio-6 fosfato in due passaggi: il primo, catalizzato da una inositolo-3 fosfato sintasi (come ISYNA1) lo converte in mio-inositolo-1 fosfato, che viene poi defosforilato a mio-inositolo da una fosfatasi. Negli umani la maggior parte dell'inositolo, generralmente alcuni grammi al giorni) viene sintetizzato nei reni. |
|||
Il mioinositolo è classificato come un componente del [[Vitamina B|complesso B]] (riferendosi ad esso come B7) ed è sintetizzato dal corpo umano. Si presenta come una polvere di bassa palpabilità, di colore bianco niveo, inodore, dal sapore lievemente dolce. È utilizzato anche come integratore nelle attività sportive, in particolare per l'attivazione di alcune funzioni epatiche. Ad oggi non è iscritto tra le sostanze dopanti. |
|||
=== Acido fitico === |
|||
L'[[acido fitico]] (IP6 o fitato), è un derivato dell'inositolo formato da una mlecola di inositolo a cui sono legati gruppi fosfato al posto degli -OH e rappresenta la principale forma di stoccaggio di fosforo inorganico in molte pecie vegetali, specie nei semi.<ref name="phytochemicals">[http://www.phytochemicals.info/phytochemicals/phytic-acid.php Phytic acid]</ref> L'acido fitico è inassorbibile dagli organismi superiori, a parte i ruminanti, perchè non possiedono nel loro apparato digestivo i batteri e gli enzimi in grado di degradare questo composto. Inoltre l'acido fitico, per via della sua capacità di legare ioni metallici come calcio, magnesio, zinco e ferro, può esacerbare stati di carenza di minerali in soggetti predisposti che mangiano grandi quantità di vegetali (come accade ad esempio nei paesi in via di sviluppo).<ref>{{cite journal|vauthors=Hurrell RF|title=Influence of vegetable protein sources on trace element and mineral bioavailability|journal=The Journal of Nutrition|volume=133|issue=9|pages=2973S–7S|year=2003|pmid=12949395|url=http://jn.nutrition.org/cgi/pmidlookup?view=long&pmid=12949395}}</ref><ref>{{Cite book|chapter=Phytates|title=Toxicants Occurring Naturally in Foods|author=Committee on Food Protection|author2=Food and Nutrition Board|author3=National Research Council|publisher=National Academy of Sciences|year=1973|isbn=978-0-309-02117-3|pages=363–371|url=https://books.google.com/books?id=lIsrAAAAYAAJ&pg=PA363}}</ref> |
|||
[[File:Inositol biosintesi.png|centro|miniatura|800x800px|Sintesi del mio-inositolo]] |
|||
== Ruolo biologico e applicazioni == |
== Ruolo biologico e applicazioni == |
||
L'inositolo ed i suoi derivati partecipano a numerosi e fondamentali processi biologici, quali: |
|||
* Trasduzione del segnale dell'insulina [[Insulin]] <ref name="Larner J 2002 47–60">{{cite journal |vauthors=Larner J |title=D-chiro-inositol--its functional role in insulin action and its deficit in insulin resistance |journal=International Journal of Experimental Diabetes Research |volume=3 |issue=1 |pages=47–60 |year=2002 |pmid=11900279 |pmc=2478565 |doi=10.1080/15604280212528 }}</ref> |
|||
La struttura dell'inositolo gioca un ruolo fondamentale nei messaggeri secondari in cellule eucariotiche, come inositolo fosfato o come [[lipidi]] [[fosfatidilinositolo]] (PI) e fosfatidilinositolofosfato (PIP). |
|||
* Formazione del [[citoscheletro]] |
|||
* Sistema nervoso ([[epsina]]) |
|||
* Controllo della concentrazione di calcio intracellulare <ref>{{cite journal |vauthors=Gerasimenko JV, Flowerdew SE, Voronina SG, Sukhomlin TK, Tepikin AV, Petersen OH, Gerasimenko OV |title=Bile acids induce Ca2+ release from both the endoplasmic reticulum and acidic intracellular calcium stores through activation of inositol trisphosphate receptors and ryanodine receptors |journal=The Journal of Biological Chemistry |volume=281 |issue=52 |pages=40154–63 |year=2006 |pmid=17074764 |doi=10.1074/jbc.M606402200 }}</ref> |
|||
* Mantenimento del potenziale di membrana cellulare <ref name="pmid9017197">{{cite journal |vauthors=Kukuljan M, Vergara L, Stojilkovic SS |title=Modulation of the kinetics of inositol 1,4,5-trisphosphate-induced [Ca2+]i oscillations by calcium entry in pituitary gonadotrophs |journal=Biophysical Journal |volume=72 |issue=2 Pt 1 |pages=698–707 |year=1997 |pmid=9017197 |pmc=1185595 |doi=10.1016/S0006-3495(97)78706-X |bibcode=1997BpJ....72..698K }}</ref> |
|||
* Degradazione dei grassi <ref name="pmid3103610">{{cite journal |vauthors=Rapiejko PJ, Northup JK, Evans T, Brown JE, Malbon CC |title=G-proteins of fat-cells. Role in hormonal regulation of intracellular inositol 1,4,5-trisphosphate |journal=The Biochemical Journal |volume=240 |issue=1 |pages=35–40 |year=1986 |pmid=3103610 |pmc=1147372 |url=http://www.biochemj.org/cgi/pmidlookup?view=long&pmid=3103610 }}</ref> |
|||
* Regolazione dell'espressione genica <ref>{{cite journal |vauthors=Shen X, Xiao H, Ranallo R, Wu WH, Wu C |title=Modulation of ATP-dependent chromatin-remodeling complexes by inositol polyphosphates |journal=Science |volume=299 |issue=5603 |pages=112–4 |year=2003 |pmid=12434013 |doi=10.1126/science.1078068 }}</ref><ref>{{cite journal |vauthors=Steger DJ, Haswell ES, Miller AL, Wente SR, O'Shea EK |title=Regulation of chromatin remodeling by inositol polyphosphates |journal=Science |volume=299 |issue=5603 |pages=114–6 |year=2003 |pmid=12434012 |pmc=1458531 |doi=10.1126/science.1078062 }}</ref> |
|||
Dalla sua fosforilazione si possono ottenere fino a 70 diverse molecole (raccolti in dei gruppi in base al numero di gruppi fosfato presenti, IP1-IP9), ognuno con un diverso ruolo nel signalling intracellulare. Inoltre possono essere legate a numerosi altri composti come ad esempio i lipidi, per formare i fosfatidilinositoli polifosfati.<ref>{{Cita pubblicazione|nome=Marine L.|cognome=Croze|data=October 2013|titolo=Potential role and therapeutic interests of myo-inositol in metabolic diseases|rivista=Biochimie|volume=95|numero=10|pp=1811–1827|accesso=2017-06-24|doi=10.1016/j.biochi.2013.05.011|url=http://www.ncbi.nlm.nih.gov/pubmed/23764390|nome2=Christophe O.|cognome2=Soulage}}</ref> |
|||
=== Farmacologia === |
|||
Il myo-inositolo in studi a [[doppio cieco]] è risultato efficace nel trattamento del [[disturbo ossessivo-compulsivo]]. La sua efficacia è equiparabile a quella degli [[SSRI]] ed è virtualmente privo di effetti collaterali.<ref>{{cita pubblicazione |
|||
L'Inositolo è assorbito mediante un sistema di co-trasporto sodio dipendente che media anche l'assorbimento di glucosio (l'integrazione di inositolo si è infatti dimostrata in grado di limitare quella di glucosio).<ref>{{Cita pubblicazione|nome=Michael J.|cognome=Coady|data=2002-09-20|titolo=Identification of a novel Na+/myo-inositol cotransporter|rivista=The Journal of Biological Chemistry|volume=277|numero=38|pp=35219–35224|accesso=2017-06-24|doi=10.1074/jbc.M204321200|url=http://www.ncbi.nlm.nih.gov/pubmed/12133831|nome2=Bernadette|cognome2=Wallendorff|nome3=Dominique G.|cognome3=Gagnon}}</ref> L'applicazione di soft gel all'inositolo (delle capsule riempite di liquido in modo da eliminare steps limitanti come la dissoluzione) ha permesso di incrementare notevolmente la biodisponibilità orale del composto del 30%.<ref>{{Cita pubblicazione|nome=Gianfranco|cognome=Carlomagno|data=March 2012|titolo=Myo-inositol in a new pharmaceutical form: a step forward to a broader clinical use|rivista=Expert Opinion on Drug Delivery|volume=9|numero=3|pp=267–271|accesso=2017-06-24|doi=10.1517/17425247.2012.662953|url=http://www.ncbi.nlm.nih.gov/pubmed/22339497|nome2=Sara|cognome2=De Grazia|nome3=Vittorio|cognome3=Unfer}}</ref> |
|||
Dopo l'ingestione, l'inositolo raggiunge il picco plasmatico in circa 2-3 ore.<ref>{{Cita pubblicazione|nome=Gianfranco|cognome=Carlomagno|data=March 2012|titolo=Myo-inositol in a new pharmaceutical form: a step forward to a broader clinical use|rivista=Expert Opinion on Drug Delivery|volume=9|numero=3|pp=267–271|accesso=2017-06-24|doi=10.1517/17425247.2012.662953|url=http://www.ncbi.nlm.nih.gov/pubmed/22339497|nome2=Sara|cognome2=De Grazia|nome3=Vittorio|cognome3=Unfer}}</ref> Nell'organismo viene convertito rapidamente in alcuni isomeri come epi- e D-chiro- da delle epimerasi, alcune delle quali risultano essere presenti in bassa quantità nei soggetti con insulino resistenza, e che vengono saturarate rapidamente da dosi medie (alcuni grammi) del composto.<ref>{{Cita pubblicazione|nome=Joseph|cognome=Larner|data=2002|titolo=D-chiro-inositol--its functional role in insulin action and its deficit in insulin resistance|rivista=International Journal of Experimental Diabetes Research|volume=3|numero=1|pp=47–60|accesso=2017-06-24|doi=10.1080/15604280212528|url=http://www.ncbi.nlm.nih.gov/pubmed/11900279}}</ref> L'inositolo ha mostrato efficacia in alcuni disturbi psichiatrici ma ha una bassa permeabilità nella barriera ematoencefalica (meno del 3% della concentrazione del composto circolante riesce ad attraversarla)<ref>{{Cita pubblicazione|nome=R.|cognome=Spector|data=August 1988|titolo=Myo-inositol transport through the blood-brain barrier|rivista=Neurochemical Research|volume=13|numero=8|pp=785–787|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/3173626}}</ref>, che però tende ad aumentare nel corso di un trattamento continuato: il trattamento con 12 g al giorno del composto ha comportato un aumento del 70% dei livelli di inositolo nel fluido cererbrospinale di pazienti. <ref>{{Cita pubblicazione|nome=J.|cognome=Levine|data=1993-11-05|titolo=Inositol treatment raises CSF inositol levels|rivista=Brain Research|volume=627|numero=1|pp=168–170|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/8293297|nome2=A.|cognome2=Rapaport|nome3=L.|cognome3=Lev}}</ref> |
|||
=== Usi terapeutici === |
|||
La struttura dell'inositolo gioca un ruolo fondamentale nei messaggeri secondari in cellule eucariotiche, come inositolo fosfato o come [[lipidi]] [[fosfatidilinositolo]] (PI) e fosfatidilinositolofosfato (PIP). Questa sua prorpietà sembra essere la responsabile dei suoi effetti teraputici, alcuni dei quali provati anche in test clinici su pazienti. Il mio inositolo è considerato come un composto sicuro ed è inoltre idrosolubile (al pari di altri composti del complesso delle vitamine B) che ne previene un eccessivo accumulo. La sua deplezione alimentare non sembra causare stati patologici, proprio grazie alla capacità del corpo di sintetizzarlo, ma la sua integrazione si è mostrata capace di agire su diverse patologie, in particolare disturbi d'ansia, sindrome dell'ovaio policistico, sindromi metaboliche senza causare effetti collaterali rilevanti (si possono presentare disturbi gastro intestinali nel 5% dei pazienti specie ai dosaggi piu alti). |
|||
==== Sistema nervoso centrale ==== |
|||
L'inositolo ed i suoi derivati sembrano giocare un ruolo fondamentale nell'equilibrio del sistema nervoso centrale, anche se le sue numerosi implicazioni non sono state ancora del tutto delucidate. Bassi livelli di mio-inositolo sono stati rilevati nel cervello di pazienti depressi e di suicidi;<ref>{{Cita pubblicazione|nome=H.|cognome=Shimon|data=August 1997|titolo=Reduced frontal cortex inositol levels in postmortem brain of suicide victims and patients with bipolar disorder|rivista=The American Journal of Psychiatry|volume=154|numero=8|pp=1148–1150|accesso=2017-06-24|doi=10.1176/ajp.154.8.1148|url=http://www.ncbi.nlm.nih.gov/pubmed/9247405|nome2=G.|cognome2=Agam|nome3=R. H.|cognome3=Belmaker}}</ref> i sali di litio, uno dei trattamenti di prima linea per il disturbo bipolare, vanno tra le altre cose ad alterare i livelli di inositoli nel cervello.<ref>{{Cita pubblicazione|nome=H. K.|cognome=Manji|data=October 1996|titolo=Modulation of protein kinase C isozymes and substrates by lithium: the role of myo-inositol|rivista=Neuropsychopharmacology: Official Publication of the American College of Neuropsychopharmacology|volume=15|numero=4|pp=370–381|accesso=2017-06-24|doi=10.1016/0893-133X(95)00243-7|url=http://www.ncbi.nlm.nih.gov/pubmed/8887991|nome2=Y.|cognome2=Bersudsky|nome3=G.|cognome3=Chen}}</ref> Perciò il mio-inositolo è stato sperimentato nel trattamento di diverse patologie psichiatriche.<ref>{{Cita pubblicazione|nome=J.|cognome=Levine|data=May 1997|titolo=Controlled trials of inositol in psychiatry|rivista=European Neuropsychopharmacology: The Journal of the European College of Neuropsychopharmacology|volume=7|numero=2|pp=147–155|accesso=2017-06-24|url=https://www.ncbi.nlm.nih.gov/pubmed/9169302}}</ref> |
|||
===== Disturbi depressivi ed ansia ===== |
|||
Sembra avere qualche efficacia nel trattamento della depressione (a dosaggi superiori a 12 g\giorno) dove in alcuni studi ha mostrato una diminuzione statisticamente significativa rispetto al placebo dei sintomi (da 33.4 a 21.6 in media nei pazienti trattati con inositolo, rispetto 32.9 to 28.9 nel gruppo placebo placebo misurati con la scala HDS secondo i risultati di uno studio).<ref>{{Cita pubblicazione|nome=J.|cognome=Levine|data=May 1995|titolo=Double-blind, controlled trial of inositol treatment of depression|rivista=The American Journal of Psychiatry|volume=152|numero=5|pp=792–794|accesso=2017-06-24|doi=10.1176/ajp.152.5.792|url=http://www.ncbi.nlm.nih.gov/pubmed/7726322|nome2=Y.|cognome2=Barak|nome3=M.|cognome3=Gonzalves}}</ref><ref>{{Cita pubblicazione|nome=J.|cognome=Levine|data=1995|titolo=Follow-up and relapse analysis of an inositol study of depression|rivista=The Israel Journal of Psychiatry and Related Sciences|volume=32|numero=1|pp=14–21|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/7622343|nome2=Y.|cognome2=Barak|nome3=O.|cognome3=Kofman}}</ref> Alcuni pazienti che non hanno risposto al trattamento con inositolo hanno trovato beneficio con un SSRI, ma l'aggiunta di inositolo ad un SSRI non sembra fornire benefici aggiuntivi all'effetto dell'antidepressivo.<ref>{{Cita pubblicazione|nome=B.|cognome=Nemets|data=1999|titolo=Inositol addition does not improve depression in SSRI treatment failures|rivista=Journal of Neural Transmission (Vienna, Austria: 1996)|volume=106|numero=7-8|pp=795–798|accesso=2017-06-24|doi=10.1007/s007020050200|url=http://www.ncbi.nlm.nih.gov/pubmed/10907738|nome2=A.|cognome2=Mishory|nome3=J.|cognome3=Levine}}</ref><ref>{{Cita pubblicazione|nome=J.|cognome=Levine|data=1999-02-01|titolo=Combination of inositol and serotonin reuptake inhibitors in the treatment of depression|rivista=Biological Psychiatry|volume=45|numero=3|pp=270–273|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/10023500|nome2=A.|cognome2=Mishori|nome3=M.|cognome3=Susnosky}}</ref> |
|||
Il myo-inositolo (al dosaggio di 18 g\giorno) in studi in [[doppio cieco]] è risultato efficace nel trattamento del [[disturbo ossessivo-compulsivo]] quanto gli SSRI, dei farmaci antidepressivi utilizzati come trattamento per questa patologia, ma a differenza di questi è risultato virtualmente privo di effetti collaterali.<ref>{{Cita pubblicazione|nome=S.|cognome=Seedat|data=November 1999|titolo=Inositol augmentation of serotonin reuptake inhibitors in treatment-refractory obsessive-compulsive disorder: an open trial|rivista=International Clinical Psychopharmacology|volume=14|numero=6|pp=353–356|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/10565802|nome2=D. J.|cognome2=Stein}}</ref><ref>{{cita pubblicazione |
|||
|autore=Fux M, Levine J, Aviv A, Belmaker RH |
|autore=Fux M, Levine J, Aviv A, Belmaker RH |
||
|titolo=Inositol treatment of obsessive-compulsive disorder |
|titolo=Inositol treatment of obsessive-compulsive disorder |
||
| Riga 99: | Riga 131: | ||
|pmid=8780431 |
|pmid=8780431 |
||
}} |
}} |
||
</ref> |
|||
</ref> Tuttavia la quantità impiegata era di 18 grammi al giorno per 6 settimane: non vi sono ancora studi sui possibili effetti per periodi più prolungati. |
|||
In un altro studio, inositolo al dosaggio di 18 grammi al giorno, è risultato efficacie quanto fluvoxamina (un antidepressivo SSRI) nel trattamento del disturbo da attacchi di panico.<ref>{{Cita pubblicazione|nome=A.|cognome=Palatnik|data=June 2001|titolo=Double-blind, controlled, crossover trial of inositol versus fluvoxamine for the treatment of panic disorder|rivista=Journal of Clinical Psychopharmacology|volume=21|numero=3|pp=335–339|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/11386498|nome2=K.|cognome2=Frolov|nome3=M.|cognome3=Fux}}</ref> Sembra che anche una dose minore (di 12 g\giorno) possa avere una qualche efficacia.<ref>{{Cita pubblicazione|nome=J.|cognome=Benjamin|data=July 1995|titolo=Double-blind, placebo-controlled, crossover trial of inositol treatment for panic disorder|rivista=The American Journal of Psychiatry|volume=152|numero=7|pp=1084–1086|accesso=2017-06-24|doi=10.1176/ajp.152.7.1084|url=http://www.ncbi.nlm.nih.gov/pubmed/7793450|nome2=J.|cognome2=Levine|nome3=M.|cognome3=Fux}}</ref> Sembra che la sua efficacia come ansiolitico dipenda dalla gravità iniziale della patologia, fornendo i benefici maggiori nei pazienti con disturbo grave.<ref>{{Cita pubblicazione|nome=O.|cognome=Kofman|data=2000|titolo=The anxiolytic effect of chronic inositol depends on the baseline level of anxiety|rivista=Journal of Neural Transmission (Vienna, Austria: 1996)|volume=107|numero=2|pp=241–253|accesso=2017-06-24|doi=10.1007/s007020050020|url=http://www.ncbi.nlm.nih.gov/pubmed/10847563|nome2=H.|cognome2=Einat|nome3=H.|cognome3=Cohen}}</ref> |
|||
===== Disturbo disforico mestruale ===== |
|||
Il disturbo disforico premestruale è un disordine dell'umore associato alla sindrome premestruale.<ref>{{Cita pubblicazione|nome=I.|cognome=Zukov|data=2010|titolo=Premenstrual dysphoric disorder--review of actual findings about mental disorders related to menstrual cycle and possibilities of their therapy|rivista=Prague Medical Report|volume=111|numero=1|pp=12–24|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/20359434|nome2=R.|cognome2=Ptácek|nome3=J.|cognome3=Raboch}}</ref> Lintegrazione di 4 g di inositolo 3 volte al giorno ha mostrato in uno studio di diminuire i disturbi dell'umore e di depressione ed ansia in maniera statisticamente significativa, questi effetti benefici si sono mantenuti per i 6 mesi del trattamento. Tuttavia non sono stati condotti numerosi studi per replicare i risultati.<ref>{{Cita pubblicazione|nome=Carlomagno|cognome=Gianfranco|data=October 2011|titolo=Myo-inositol in the treatment of premenstrual dysphoric disorder|rivista=Human Psychopharmacology|volume=26|numero=7|pp=526–530|accesso=2017-06-24|doi=10.1002/hup.1241|url=http://www.ncbi.nlm.nih.gov/pubmed/22031267|nome2=Unfer|cognome2=Vittorio|nome3=Buffo|cognome3=Silvia}}</ref> |
|||
L'inositolo è stato sperimentato anche nel trattamento di disturbo post traumatico da stress,<ref>{{Cita pubblicazione|nome=Z.|cognome=Kaplan|data=1996|titolo=Inositol treatment of post-traumatic stress disorder|rivista=Anxiety|volume=2|numero=1|pp=51–52|accesso=2017-06-24|doi=10.1002/(SICI)1522-7154(1996)2:13.0.CO;2-G|url=http://www.ncbi.nlm.nih.gov/pubmed/9160600|nome2=M.|cognome2=Amir|nome3=M.|cognome3=Swartz}}</ref> disturbo bipolare,<ref>{{Cita pubblicazione|nome=Andrew A.|cognome=Nierenberg|data=February 2006|titolo=Treatment-resistant bipolar depression: a STEP-BD equipoise randomized effectiveness trial of antidepressant augmentation with lamotrigine, inositol, or risperidone|rivista=The American Journal of Psychiatry|volume=163|numero=2|pp=210–216|accesso=2017-06-24|doi=10.1176/appi.ajp.163.2.210|url=http://www.ncbi.nlm.nih.gov/pubmed/16449473|nome2=Michael J.|cognome2=Ostacher|nome3=Joseph R.|cognome3=Calabrese}}</ref> schizofrenia<ref>{{Cita pubblicazione|nome=J.|cognome=Levine|data=1993 Apr 15-May 1|titolo=Lack of effect of inositol treatment in chronic schizophrenia|rivista=Biological Psychiatry|volume=33|numero=8-9|pp=673–675|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/8329500|nome2=R.|cognome2=Umansky|nome3=G.|cognome3=Ezrielev}}</ref> e per il morbo di Alzheimer<ref>{{Cita pubblicazione|nome=Y.|cognome=Barak|data=May 1996|titolo=Inositol treatment of Alzheimer's disease: a double blind, cross-over placebo controlled trial|rivista=Progress in Neuro-Psychopharmacology & Biological Psychiatry|volume=20|numero=4|pp=729–735|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/8843494|nome2=J.|cognome2=Levine|nome3=A.|cognome3=Glasman}}</ref><ref>{{Cita pubblicazione|nome=S.|cognome=Salloway|data=2011-09-27|titolo=A phase 2 randomized trial of ELND005, scyllo-inositol, in mild to moderate Alzheimer disease|rivista=Neurology|volume=77|numero=13|pp=1253–1262|accesso=2017-06-24|doi=10.1212/WNL.0b013e3182309fa5|url=http://www.ncbi.nlm.nih.gov/pubmed/21917766|nome2=R.|cognome2=Sperling|nome3=R.|cognome3=Keren}}</ref> non mostrando però in questi casi efficacia significativa. |
|||
==== Sindrome metabolica e diabete ==== |
|||
La [[sindrome metabolica]] è una patologia complessa e multifattoriale nella quale diversi fattori fra loro correlati concorrono ad aumentare la possibilità di sviluppare patologie a carico dell'[[apparato circolatorio]] e [[diabete]]. |
|||
L'inositolo fa parte di una serie di composti che attivano la risposta dell'insulina all'interno della cellula<ref>{{Cita pubblicazione|nome=A. R.|cognome=Saltiel|data=March 1990|titolo=Second messengers of insulin action|rivista=Diabetes Care|volume=13|numero=3|pp=244–256|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/2137771}}</ref> (è uno dei principali messaggeri secondari) di cui fanno parte i "fosfoglicani legati all'inositolo" di tipo A (IGP-A) e quelli di tipo P (IGP-P o D-chiro-inositolo legato a galattosamine).<ref>{{Cita pubblicazione|nome=H. N.|cognome=Caro|data=August 1997|titolo=Isolation and partial characterisation of insulin-mimetic inositol phosphoglycans from human liver|rivista=Biochemical and Molecular Medicine|volume=61|numero=2|pp=214–228|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/9259987|nome2=S.|cognome2=Kunjara|nome3=T. W.|cognome3=Rademacher}}</ref> Questi composti hanno delle funzioni opposte all'interno del metabolismo e tendono ad antagonizzarsi, per cui il loro bilancio è essenziale al corretto funzionamento dell'organismo e l'insulino resistenza è associata ad uno sbilanciamento di questi sistemi.<ref>{{Cita pubblicazione|nome=S.|cognome=Kunjara|data=December 1999|titolo=Inositol phosphoglycans in diabetes and obesity: urinary levels of IPG A-type and IPG P-type, and relationship to pathophysiological changes|rivista=Molecular Genetics and Metabolism|volume=68|numero=4|pp=488–502|accesso=2017-06-24|doi=10.1006/mgme.1999.2936|url=http://www.ncbi.nlm.nih.gov/pubmed/10607479|nome2=D. Y.|cognome2=Wang|nome3=A. L.|cognome3=Greenbaum}}</ref> L'inositolo sembra agire normalizzando il rapporto tra questi composti.<ref>{{Cita pubblicazione|nome=J.|cognome=Larner|data=March 2001|titolo=D-chiro-inositol in insulin action and insulin resistance-old-fashioned biochemistry still at work|rivista=IUBMB life|volume=51|numero=3|pp=139–148|accesso=2017-06-24|doi=10.1080/152165401753544205|url=http://www.ncbi.nlm.nih.gov/pubmed/11547915}}</ref> |
|||
L'insulina promuove l'ingresso di glucosio nelle cellule anche attraverso la mobilitazione delle riserve vescicolari dei trasportatori del glucosio (GluT4), delle proteine trasportatrici di membrana che grazie all'attivazione di una serie di messaggeri chimici, di cui fanno parte dei derivati fosforilati dell'inositolo come il PIP3, vengono trasportati nella membrana.<ref>{{Cita pubblicazione|nome=Anne M.|cognome=Kong|data=August 2006|titolo=Phosphatidylinositol 3-phosphate [PtdIns3P] is generated at the plasma membrane by an inositol polyphosphate 5-phosphatase: endogenous PtdIns3P can promote GLUT4 translocation to the plasma membrane|rivista=Molecular and Cellular Biology|volume=26|numero=16|pp=6065–6081|accesso=2017-06-24|doi=10.1128/MCB.00203-06|url=http://www.ncbi.nlm.nih.gov/pubmed/16880518|nome2=Kristy A.|cognome2=Horan|nome3=Absorn|cognome3=Sriratana}}</ref><ref>{{Cita pubblicazione|nome=Akihiko|cognome=Taguchi|data=2008-05-16|titolo=Identification of Glypican3 as a novel GLUT4-binding protein|rivista=Biochemical and Biophysical Research Communications|volume=369|numero=4|pp=1204–1208|accesso=2017-06-24|doi=10.1016/j.bbrc.2008.03.027|url=http://www.ncbi.nlm.nih.gov/pubmed/18343214|nome2=Masahiro|cognome2=Emoto|nome3=Shigeru|cognome3=Okuya}}</ref> In dei modelli animali, l'ingestione di inositolo ha promosso l'espressione dei trasportatori del glucosio e quindi dimiuito l'insulino resistenza.<ref>{{Cita pubblicazione|nome=Yoko|cognome=Yamashita|data=2013-05-22|titolo=Detection of orally administered inositol stereoisomers in mouse blood plasma and their effects on translocation of glucose transporter 4 in skeletal muscle cells|rivista=Journal of Agricultural and Food Chemistry|volume=61|numero=20|pp=4850–4854|accesso=2017-06-24|doi=10.1021/jf305322t|url=http://www.ncbi.nlm.nih.gov/pubmed/23641877|nome2=Masaru|cognome2=Yamaoka|nome3=Tomohisa|cognome3=Hasunuma}}</ref>Inoltre l'integrazione con inositolo 10g\giorno si è mostrata in grado di diminuire il colesterolo LDL nelle persone con sindrome metabolica (ma non nei pazienti che non la hanno) probabilmente come effetto secondario all'aumento di particolari lipoproteine prodotte dai reni (i plasmalogeni) la cui quantitò tende a diminuire con l'età e in soggetti con iperlipidemie.<ref>{{Cita pubblicazione|nome=Ryouta|cognome=Maeba|data=June 2008|titolo=Myo-inositol treatment increases serum plasmalogens and decreases small dense LDL, particularly in hyperlipidemic subjects with metabolic syndrome|rivista=Journal of Nutritional Science and Vitaminology|volume=54|numero=3|pp=196–202|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/18635905|nome2=Hiroshi|cognome2=Hara|nome3=Hiroshi|cognome3=Ishikawa}}</ref><ref>{{Cita pubblicazione|nome=Ryouta|cognome=Maeba|data=February 2007|titolo=Plasmalogens in human serum positively correlate with high- density lipoprotein and decrease with aging|rivista=Journal of Atherosclerosis and Thrombosis|volume=14|numero=1|pp=12–18|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/17332687|nome2=Tomomi|cognome2=Maeda|nome3=Makoto|cognome3=Kinoshita}}</ref> |
|||
In uno studio, in delle donne con sindrome metabolica post menopausa, l'integrazione con inositolo alla dose di 2 grammi al giorno ha causato il miglioramento dei marker metabolici per la malattia (livelli di insulina, glucosio ed insulino resistenza) che si sono mantenuti durane te tutta la durata dello studio (un anno) mostrando anzi un lieve ulteriore miglioramento nel corso dei mesi.<ref>{{Cita pubblicazione|nome=Domenico|cognome=Giordano|data=January 2011|titolo=Effects of myo-inositol supplementation in postmenopausal women with metabolic syndrome: a perspective, randomized, placebo-controlled study|rivista=Menopause (New York, N.Y.)|volume=18|numero=1|pp=102–104|accesso=2017-06-24|doi=10.1097/gme.0b013e3181e8e1b1|url=http://www.ncbi.nlm.nih.gov/pubmed/20811299|nome2=Francesco|cognome2=Corrado|nome3=Angelo|cognome3=Santamaria}}</ref> <ref>{{Cita pubblicazione|nome=A.|cognome=Santamaria|data=October 2012|titolo=One-year effects of myo-inositol supplementation in postmenopausal women with metabolic syndrome|rivista=Climacteric: The Journal of the International Menopause Society|volume=15|numero=5|pp=490–495|accesso=2017-06-24|doi=10.3109/13697137.2011.631063|url=http://www.ncbi.nlm.nih.gov/pubmed/22192068|nome2=D.|cognome2=Giordano|nome3=F.|cognome3=Corrado}}</ref> Usato al dosaggio di 4g\giorno, in uno studio ha mostrato di diminuire i marker di diabete gestionale nelle donne incinte (in particolare livelli di glucosio ed insulino resistenza) <ref>{{Cita pubblicazione|nome=F.|cognome=Corrado|data=August 2011|titolo=The effect of myoinositol supplementation on insulin resistance in patients with gestational diabetes|rivista=Diabetic Medicine: A Journal of the British Diabetic Association|volume=28|numero=8|pp=972–975|accesso=2017-06-24|doi=10.1111/j.1464-5491.2011.03284.x|url=http://www.ncbi.nlm.nih.gov/pubmed/21414183|nome2=R.|cognome2=D'Anna|nome3=G.|cognome3=Di Vieste}}</ref> e di diminuire il rischio di sviluppo di diabete gestionale nelle donne con ovaio policistico dal 52% al 17,2%, senza però influire sull'andamento della gravidanza.<ref>{{Cita pubblicazione|nome=R.|cognome=D'Anna|data=June 2012|titolo=Myo-inositol may prevent gestational diabetes in PCOS women|rivista=Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology|volume=28|numero=6|pp=440–442|accesso=2017-06-24|doi=10.3109/09513590.2011.633665|url=http://www.ncbi.nlm.nih.gov/pubmed/22122627|nome2=V.|cognome2=Di Benedetto|nome3=P.|cognome3=Rizzo}}</ref><ref>{{Cita pubblicazione|nome=G.|cognome=Carlomagno|data=August 2011|titolo=Inositol safety: clinical evidences|rivista=European Review for Medical and Pharmacological Sciences|volume=15|numero=8|pp=931–936|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/21845803|nome2=V.|cognome2=Unfer}}</ref> |
|||
==== Sindrome dell'ovaio policistico ==== |
|||
Molto promettenti ed ormai numericamente consistenti sono gli studi che dimostrano l'utilità dell'inositolo, ed in particolare del D-chiro-inositolo (DCI), nel trattamento della sindrome dell'[[ovaio policistico]] (PCOS), una sindrome caratterizzata tra l'altro da scarso controllo del glucosio ematico, iperandrogenismo, squilibri ormonali, che per non risultando pericolosa nell'immediato può predisporre allo sviluppo di altre malattie.<ref>{{Cita pubblicazione|nome=Marcin|cognome=Stankiewicz|data=2006|titolo=Diagnosis and management of polycystic ovary syndrome: a practical guide|rivista=Drugs|volume=66|numero=7|pp=903–912|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/16740005|nome2=Robert|cognome2=Norman}}</ref><ref>{{Cita pubblicazione|nome=A.|cognome=Daniilidis|data=April 2009|titolo=Long term health consequences of polycystic ovarian syndrome: a review analysis|rivista=Hippokratia|volume=13|numero=2|pp=90–92|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/19561777|nome2=K.|cognome2=Dinas}}</ref> In studi in doppio cieco è stato dimostrato che l'inositolo è un trattamento efficace e sicuro contemporaneamente per diverse manifestazioni cliniche della sindrome dell'ovaio policistico (PCOS) tra cui l'insulino-resistenza, [[iperandrogenismo]],<ref>{{Cita pubblicazione|nome=D.|cognome=Costantino|data=March 2009|titolo=Metabolic and hormonal effects of myo-inositol in women with polycystic ovary syndrome: a double-blind trial|rivista=European Review for Medical and Pharmacological Sciences|volume=13|numero=2|pp=105–110|accesso=2017-06-24|url=https://www.ncbi.nlm.nih.gov/pubmed/19499845|nome2=G.|cognome2=Minozzi|nome3=E.|cognome3=Minozzi}}</ref> fertilità (in maniera piu efficacie rispetto alla metformina)<ref>{{Cita pubblicazione|nome=Emanuela|cognome=Raffone|data=April 2010|titolo=Insulin sensitiser agents alone and in co-treatment with r-FSH for ovulation induction in PCOS women|rivista=Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology|volume=26|numero=4|pp=275–280|accesso=2017-06-24|doi=10.3109/09513590903366996|url=http://www.ncbi.nlm.nih.gov/pubmed/20222840|nome2=Pietro|cognome2=Rizzo|nome3=Vincenzo|cognome3=Benedetto}}</ref><ref>{{Cita pubblicazione|nome=Enrico|cognome=Papaleo|data=December 2007|titolo=Myo-inositol in patients with polycystic ovary syndrome: a novel method for ovulation induction|rivista=Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology|volume=23|numero=12|pp=700–703|accesso=2017-06-24|doi=10.1080/09513590701672405|url=http://www.ncbi.nlm.nih.gov/pubmed/17952759|nome2=Vittorio|cognome2=Unfer|nome3=Jean-Patrice|cognome3=Baillargeon}}</ref> e [[oligoamenorrea]], sia con DCI<ref>{{Cita pubblicazione| autore= Nestler J E, Jakubowicz D J, Reamer P, Gunn R D, Allan G| titolo= Ovulatory and metabolic effects of D-chiro-inositol in the polycystic ovary syndrome| rivista= N Engl J Med| anno= 1999| volume= 340| numero= 17| pp= 1314–1320| pmid= 10219066| doi= 10.1056/NEJM199904293401703}}</ref><ref>{{Cita pubblicazione| autore= Iuorno M J, Jakubowicz D J, Baillargeon J P, Dillon P, Gunn R D, Allan G, Nestler J E| titolo= Effects of d-chiro-inositol in lean women with the polycystic ovary syndrome| rivista= Endocr Pract| anno= 2002| volume= 8| numero= 6| pp= 417–423| pmid= 15251831}}</ref> che con mio-inositolo a dosaggi di 2 grammi al giorno<ref>{{Cita pubblicazione|nome=V.|cognome=Unfer|data=July 2012|titolo=Effects of myo-inositol in women with PCOS: a systematic review of randomized controlled trials|rivista=Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology|volume=28|numero=7|pp=509–515|accesso=2017-06-24|doi=10.3109/09513590.2011.650660|url=https://www.ncbi.nlm.nih.gov/pubmed/22296306|nome2=G.|cognome2=Carlomagno|nome3=G.|cognome3=Dante}}</ref><ref>{{Cita pubblicazione|nome=P. G.|cognome=Artini|data=April 2013|titolo=Endocrine and clinical effects of myo-inositol administration in polycystic ovary syndrome. A randomized study|rivista=Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology|volume=29|numero=4|pp=375–379|accesso=2017-06-24|doi=10.3109/09513590.2012.743020|url=https://www.ncbi.nlm.nih.gov/pubmed/23336594|nome2=O. M.|cognome2=Di Berardino|nome3=F.|cognome3=Papini}}</ref> che con loro combinazioni che si crebe abbia un effetto sinergico (ad esempio a dosaggi di 2 g e 0,2 g rispettivamente di mio e D-chiro inositolo).<ref>{{Cita pubblicazione|nome=Franco|cognome=Lisi|data=2012-07-23|titolo=Pretreatment with myo-inositol in non polycystic ovary syndrome patients undergoing multiple follicular stimulation for IVF: a pilot study|rivista=Reproductive biology and endocrinology: RB&E|volume=10|pp=52|accesso=2017-06-24|doi=10.1186/1477-7827-10-52|url=http://www.ncbi.nlm.nih.gov/pubmed/22823904|nome2=Piero|cognome2=Carfagna|nome3=Mario Montanino|cognome3=Oliva}}</ref> Alcuni studi hanno evidenziato come il loro effetto possa essere aumentato con l'integrazione di melatonina.<ref>{{Cita pubblicazione|nome=Vittorio|cognome=Unfer|data=November 2011|titolo=Effect of a supplementation with myo-inositol plus melatonin on oocyte quality in women who failed to conceive in previous in vitro fertilization cycles for poor oocyte quality: a prospective, longitudinal, cohort study|rivista=Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology|volume=27|numero=11|pp=857–861|accesso=2017-06-24|doi=10.3109/09513590.2011.564687|url=http://www.ncbi.nlm.nih.gov/pubmed/21463230|nome2=Emanuela|cognome2=Raffone|nome3=Piero|cognome3=Rizzo}}</ref><ref>{{Cita pubblicazione|nome=P.|cognome=Rizzo|data=June 2010|titolo=Effect of the treatment with myo-inositol plus folic acid plus melatonin in comparison with a treatment with myo-inositol plus folic acid on oocyte quality and pregnancy outcome in IVF cycles. A prospective, clinical trial|rivista=European Review for Medical and Pharmacological Sciences|volume=14|numero=6|pp=555–561|accesso=2017-06-24|url=http://www.ncbi.nlm.nih.gov/pubmed/20712264|nome2=E.|cognome2=Raffone|nome3=V.|cognome3=Benedetto}}</ref> |
|||
| ⚫ | Questi studi hanno dimostrato che esistono difetti nel metabolismo del [[D-chiro-inositolo|DCI]] nella sindrome dell'ovaio policistico che possono essere corretti da una sua integrazione, chiarendo così il conseguente ruolo del DCI nella trasduzione del segnale dell'insulina.<ref name="Larner J 2002 47–60">{{Cita pubblicazione| autore= Larner J| titolo= D-chiro-inositol--its functional role in insulin action and its deficit in insulin resistance |
||
Molto promettenti ed ormai numericamente consistenti sono gli studi che dimostrano l'utilità del D- chiro -inositolo (DCI) nel trattamento della PCOS (sindrome dell'[[ovaio policistico]]). Infatti, è stato trovato in studi in doppio cieco che esso è un trattamento efficace per diverse manifestazioni cliniche della sindrome dell'ovaio policistico (PCOS), tra cui l'insulino-resistenza, [[iperandrogenismo]], e [[oligoamenorrea]].<ref>{{Cita pubblicazione| autore= Nestler J E, Jakubowicz D J, Reamer P, Gunn R D, Allan G| titolo= Ovulatory and metabolic effects of D-chiro-inositol in the polycystic ovary syndrome| rivista= N Engl J Med| anno= 1999| volume= 340| numero= 17| pp= 1314–1320| pmid= 10219066| doi= 10.1056/NEJM199904293401703}}</ref><ref>{{Cita pubblicazione| autore= Iuorno M J, Jakubowicz D J, Baillargeon J P, Dillon P, Gunn R D, Allan G, Nestler J E| titolo= Effects of d-chiro-inositol in lean women with the polycystic ovary syndrome| rivista= Endocr Pract| anno= 2002| volume= 8| numero= 6| pp= 417–423| pmid= 15251831}}</ref> |
|||
| ⚫ | Questi studi hanno dimostrato che esistono difetti |
||
| rivista= Int J Exp Diabetes Res| anno= 2002| volume= 3| numero= 1| pp= 47–60| pmid= 11900279| doi= 10.1080/15604280212528| pmc= 2478565}}</ref><ref name="Nestler-2000">{{Cita pubblicazione | cognome = Nestler | nome = JE. | coautori = DJ. Jakubowicz; MJ. Iuorno | titolo = Role of inositolphosphoglycan mediators of insulin action in the polycystic ovary syndrome. | rivista = J Pediatr Endocrinol Metab | volume = 13 Suppl 5 | pp = 1295-8 | anno = 2000 | pmid = 11117673 }}</ref> |
| rivista= Int J Exp Diabetes Res| anno= 2002| volume= 3| numero= 1| pp= 47–60| pmid= 11900279| doi= 10.1080/15604280212528| pmc= 2478565}}</ref><ref name="Nestler-2000">{{Cita pubblicazione | cognome = Nestler | nome = JE. | coautori = DJ. Jakubowicz; MJ. Iuorno | titolo = Role of inositolphosphoglycan mediators of insulin action in the polycystic ovary syndrome. | rivista = J Pediatr Endocrinol Metab | volume = 13 Suppl 5 | pp = 1295-8 | anno = 2000 | pmid = 11117673 }}</ref> |
||
Versione delle 15:55, 24 giu 2017
| Inositolo | |
|---|---|
 | |
 | |
| Nome IUPAC | |
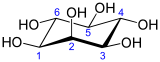
| cis-1,2,3,5-trans-4,6-cicloesanesolo | |
| Abbreviazioni | |
| mio-inositolo | |
| Nomi alternativi | |
| cicloesanesolo, cicloesitolo, dambosio, inositale, inosite, iso-inositolo, inositene, inositina, i-inositolo, MI, Meat sugar, mesoinosite, meso-inositolo, mesolo, mesovite, Mioinosite, fattore antialopecia del topo, nucite, faseomannite, faseomannitolo, scyllite (per l'isomero scyllo-inositolo) | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C6H12O6 |
| Massa molecolare (u) | 180.16 g/mol |
| Numero CAS | |
| Numero EINECS | 230-024-9 |
| PubChem | 892 |
| SMILES | C1(C(C(C(C(C1O)O)O)O)O)O |
| Indicazioni di sicurezza | |
| Frasi H | --- |
| Consigli P | ---[1] |
L'inositolo (chiamato a volte anche vitamina B7) è un composto di origine biologica, strutturalmente simile al glucosio (anche se chimicamente non è uno zucchero) coinvolto in numero processi biologici tra cui quelli di signalling cellulare e come elemento strutturale. Può essere sia assunto con dieta che sintetizzato dal corpo umano, dove può presentare un grado più. In particolare, il mio-inositlo è la forma che non presenta gruppi fosforici legati.
Chimica
Con inositolo ci si riferisce ad una famiglia di molecole dalla struttura simile che differiscono per essere stereoisomeri. Chimicamente gli inositoli sono dei polioli carbociclici, non sono uno zucchero essendo i monosaccaridi, nella loro forma ciclica, emiacetali o emichetali (struttura eterociclica contenente ossigeno). La forma più importante in natura è il myo-inositolo (cis-1,2,3,5-trans-4,6-cicloesanesolo) ma occasionalmnete si rilevano altri isomeri confermazionali che differiscono solamente per il differente orientamento dei gruppi -OH, come scyllo-, chiro-, muco-, neo-inositolo. Altri isomeri possibili sono il allo-, epi-, cis-inositolo. Quando ci si riferisce agli integratori alimentari, generalmente si intende il mio-inositolo.
Nella sua conformazione più stabile il mio-inositolo assume la conformazione a sedia, in cui 5 idrossili sono posti in conformazione equaotoriale ed 1 in conformazione assiale (quello in C2) che si presenta come una polvere di bassa palpabilità, di colore bianco niveo, inodore, dal sapore lievemente dolce.
Presenza in natura e sintesi
L'inositolo si trova in molti alimenti, in particolare nei cereali, nelle noci, nella frutta specialmente in meloni ed arance dove si ritrova molto spesso essi insolubili di difficile assorbimento, per questo motivo l'inositolo contentuto negli alimenti è spesso scarsamente asssorbibile. L'inositolo non è in realtà una vitamina (anche se è spesso conosciuto come Vitamina B7), perchè a differenza di queste, l'organismo è in grado di sintetizzarlo in quantità sufficiente per cui ricade nella classe delle pseudovitamine nel complesso B.
Il mio-Inositolo è sintetizzato a partire dal glucosio-6 fosfato in due passaggi: il primo, catalizzato da una inositolo-3 fosfato sintasi (come ISYNA1) lo converte in mio-inositolo-1 fosfato, che viene poi defosforilato a mio-inositolo da una fosfatasi. Negli umani la maggior parte dell'inositolo, generralmente alcuni grammi al giorni) viene sintetizzato nei reni.
Acido fitico
L'acido fitico (IP6 o fitato), è un derivato dell'inositolo formato da una mlecola di inositolo a cui sono legati gruppi fosfato al posto degli -OH e rappresenta la principale forma di stoccaggio di fosforo inorganico in molte pecie vegetali, specie nei semi.[2] L'acido fitico è inassorbibile dagli organismi superiori, a parte i ruminanti, perchè non possiedono nel loro apparato digestivo i batteri e gli enzimi in grado di degradare questo composto. Inoltre l'acido fitico, per via della sua capacità di legare ioni metallici come calcio, magnesio, zinco e ferro, può esacerbare stati di carenza di minerali in soggetti predisposti che mangiano grandi quantità di vegetali (come accade ad esempio nei paesi in via di sviluppo).[3][4]

Ruolo biologico e applicazioni
L'inositolo ed i suoi derivati partecipano a numerosi e fondamentali processi biologici, quali:
- Trasduzione del segnale dell'insulina Insulin [5]
- Formazione del citoscheletro
- Sistema nervoso (epsina)
- Controllo della concentrazione di calcio intracellulare [6]
- Mantenimento del potenziale di membrana cellulare [7]
- Degradazione dei grassi [8]
- Regolazione dell'espressione genica [9][10]
Dalla sua fosforilazione si possono ottenere fino a 70 diverse molecole (raccolti in dei gruppi in base al numero di gruppi fosfato presenti, IP1-IP9), ognuno con un diverso ruolo nel signalling intracellulare. Inoltre possono essere legate a numerosi altri composti come ad esempio i lipidi, per formare i fosfatidilinositoli polifosfati.[11]
Farmacologia
L'Inositolo è assorbito mediante un sistema di co-trasporto sodio dipendente che media anche l'assorbimento di glucosio (l'integrazione di inositolo si è infatti dimostrata in grado di limitare quella di glucosio).[12] L'applicazione di soft gel all'inositolo (delle capsule riempite di liquido in modo da eliminare steps limitanti come la dissoluzione) ha permesso di incrementare notevolmente la biodisponibilità orale del composto del 30%.[13]
Dopo l'ingestione, l'inositolo raggiunge il picco plasmatico in circa 2-3 ore.[14] Nell'organismo viene convertito rapidamente in alcuni isomeri come epi- e D-chiro- da delle epimerasi, alcune delle quali risultano essere presenti in bassa quantità nei soggetti con insulino resistenza, e che vengono saturarate rapidamente da dosi medie (alcuni grammi) del composto.[15] L'inositolo ha mostrato efficacia in alcuni disturbi psichiatrici ma ha una bassa permeabilità nella barriera ematoencefalica (meno del 3% della concentrazione del composto circolante riesce ad attraversarla)[16], che però tende ad aumentare nel corso di un trattamento continuato: il trattamento con 12 g al giorno del composto ha comportato un aumento del 70% dei livelli di inositolo nel fluido cererbrospinale di pazienti. [17]
Usi terapeutici
La struttura dell'inositolo gioca un ruolo fondamentale nei messaggeri secondari in cellule eucariotiche, come inositolo fosfato o come lipidi fosfatidilinositolo (PI) e fosfatidilinositolofosfato (PIP). Questa sua prorpietà sembra essere la responsabile dei suoi effetti teraputici, alcuni dei quali provati anche in test clinici su pazienti. Il mio inositolo è considerato come un composto sicuro ed è inoltre idrosolubile (al pari di altri composti del complesso delle vitamine B) che ne previene un eccessivo accumulo. La sua deplezione alimentare non sembra causare stati patologici, proprio grazie alla capacità del corpo di sintetizzarlo, ma la sua integrazione si è mostrata capace di agire su diverse patologie, in particolare disturbi d'ansia, sindrome dell'ovaio policistico, sindromi metaboliche senza causare effetti collaterali rilevanti (si possono presentare disturbi gastro intestinali nel 5% dei pazienti specie ai dosaggi piu alti).
Sistema nervoso centrale
L'inositolo ed i suoi derivati sembrano giocare un ruolo fondamentale nell'equilibrio del sistema nervoso centrale, anche se le sue numerosi implicazioni non sono state ancora del tutto delucidate. Bassi livelli di mio-inositolo sono stati rilevati nel cervello di pazienti depressi e di suicidi;[18] i sali di litio, uno dei trattamenti di prima linea per il disturbo bipolare, vanno tra le altre cose ad alterare i livelli di inositoli nel cervello.[19] Perciò il mio-inositolo è stato sperimentato nel trattamento di diverse patologie psichiatriche.[20]
Disturbi depressivi ed ansia
Sembra avere qualche efficacia nel trattamento della depressione (a dosaggi superiori a 12 g\giorno) dove in alcuni studi ha mostrato una diminuzione statisticamente significativa rispetto al placebo dei sintomi (da 33.4 a 21.6 in media nei pazienti trattati con inositolo, rispetto 32.9 to 28.9 nel gruppo placebo placebo misurati con la scala HDS secondo i risultati di uno studio).[21][22] Alcuni pazienti che non hanno risposto al trattamento con inositolo hanno trovato beneficio con un SSRI, ma l'aggiunta di inositolo ad un SSRI non sembra fornire benefici aggiuntivi all'effetto dell'antidepressivo.[23][24]
Il myo-inositolo (al dosaggio di 18 g\giorno) in studi in doppio cieco è risultato efficace nel trattamento del disturbo ossessivo-compulsivo quanto gli SSRI, dei farmaci antidepressivi utilizzati come trattamento per questa patologia, ma a differenza di questi è risultato virtualmente privo di effetti collaterali.[25][26]
In un altro studio, inositolo al dosaggio di 18 grammi al giorno, è risultato efficacie quanto fluvoxamina (un antidepressivo SSRI) nel trattamento del disturbo da attacchi di panico.[27] Sembra che anche una dose minore (di 12 g\giorno) possa avere una qualche efficacia.[28] Sembra che la sua efficacia come ansiolitico dipenda dalla gravità iniziale della patologia, fornendo i benefici maggiori nei pazienti con disturbo grave.[29]
Disturbo disforico mestruale
Il disturbo disforico premestruale è un disordine dell'umore associato alla sindrome premestruale.[30] Lintegrazione di 4 g di inositolo 3 volte al giorno ha mostrato in uno studio di diminuire i disturbi dell'umore e di depressione ed ansia in maniera statisticamente significativa, questi effetti benefici si sono mantenuti per i 6 mesi del trattamento. Tuttavia non sono stati condotti numerosi studi per replicare i risultati.[31]
L'inositolo è stato sperimentato anche nel trattamento di disturbo post traumatico da stress,[32] disturbo bipolare,[33] schizofrenia[34] e per il morbo di Alzheimer[35][36] non mostrando però in questi casi efficacia significativa.
Sindrome metabolica e diabete
La sindrome metabolica è una patologia complessa e multifattoriale nella quale diversi fattori fra loro correlati concorrono ad aumentare la possibilità di sviluppare patologie a carico dell'apparato circolatorio e diabete.
L'inositolo fa parte di una serie di composti che attivano la risposta dell'insulina all'interno della cellula[37] (è uno dei principali messaggeri secondari) di cui fanno parte i "fosfoglicani legati all'inositolo" di tipo A (IGP-A) e quelli di tipo P (IGP-P o D-chiro-inositolo legato a galattosamine).[38] Questi composti hanno delle funzioni opposte all'interno del metabolismo e tendono ad antagonizzarsi, per cui il loro bilancio è essenziale al corretto funzionamento dell'organismo e l'insulino resistenza è associata ad uno sbilanciamento di questi sistemi.[39] L'inositolo sembra agire normalizzando il rapporto tra questi composti.[40]
L'insulina promuove l'ingresso di glucosio nelle cellule anche attraverso la mobilitazione delle riserve vescicolari dei trasportatori del glucosio (GluT4), delle proteine trasportatrici di membrana che grazie all'attivazione di una serie di messaggeri chimici, di cui fanno parte dei derivati fosforilati dell'inositolo come il PIP3, vengono trasportati nella membrana.[41][42] In dei modelli animali, l'ingestione di inositolo ha promosso l'espressione dei trasportatori del glucosio e quindi dimiuito l'insulino resistenza.[43]Inoltre l'integrazione con inositolo 10g\giorno si è mostrata in grado di diminuire il colesterolo LDL nelle persone con sindrome metabolica (ma non nei pazienti che non la hanno) probabilmente come effetto secondario all'aumento di particolari lipoproteine prodotte dai reni (i plasmalogeni) la cui quantitò tende a diminuire con l'età e in soggetti con iperlipidemie.[44][45]
In uno studio, in delle donne con sindrome metabolica post menopausa, l'integrazione con inositolo alla dose di 2 grammi al giorno ha causato il miglioramento dei marker metabolici per la malattia (livelli di insulina, glucosio ed insulino resistenza) che si sono mantenuti durane te tutta la durata dello studio (un anno) mostrando anzi un lieve ulteriore miglioramento nel corso dei mesi.[46] [47] Usato al dosaggio di 4g\giorno, in uno studio ha mostrato di diminuire i marker di diabete gestionale nelle donne incinte (in particolare livelli di glucosio ed insulino resistenza) [48] e di diminuire il rischio di sviluppo di diabete gestionale nelle donne con ovaio policistico dal 52% al 17,2%, senza però influire sull'andamento della gravidanza.[49][50]
Sindrome dell'ovaio policistico
Molto promettenti ed ormai numericamente consistenti sono gli studi che dimostrano l'utilità dell'inositolo, ed in particolare del D-chiro-inositolo (DCI), nel trattamento della sindrome dell'ovaio policistico (PCOS), una sindrome caratterizzata tra l'altro da scarso controllo del glucosio ematico, iperandrogenismo, squilibri ormonali, che per non risultando pericolosa nell'immediato può predisporre allo sviluppo di altre malattie.[51][52] In studi in doppio cieco è stato dimostrato che l'inositolo è un trattamento efficace e sicuro contemporaneamente per diverse manifestazioni cliniche della sindrome dell'ovaio policistico (PCOS) tra cui l'insulino-resistenza, iperandrogenismo,[53] fertilità (in maniera piu efficacie rispetto alla metformina)[54][55] e oligoamenorrea, sia con DCI[56][57] che con mio-inositolo a dosaggi di 2 grammi al giorno[58][59] che con loro combinazioni che si crebe abbia un effetto sinergico (ad esempio a dosaggi di 2 g e 0,2 g rispettivamente di mio e D-chiro inositolo).[60] Alcuni studi hanno evidenziato come il loro effetto possa essere aumentato con l'integrazione di melatonina.[61][62]
Questi studi hanno dimostrato che esistono difetti nel metabolismo del DCI nella sindrome dell'ovaio policistico che possono essere corretti da una sua integrazione, chiarendo così il conseguente ruolo del DCI nella trasduzione del segnale dell'insulina.[5][63]
Note
- ^ Sigma Aldrich; rev. del 06.07.2012
- ^ Phytic acid
- ^ Hurrell RF, Influence of vegetable protein sources on trace element and mineral bioavailability, in The Journal of Nutrition, vol. 133, n. 9, 2003, pp. 2973S–7S.
- ^ Committee on Food Protection, Phytates, in Toxicants Occurring Naturally in Foods, National Academy of Sciences, 1973, pp. 363–371, ISBN 978-0-309-02117-3.
- ^ a b Larner J, D-chiro-inositol--its functional role in insulin action and its deficit in insulin resistance, in International Journal of Experimental Diabetes Research, vol. 3, n. 1, 2002, pp. 47–60, DOI:10.1080/15604280212528. Errore nelle note: Tag
<ref>non valido; il nome "Larner J 2002 47–60" è stato definito più volte con contenuti diversi - ^ Gerasimenko JV, Flowerdew SE, Voronina SG, Sukhomlin TK, Tepikin AV, Petersen OH, Gerasimenko OV, Bile acids induce Ca2+ release from both the endoplasmic reticulum and acidic intracellular calcium stores through activation of inositol trisphosphate receptors and ryanodine receptors, in The Journal of Biological Chemistry, vol. 281, n. 52, 2006, pp. 40154–63, DOI:10.1074/jbc.M606402200.
- ^ Kukuljan M, Vergara L, Stojilkovic SS, Modulation of the kinetics of inositol 1,4,5-trisphosphate-induced [Ca2+]i oscillations by calcium entry in pituitary gonadotrophs, in Biophysical Journal, vol. 72, 2 Pt 1, 1997, pp. 698–707, DOI:10.1016/S0006-3495(97)78706-X.
- ^ Rapiejko PJ, Northup JK, Evans T, Brown JE, Malbon CC, G-proteins of fat-cells. Role in hormonal regulation of intracellular inositol 1,4,5-trisphosphate, in The Biochemical Journal, vol. 240, n. 1, 1986, pp. 35–40.
- ^ Shen X, Xiao H, Ranallo R, Wu WH, Wu C, Modulation of ATP-dependent chromatin-remodeling complexes by inositol polyphosphates, in Science, vol. 299, n. 5603, 2003, pp. 112–4, DOI:10.1126/science.1078068.
- ^ Steger DJ, Haswell ES, Miller AL, Wente SR, O'Shea EK, Regulation of chromatin remodeling by inositol polyphosphates, in Science, vol. 299, n. 5603, 2003, pp. 114–6, DOI:10.1126/science.1078062.
- ^ Marine L. Croze e Christophe O. Soulage, Potential role and therapeutic interests of myo-inositol in metabolic diseases, in Biochimie, vol. 95, n. 10, October 2013, pp. 1811–1827, DOI:10.1016/j.biochi.2013.05.011. URL consultato il 24 giugno 2017.
- ^ Michael J. Coady, Bernadette Wallendorff e Dominique G. Gagnon, Identification of a novel Na+/myo-inositol cotransporter, in The Journal of Biological Chemistry, vol. 277, n. 38, 20 settembre 2002, pp. 35219–35224, DOI:10.1074/jbc.M204321200. URL consultato il 24 giugno 2017.
- ^ Gianfranco Carlomagno, Sara De Grazia e Vittorio Unfer, Myo-inositol in a new pharmaceutical form: a step forward to a broader clinical use, in Expert Opinion on Drug Delivery, vol. 9, n. 3, March 2012, pp. 267–271, DOI:10.1517/17425247.2012.662953. URL consultato il 24 giugno 2017.
- ^ Gianfranco Carlomagno, Sara De Grazia e Vittorio Unfer, Myo-inositol in a new pharmaceutical form: a step forward to a broader clinical use, in Expert Opinion on Drug Delivery, vol. 9, n. 3, March 2012, pp. 267–271, DOI:10.1517/17425247.2012.662953. URL consultato il 24 giugno 2017.
- ^ Joseph Larner, D-chiro-inositol--its functional role in insulin action and its deficit in insulin resistance, in International Journal of Experimental Diabetes Research, vol. 3, n. 1, 2002, pp. 47–60, DOI:10.1080/15604280212528. URL consultato il 24 giugno 2017.
- ^ R. Spector, Myo-inositol transport through the blood-brain barrier, in Neurochemical Research, vol. 13, n. 8, August 1988, pp. 785–787. URL consultato il 24 giugno 2017.
- ^ J. Levine, A. Rapaport e L. Lev, Inositol treatment raises CSF inositol levels, in Brain Research, vol. 627, n. 1, 5 novembre 1993, pp. 168–170. URL consultato il 24 giugno 2017.
- ^ H. Shimon, G. Agam e R. H. Belmaker, Reduced frontal cortex inositol levels in postmortem brain of suicide victims and patients with bipolar disorder, in The American Journal of Psychiatry, vol. 154, n. 8, August 1997, pp. 1148–1150, DOI:10.1176/ajp.154.8.1148. URL consultato il 24 giugno 2017.
- ^ H. K. Manji, Y. Bersudsky e G. Chen, Modulation of protein kinase C isozymes and substrates by lithium: the role of myo-inositol, in Neuropsychopharmacology: Official Publication of the American College of Neuropsychopharmacology, vol. 15, n. 4, October 1996, pp. 370–381, DOI:10.1016/0893-133X(95)00243-7. URL consultato il 24 giugno 2017.
- ^ J. Levine, Controlled trials of inositol in psychiatry, in European Neuropsychopharmacology: The Journal of the European College of Neuropsychopharmacology, vol. 7, n. 2, May 1997, pp. 147–155. URL consultato il 24 giugno 2017.
- ^ J. Levine, Y. Barak e M. Gonzalves, Double-blind, controlled trial of inositol treatment of depression, in The American Journal of Psychiatry, vol. 152, n. 5, May 1995, pp. 792–794, DOI:10.1176/ajp.152.5.792. URL consultato il 24 giugno 2017.
- ^ J. Levine, Y. Barak e O. Kofman, Follow-up and relapse analysis of an inositol study of depression, in The Israel Journal of Psychiatry and Related Sciences, vol. 32, n. 1, 1995, pp. 14–21. URL consultato il 24 giugno 2017.
- ^ B. Nemets, A. Mishory e J. Levine, Inositol addition does not improve depression in SSRI treatment failures, in Journal of Neural Transmission (Vienna, Austria: 1996), vol. 106, n. 7-8, 1999, pp. 795–798, DOI:10.1007/s007020050200. URL consultato il 24 giugno 2017.
- ^ J. Levine, A. Mishori e M. Susnosky, Combination of inositol and serotonin reuptake inhibitors in the treatment of depression, in Biological Psychiatry, vol. 45, n. 3, 1º febbraio 1999, pp. 270–273. URL consultato il 24 giugno 2017.
- ^ S. Seedat e D. J. Stein, Inositol augmentation of serotonin reuptake inhibitors in treatment-refractory obsessive-compulsive disorder: an open trial, in International Clinical Psychopharmacology, vol. 14, n. 6, November 1999, pp. 353–356. URL consultato il 24 giugno 2017.
- ^ Fux M, Levine J, Aviv A, Belmaker RH, Inositol treatment of obsessive-compulsive disorder, in American Journal of Psychiatry, vol. 153, n. 9, 1996, pp. 1219–21, PMID 8780431.
- ^ A. Palatnik, K. Frolov e M. Fux, Double-blind, controlled, crossover trial of inositol versus fluvoxamine for the treatment of panic disorder, in Journal of Clinical Psychopharmacology, vol. 21, n. 3, June 2001, pp. 335–339. URL consultato il 24 giugno 2017.
- ^ J. Benjamin, J. Levine e M. Fux, Double-blind, placebo-controlled, crossover trial of inositol treatment for panic disorder, in The American Journal of Psychiatry, vol. 152, n. 7, July 1995, pp. 1084–1086, DOI:10.1176/ajp.152.7.1084. URL consultato il 24 giugno 2017.
- ^ O. Kofman, H. Einat e H. Cohen, The anxiolytic effect of chronic inositol depends on the baseline level of anxiety, in Journal of Neural Transmission (Vienna, Austria: 1996), vol. 107, n. 2, 2000, pp. 241–253, DOI:10.1007/s007020050020. URL consultato il 24 giugno 2017.
- ^ I. Zukov, R. Ptácek e J. Raboch, Premenstrual dysphoric disorder--review of actual findings about mental disorders related to menstrual cycle and possibilities of their therapy, in Prague Medical Report, vol. 111, n. 1, 2010, pp. 12–24. URL consultato il 24 giugno 2017.
- ^ Carlomagno Gianfranco, Unfer Vittorio e Buffo Silvia, Myo-inositol in the treatment of premenstrual dysphoric disorder, in Human Psychopharmacology, vol. 26, n. 7, October 2011, pp. 526–530, DOI:10.1002/hup.1241. URL consultato il 24 giugno 2017.
- ^ Z. Kaplan, M. Amir e M. Swartz, Inositol treatment of post-traumatic stress disorder, in Anxiety, vol. 2, n. 1, 1996, pp. 51–52, DOI:10.1002/(SICI)1522-7154(1996)2:13.0.CO;2-G. URL consultato il 24 giugno 2017.
- ^ Andrew A. Nierenberg, Michael J. Ostacher e Joseph R. Calabrese, Treatment-resistant bipolar depression: a STEP-BD equipoise randomized effectiveness trial of antidepressant augmentation with lamotrigine, inositol, or risperidone, in The American Journal of Psychiatry, vol. 163, n. 2, February 2006, pp. 210–216, DOI:10.1176/appi.ajp.163.2.210. URL consultato il 24 giugno 2017.
- ^ J. Levine, R. Umansky e G. Ezrielev, Lack of effect of inositol treatment in chronic schizophrenia, in Biological Psychiatry, vol. 33, n. 8-9, 1993 Apr 15-May 1, pp. 673–675. URL consultato il 24 giugno 2017.
- ^ Y. Barak, J. Levine e A. Glasman, Inositol treatment of Alzheimer's disease: a double blind, cross-over placebo controlled trial, in Progress in Neuro-Psychopharmacology & Biological Psychiatry, vol. 20, n. 4, May 1996, pp. 729–735. URL consultato il 24 giugno 2017.
- ^ S. Salloway, R. Sperling e R. Keren, A phase 2 randomized trial of ELND005, scyllo-inositol, in mild to moderate Alzheimer disease, in Neurology, vol. 77, n. 13, 27 settembre 2011, pp. 1253–1262, DOI:10.1212/WNL.0b013e3182309fa5. URL consultato il 24 giugno 2017.
- ^ A. R. Saltiel, Second messengers of insulin action, in Diabetes Care, vol. 13, n. 3, March 1990, pp. 244–256. URL consultato il 24 giugno 2017.
- ^ H. N. Caro, S. Kunjara e T. W. Rademacher, Isolation and partial characterisation of insulin-mimetic inositol phosphoglycans from human liver, in Biochemical and Molecular Medicine, vol. 61, n. 2, August 1997, pp. 214–228. URL consultato il 24 giugno 2017.
- ^ S. Kunjara, D. Y. Wang e A. L. Greenbaum, Inositol phosphoglycans in diabetes and obesity: urinary levels of IPG A-type and IPG P-type, and relationship to pathophysiological changes, in Molecular Genetics and Metabolism, vol. 68, n. 4, December 1999, pp. 488–502, DOI:10.1006/mgme.1999.2936. URL consultato il 24 giugno 2017.
- ^ J. Larner, D-chiro-inositol in insulin action and insulin resistance-old-fashioned biochemistry still at work, in IUBMB life, vol. 51, n. 3, March 2001, pp. 139–148, DOI:10.1080/152165401753544205. URL consultato il 24 giugno 2017.
- ^ Anne M. Kong, Kristy A. Horan e Absorn Sriratana, Phosphatidylinositol 3-phosphate [PtdIns3P] is generated at the plasma membrane by an inositol polyphosphate 5-phosphatase: endogenous PtdIns3P can promote GLUT4 translocation to the plasma membrane, in Molecular and Cellular Biology, vol. 26, n. 16, August 2006, pp. 6065–6081, DOI:10.1128/MCB.00203-06. URL consultato il 24 giugno 2017.
- ^ Akihiko Taguchi, Masahiro Emoto e Shigeru Okuya, Identification of Glypican3 as a novel GLUT4-binding protein, in Biochemical and Biophysical Research Communications, vol. 369, n. 4, 16 maggio 2008, pp. 1204–1208, DOI:10.1016/j.bbrc.2008.03.027. URL consultato il 24 giugno 2017.
- ^ Yoko Yamashita, Masaru Yamaoka e Tomohisa Hasunuma, Detection of orally administered inositol stereoisomers in mouse blood plasma and their effects on translocation of glucose transporter 4 in skeletal muscle cells, in Journal of Agricultural and Food Chemistry, vol. 61, n. 20, 22 maggio 2013, pp. 4850–4854, DOI:10.1021/jf305322t. URL consultato il 24 giugno 2017.
- ^ Ryouta Maeba, Hiroshi Hara e Hiroshi Ishikawa, Myo-inositol treatment increases serum plasmalogens and decreases small dense LDL, particularly in hyperlipidemic subjects with metabolic syndrome, in Journal of Nutritional Science and Vitaminology, vol. 54, n. 3, June 2008, pp. 196–202. URL consultato il 24 giugno 2017.
- ^ Ryouta Maeba, Tomomi Maeda e Makoto Kinoshita, Plasmalogens in human serum positively correlate with high- density lipoprotein and decrease with aging, in Journal of Atherosclerosis and Thrombosis, vol. 14, n. 1, February 2007, pp. 12–18. URL consultato il 24 giugno 2017.
- ^ Domenico Giordano, Francesco Corrado e Angelo Santamaria, Effects of myo-inositol supplementation in postmenopausal women with metabolic syndrome: a perspective, randomized, placebo-controlled study, in Menopause (New York, N.Y.), vol. 18, n. 1, January 2011, pp. 102–104, DOI:10.1097/gme.0b013e3181e8e1b1. URL consultato il 24 giugno 2017.
- ^ A. Santamaria, D. Giordano e F. Corrado, One-year effects of myo-inositol supplementation in postmenopausal women with metabolic syndrome, in Climacteric: The Journal of the International Menopause Society, vol. 15, n. 5, October 2012, pp. 490–495, DOI:10.3109/13697137.2011.631063. URL consultato il 24 giugno 2017.
- ^ F. Corrado, R. D'Anna e G. Di Vieste, The effect of myoinositol supplementation on insulin resistance in patients with gestational diabetes, in Diabetic Medicine: A Journal of the British Diabetic Association, vol. 28, n. 8, August 2011, pp. 972–975, DOI:10.1111/j.1464-5491.2011.03284.x. URL consultato il 24 giugno 2017.
- ^ R. D'Anna, V. Di Benedetto e P. Rizzo, Myo-inositol may prevent gestational diabetes in PCOS women, in Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology, vol. 28, n. 6, June 2012, pp. 440–442, DOI:10.3109/09513590.2011.633665. URL consultato il 24 giugno 2017.
- ^ G. Carlomagno e V. Unfer, Inositol safety: clinical evidences, in European Review for Medical and Pharmacological Sciences, vol. 15, n. 8, August 2011, pp. 931–936. URL consultato il 24 giugno 2017.
- ^ Marcin Stankiewicz e Robert Norman, Diagnosis and management of polycystic ovary syndrome: a practical guide, in Drugs, vol. 66, n. 7, 2006, pp. 903–912. URL consultato il 24 giugno 2017.
- ^ A. Daniilidis e K. Dinas, Long term health consequences of polycystic ovarian syndrome: a review analysis, in Hippokratia, vol. 13, n. 2, April 2009, pp. 90–92. URL consultato il 24 giugno 2017.
- ^ D. Costantino, G. Minozzi e E. Minozzi, Metabolic and hormonal effects of myo-inositol in women with polycystic ovary syndrome: a double-blind trial, in European Review for Medical and Pharmacological Sciences, vol. 13, n. 2, March 2009, pp. 105–110. URL consultato il 24 giugno 2017.
- ^ Emanuela Raffone, Pietro Rizzo e Vincenzo Benedetto, Insulin sensitiser agents alone and in co-treatment with r-FSH for ovulation induction in PCOS women, in Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology, vol. 26, n. 4, April 2010, pp. 275–280, DOI:10.3109/09513590903366996. URL consultato il 24 giugno 2017.
- ^ Enrico Papaleo, Vittorio Unfer e Jean-Patrice Baillargeon, Myo-inositol in patients with polycystic ovary syndrome: a novel method for ovulation induction, in Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology, vol. 23, n. 12, December 2007, pp. 700–703, DOI:10.1080/09513590701672405. URL consultato il 24 giugno 2017.
- ^ Nestler J E, Jakubowicz D J, Reamer P, Gunn R D, Allan G, Ovulatory and metabolic effects of D-chiro-inositol in the polycystic ovary syndrome, in N Engl J Med, vol. 340, n. 17, 1999, pp. 1314–1320, DOI:10.1056/NEJM199904293401703, PMID 10219066.
- ^ Iuorno M J, Jakubowicz D J, Baillargeon J P, Dillon P, Gunn R D, Allan G, Nestler J E, Effects of d-chiro-inositol in lean women with the polycystic ovary syndrome, in Endocr Pract, vol. 8, n. 6, 2002, pp. 417–423, PMID 15251831.
- ^ V. Unfer, G. Carlomagno e G. Dante, Effects of myo-inositol in women with PCOS: a systematic review of randomized controlled trials, in Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology, vol. 28, n. 7, July 2012, pp. 509–515, DOI:10.3109/09513590.2011.650660. URL consultato il 24 giugno 2017.
- ^ P. G. Artini, O. M. Di Berardino e F. Papini, Endocrine and clinical effects of myo-inositol administration in polycystic ovary syndrome. A randomized study, in Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology, vol. 29, n. 4, April 2013, pp. 375–379, DOI:10.3109/09513590.2012.743020. URL consultato il 24 giugno 2017.
- ^ Franco Lisi, Piero Carfagna e Mario Montanino Oliva, Pretreatment with myo-inositol in non polycystic ovary syndrome patients undergoing multiple follicular stimulation for IVF: a pilot study, in Reproductive biology and endocrinology: RB&E, vol. 10, 23 luglio 2012, pp. 52, DOI:10.1186/1477-7827-10-52. URL consultato il 24 giugno 2017.
- ^ Vittorio Unfer, Emanuela Raffone e Piero Rizzo, Effect of a supplementation with myo-inositol plus melatonin on oocyte quality in women who failed to conceive in previous in vitro fertilization cycles for poor oocyte quality: a prospective, longitudinal, cohort study, in Gynecological Endocrinology: The Official Journal of the International Society of Gynecological Endocrinology, vol. 27, n. 11, November 2011, pp. 857–861, DOI:10.3109/09513590.2011.564687. URL consultato il 24 giugno 2017.
- ^ P. Rizzo, E. Raffone e V. Benedetto, Effect of the treatment with myo-inositol plus folic acid plus melatonin in comparison with a treatment with myo-inositol plus folic acid on oocyte quality and pregnancy outcome in IVF cycles. A prospective, clinical trial, in European Review for Medical and Pharmacological Sciences, vol. 14, n. 6, June 2010, pp. 555–561. URL consultato il 24 giugno 2017.
- ^ JE. Nestler, DJ. Jakubowicz; MJ. Iuorno, Role of inositolphosphoglycan mediators of insulin action in the polycystic ovary syndrome., in J Pediatr Endocrinol Metab, 13 Suppl 5, 2000, pp. 1295-8, PMID 11117673.
Bibliografia
- Massimo Pandiani, Perché si ingrassa? Perdere peso e vivere in salute scegliendo la propria dieta, Tecniche Nuove, 2004, pp. 146–, ISBN 978-88-481-1679-4.
- Adam H. Balen, Polycystic ovary syndrome: a guide to clinical management, Taylor & Francis, 17 maggio 2005, pp. 136–, ISBN 978-1-84214-211-0.
- Victor Preedy, Ronald Ross Watson e Vinood Patel, Flour and Breads and Their Fortification in Health and Disease Prevention, Academic Press, 10 gennaio 2011, pp. 165–, ISBN 978-0-12-380886-8.
- Vivian A. Fonseca, Clinical diabetes: translating research into practice, Elsevier Health Sciences, 25 gennaio 2006, pp. 246–, ISBN 978-1-4160-0273-4.
- Christos S. Mantzoros, Obesity and diabetes, Springer, 25 gennaio 2006, pp. 269–, ISBN 978-1-58829-538-5.
- Nancy Dunne e William Slater, The Natural Diet Solution for PCOS and Infertility: How to Manage Polycystic Ovary Syndrome Naturally, Natural Solutions for PCOS, 1º marzo 2006, pp. 446–, ISBN 978-0-9772229-0-2.
- David E. Metzler e Carol M. Metzler, Biochemistry: the chemical reactions of living cells, Academic Press, 2003, pp. 998–, ISBN 978-0-12-492541-0.
- A. Lahiri Majumder e B. B. Biswas, Biology of inositols and phosphoinositides, Springer, 2006, pp. 64–, ISBN 978-0-387-27599-4.
- Duru Shah, R. K. Bhathena e Safala Shroff, Polycystic Ovary Syndrome, Orient Blackswan, 1º gennaio 2004, pp. 81–, ISBN 978-81-250-2633-4.
Collegamenti esterni
- (EN) IUPAC Gold Book, "inositols", su goldbook.iupac.org.